推荐产品
公司新闻/正文
miRNA研究进展盘点丨20240129期
人阅读 发布时间:2024-01-31 09:10
01
Bone-targeting engineered small extracellular vesicles carrying anti-miR-6359-CGGGAGC prevent valproic acid-induced bone loss
骨靶向工程化小细胞外囊泡携带anti-miR -6359-CGGGAGC可预防丙戊酸诱导的骨质流失
发表期刊:Signal Transduct Target Ther
影响因子:39.3
发表时间:2024年1月22日
丙戊酸(VPA)对骨稳态的临床作用和潜在机制仍存在争议。本研究证实了VPA治疗与患者和小鼠的骨量和骨密度(BMD)降低有关。这种效应归因于VPA诱导的破骨细胞形成和活性的升高。通过RNA测序,研究人员在体外观察到VPA处理的破骨细胞前体中前体miR-6359的表达显著升高,此外,使用定量实时PCR(qRT-PCR)和miR-6359荧光原位杂交(miR-6359-FISH)证明了成熟miR-6359(miR-6359)在体内的显著上调。具体而言,在VPA刺激后,miR-6359主要在破骨细胞前体和巨噬细胞中增加,但在中性粒细胞、T淋巴细胞、单核细胞和骨髓间充质干细胞(BMSC)中不增加,这影响了破骨细胞分化和骨吸收活性。此外,VPA诱导的破骨细胞前体中miR-6359的富集通过沉默SIRT3蛋白表达来增强活性氧(ROS)的产生,随后激活MAPK信号通路,从而增强破骨细胞的形成和活性,最终加速骨质流失。目前,尚无药物可以有效治疗VPA引起的骨质流失。因此,本研究通过在anti-miR-6359序列的3'-末端引入EXOmotif(CGGGAGC)来构建靶向骨内破骨细胞前体并天然携带anti-miR-6359的工程化小细胞外囊泡(E-sEVs)。结果证实了E-sEVs表现出良好的骨/破骨细胞前体靶向性,对VPA诱导的骨质流失具有保护性治疗作用,但对卵巢切除术(OVX)和糖皮质激素诱导的骨质疏松模型没有作用,这加深了对VPA诱导的骨质流失的潜在机制和治疗策略的理解。
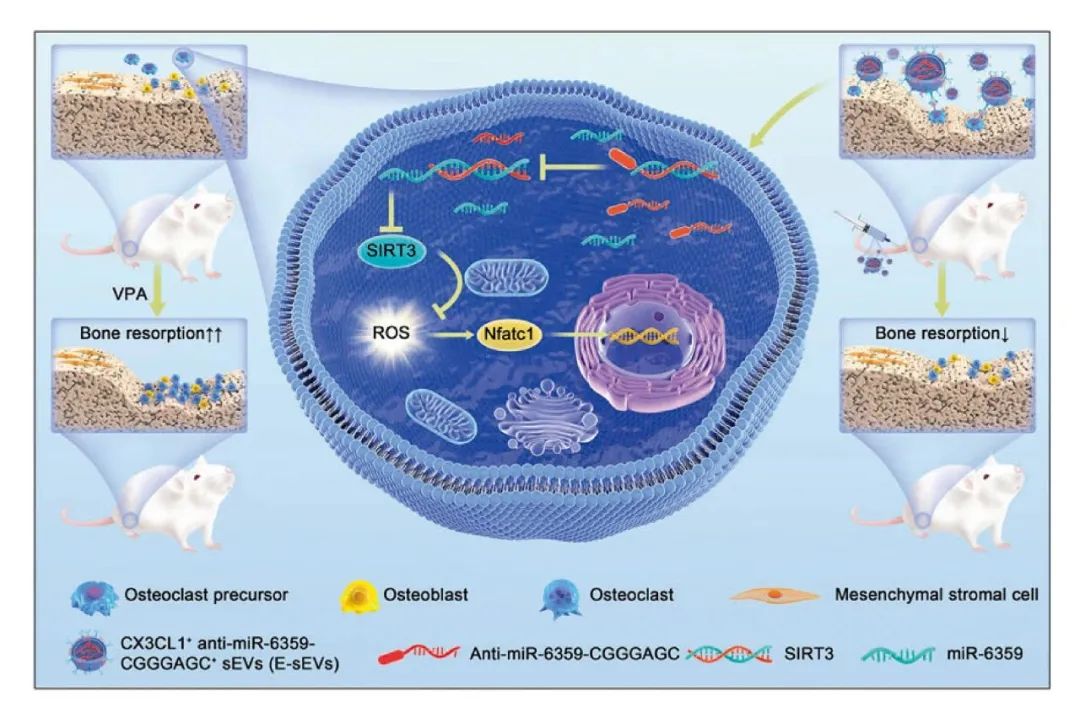
Fig1. VPA诱导骨质流失的机制以及E-sEVs如何预防骨质流失的模型示意图
原文链接:
https://www.nature.com/articles/s41392-023-01726-8#Abs1
02
Mesenchymal Stem Cell Derived Exosomes Repair Uterine Injury by Targeting Transforming Growth Factor-β Signaling
间充质干细胞来源的外泌体通过miR-125b-5p、miR-30c-5p和miR-23a-3p调节TGF-β/smad通路来修复子宫损伤
发表期刊:ACS Nano
影响因子:17.1
发表时间:2024年1月19日
宫腔粘连(IUA)是指子宫腔和宫颈内因子宫手术损伤而引起的粘连。它们是女性不孕症的重要原因。来源于间充质干细胞(MSC)的外泌体在IUA的治疗中起着积极作用。然而,它们减少受损子宫内膜纤维化的机制尚不清楚。本研究证明了来自胎盘间充质干细胞(PMSCs)的外泌体可以恢复受伤动物的子宫功能并提高其生育率。这是通过促进细胞增殖、增加子宫内膜厚度和逆转纤维化来实现的。关于这些治疗效果背后的分子机制,本研究确定了三种特异性miRNAs,即富集于PMSC-外泌体的miR-125b-5p、miR-30c-5p和miR-23a-3p,它们是治疗IUA的关键参与者。具体而言,miR-125b-5p/miR-30c-5p和miR-23a-3p通过靶向smad2和smad3的 3'-非翻译区来抑制其表达,导致转化生长因子-β(TGF-β)/smad信号通路的下调和纤维化的逆转。值得注意的是,PMSC-外泌体在宫内治疗中的安全性也得到了证实。总之,本研究表明,源自PMSCs的外泌体通过miR-125b-5p、miR-30c-5p和miR-23a-3p调节TGF-β/smad通路,具有修复受伤动物子宫内膜损伤和提高生育能力的能力。这为通过基于外泌体的无细胞疗法用于精准治疗IUA提供了见解。

Fig2. 研究模型示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38241636/
03
CMC: Cancer miRNA Census - a list of cancer-related miRNA genes
CMC:癌症miRNA普查 - 癌症相关miRNA基因列表
发表期刊:Nucleic Acids Res
影响因子:14.9
发表时间:2024年1月23日
越来越多的证据表明miRNAs在癌症中起着重要作用;然而,目前尚无明确、易于使用的癌症相关miRNAs或miRNA基因列表,可作为癌症中miRNAs分析的参考。为此,本研究创建了一个包含165个癌症相关miRNA基因的列表,称为癌症miRNA普查(CMC)。该列表基于一个分数,建立在特定miRNAs在癌症中的作用的各种类型的功能和遗传证据的基础上,例如数据库中报道的miRNA-癌症关联,miRNAs与癌症标志的关联,或癌症中遗传改变的正向选择信号。MIR21、MIR155、MIR15A、MIR17或MIRLET7s等众所周知的癌症相关miRNA基因在CMC排名中名列前茅,直接证实了该榜单的准确性和稳健性。此外,为了验证和表明CMC的可靠性,本研究对用于构建CMC的标准进行了验证,将CMC与各种癌症数据(出版物和数据库)进行了比较,并对生物途径和过程(如Gene Ontology或DisGeNET)进行了富集分析。所有验证步骤都显示CMC与癌症/癌症相关过程有很强的关联,证实了其作为癌症相关miRNA基因参考列表的有效性。

Fig3. CMC模型示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38261968/
04
miR-137 regulates PTP61F, affecting insulin signaling, metabolic homeostasis, and starvation resistance in Drosophila
miR-137调节PTP61F,影响果蝇的胰岛素信号、代谢稳态和饥饿抵抗
发表期刊:PNAS
影响因子:11.1
发表时间:2024年1月22日
miR-137是一种高度保守的脑富集microRNA(miRNA),与神经元功能和增殖有关。本研究表明果蝇miR-137无效突变体表现出体重增加、甘油三酯含量增加和运动活性降低。此外,当受到营养剥夺的挑战时,miR-137突变体表现出进食动机降低和存活时间延长。通过遗传上位和挽救实验表明,这种饥饿抵抗是由于胰岛素信号的破坏。进一步研究表明,miR-137无效突变体表现出磷酸化/活化胰岛素受体InR(InR-P)水平的急剧降低。本研究探索了这是否与miR-137预测的靶标蛋白酪氨酸磷酸酶61F(PTP61F)有关,PTP61F是哺乳动物TC-PTP/PTP1B的直系同源物,已知其能使InR-P去磷酸化。事实上,内源性标记的GFP-PTP61F在miR-137无效突变体中的水平显著升高,并且研究人员发现仅PTP61F的过表达就足以模拟miR-137突变体的许多代谢表型。最后,研究人员在miR-137无效突变体背景下敲低了PTP61F的升高水平,并表明这可以挽救InR-P的水平,恢复了正常的体重和甘油三酯含量、饥饿敏感性,并减弱了运动和饥饿诱导的喂养缺陷。本研究支持miR-137对抑制PTP61F水平至关重要的模型,从而维持正常的胰岛素信号传导和能量稳态。

Fig4. miR-137的缺失导致对饥饿的抵抗增加
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38252824/
05
miR-277 targets the proapoptotic gene-hid to ameliorate Aβ42-mediated neurodegeneration in Alzheimer's model
miR-277靶向促凋亡基因hid以改善阿尔茨海默氏症模型中Aβ42介导的神经变性
发表期刊:Cell Death Dis
影响因子:9.0
发表时间:2024年1月18日
阿尔茨海默病(AD)是一种与年龄相关的进行性神经退行性疾病,表现为认知功能下降,迄今为止尚无治愈方法。AD的原因之一是淀粉样蛋白-β42(Aβ42)斑块的积累,这些斑块触发异常的基因表达和信号传导,从而导致神经元细胞死亡,机制未知。人Aβ42在果蝇发育视网膜中的错误表达表现出AD样神经病理学。小非编码RNAs,即microRNAs(miRNAs)通过转录后调节其靶基因的表达,从而调节不同的信号通路。在正向遗传筛选中,本研究发现miR-277(人类直系同源物是has-miR-3660)是Aβ42介导的神经退行性变的遗传修饰因子。miR-277的功能缺失增强了Aβ42介导的神经退行性变。而在GMR>Aβ4背景下,miR-277的功能获得下调细胞死亡以维持神经元数量,从而恢复视网膜轴突靶向缺陷,表明功能被挽救了。此外,miR-277的功能获得挽救了在GMR > Aβ42背景下观察到的闭合和攀爬测定缺陷。因此,miR-277的功能获得在结构和功能上都挽救了Aβ42介导的神经退行性变。此外,本研究将一种进化上保守的促凋亡基因hid(head involution defective)确定为miR-277的靶标之一,并使用荧光素酶和qPCR测定法验证了这些结果。在GMR > Aβ42背景下,与单独GMR>Aβ42背景相比,miR-277的功能获得导致hid转录水平降低到其水平的三分之一。本研究提供了一种新的分子机制,其中miR-277靶向并下调促凋亡基因hid转录水平,以通过阻断细胞死亡来挽救Aβ42介导的神经变性。这些研究揭示了在人类神经退行性疾病中观察到的Aβ42积累后介导细胞死亡反应的分子机制,并为神经退行性疾病提供了新的治疗靶点。

Fig5. miR-277改善GMR > Aβ42蝇眼的神经退行性表型
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38238337/










