推荐产品
公司新闻/正文
JECCR(IF11+)丨TAMs源性外泌体LINC01592诱导食管癌免疫逃逸
人阅读 发布时间:2023-11-21 13:35
TAMs(肿瘤相关巨噬细胞)浸润促进食管癌(EC)的进展。然而,其潜在机制仍不清楚。近日,Journal of Experimental & Clinical Cancer Research期刊(IF11.3)在线发表了一篇题为Tumor-associated macrophage-derived exosomes LINC01592 induce the immune escape of esophageal cancer by decreasing MHC-I surface expression的研究论文。该研究发现TAMs和EC之间通过LINC01592/E2F6/NBR1/MHC-I轴存在显著的分子相互作用,从而促进恶性肿瘤的进展。这表明,针对该轴的治疗干预可能为该疾病的治疗带来希望。

首先,研究人员使用THP1细胞极化成M2-TAMs,以模拟TAMs。结果发现,与M0-Exos相比,M2-Exos显著抑制了T细胞介导的肿瘤细胞杀伤。然后将CD8+ T细胞与M2-Exos-EC细胞进行体外共培养,并检测CD8+ T细胞的生长以及IFN-γ、TNF-α和Gzmb的表达。结果显示,CD8+ T细胞表现出较低的TNF-α、IFN-γ和Gzmb表达水平和生长。此外,在皮下异种移植模型中,接受M2-Exos注射的小鼠肿瘤体积比接受M0-Exo注射的小鼠肿瘤体积有统计学意义的增加,并且M2-Exos显著降低了移植动物癌症样本中CD8+蛋白的表达。以上结果表明,从M2-TAM中分离得到的外泌体明显抑制了EC细胞中CD8+ CTL细胞介导的抗肿瘤免疫。

Fig1. M2-TAMs源性外泌体促进食管癌免疫逃逸
接下来,为了检测TAMs中与外泌体相关的lncRNAs,研究人员对M0-Exos和M2-Exos进行了lncRNA分析。结果发现LINC01592是一个突出的非编码RNA。随后,研究人员检测了细胞外的LINC01592。结果发现,单独添加RNase A的M2-TAM在条件培养基(CM)中未显示LINC01592水平的变化。然而,在Triton X-100和RNase A处理后,CM 中的LINC01592水平下降。此外,外泌体中的LINC01592水平与CM中的相同。表明外泌体是细胞外LINC01592的主要转运体。FISH和亚细胞分离显示,LINC01592位于细胞核和细胞质中,主要位于EC细胞的细胞核中。之后,研究人员将phalloidin标记的Eca-109细胞与PKH26标记的外泌体孵育。结果发现,经孵育的Eca-109细胞表现出phalloidin脂质染料和PKH26荧光的共定位,从而证明了外泌体的有效吸收。以上结果表明,M2分泌的LINC01592通过外泌体转运到EC细胞。

Fig2. M2-TAMs分泌的LINC01592被转移到食管癌细胞
随后,研究人员通过TCGA数据库分析发现,LINC01592在EC中大量表达,其表达水平与预后呈负相关。此外,研究发现引入外泌体抑制剂Annexin V或下调LINC01592可逆转M2-Exos显著抑制T细胞介导的肿瘤细胞杀伤。在涉及CD8+ T细胞与M2-Exos-EC细胞的体外共培养实验中。研究人员发现,引入外泌体抑制剂Annexin V或下调LINC01592逆转了CD8+ T细胞生长减缓,以及IFN-γ、TNF-α和Gzmb表达的降低。进一步的异种移植实验发现,与单独给药M2/sh-NC-Exos或M2-Exos的小鼠相比,给药M2/sh-1592#2-Exos或M2-Exos + Annexin V的小鼠表现出肿瘤体积的明显减少和CD8+蛋白水平的显著升高。以上结果表明,M2-Exos源性LINC01592负责诱导肿瘤的免疫逃避。

Fig3. M2-TAM源性外泌体LINC01592诱导肿瘤免疫逃逸
接着,研究人员探索了M2-TAMs源性外泌体LINC01592诱导肿瘤免疫逃逸的分子机制。结果发现,M2-TAMs分泌富含LINC01592的外泌体进入肿瘤细胞后,LINC01592直接结合E2F6,从而促进E2F6进入细胞核;LINC01592和E2F6的协同作用促进NBR1的转录水平。NBR1通过泛素结构域与泛素化蛋白MHC-I结合的增加介导了自噬溶酶体中MHC-I降解的增加和肿瘤细胞表面MHC-I表达的降低,进而导致肿瘤细胞逃避CD8+ CTL的免疫攻击。
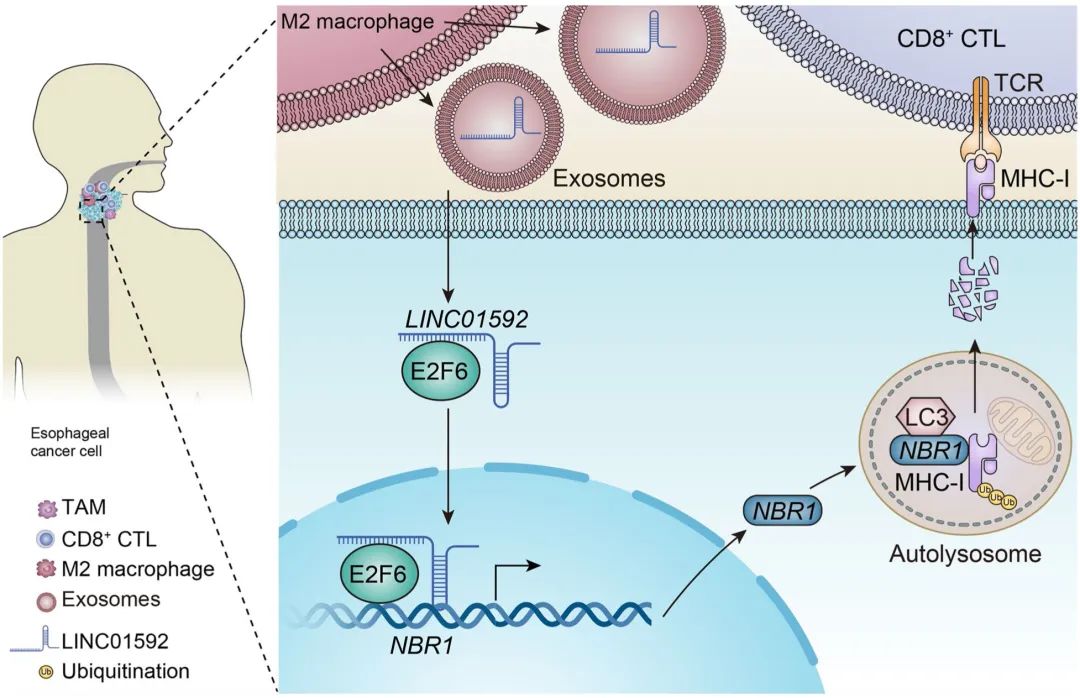
Fig4. 作用机制示意图
最后,研究人员比较了不同分级EC和正常食管上皮(NEE)组织中LINC01592/E2F6/NBR1/MHC-I的表达水平。结果发现,LINC01592/E2F6/NBR1在癌组织中表达水平较高,尤其是在III + IV级。另一方面,MHC-I的表达表现出相反的模式。此外,LINC01592/E2F6/NBR1信号轴的表达水平之间存在正相关。而MHC-I的表达与LINC01592/E2F6/NBR1成反比。IF、FISH和IHC结果显示,LINC01592水平与E2F6/NBR1信号呈正相关。而MHC-I的表达与LINC01592/E2F6/NBR1成反比。表明LINC01592表达与临床EC恶性分级成正相关,同时也揭示了LINC01592表达与患者预后成负相关。

Fig5. LINC01592/E2F6/NBR1/MHC-I轴与临床进展的相关性
总之,本研究结果证明了M2-TAM源性外泌体LINC01592通过激活E2F6/NBR1/MHC-I信号通路增强了肿瘤对免疫系统的逃避。LINC01592的肿瘤促进作用通过破坏E2F6/NBR1/MHC-I信号轴而显著降低。有趣的是,抑制LINC01592导致肿瘤细胞表面MHC-I表达增强,从而增强CD8 + T细胞回输的功效。
原文链接:
https://jeccr.biomedcentral.com/articles/10.1186/s13046-023-02871-2#Abs1
本研究使用到的lncRNA FISH探针产品由锐博生物提供!更多关于lncRNA研究的产品或服务,欢迎登陆锐博生物官方网站(www.ribobio.com)进行查询!










