广州市锐博生物科技有限公司品牌商
18 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
推荐产品
公司新闻/正文
Nature子刊丨CSTF2介导的mRNA m6A修饰驱动胰腺导管腺癌m6A亚型
886 人阅读发布时间:2023-10-19 10:11
基因转录本的N6-甲基腺苷(m6A)修饰在癌症中起关键作用。近日,Nature Communications(IF16.6)期刊在线发表了一篇题为CSTF2 mediated mRNA N6-methyladenosine modification drives pancreatic ductal adenocarcinoma m6A subtypes的研究论文。该研究报道了CSTF2促进mRNAs中的m6A修饰,IGF2BP2可增强具有高甲基化m6As的mRNA的稳定性,形成CSTF2-m6A-IGF2BP2轴。该m6A修饰相关轴的异常可能有助于PDAC的发展和进展,因此在PDAC精准医学中具有潜在的临床应用价值。

首先,研究人员对来自65例PDAC患者的98个胰腺样本(其中包括33对PDAC和相应的正常组织以及另外32个PDAC样本)进行了m6A测序(m6A-seq)。结果鉴定了17,996个m6A峰,其中195个高甲基化,93个低甲基化。鉴定出的m6A位点富集于经典GGACH motif和起始密码子和终止密码子附近的区域。288个失调的m6A位点在与癌症通路相关的基因(如细胞周期和上皮-间充质转化)中富集。先前报道的癌基因如CENPF、WNT7B和NTSR被发现在肿瘤中具有hyper-m6A甲基化。
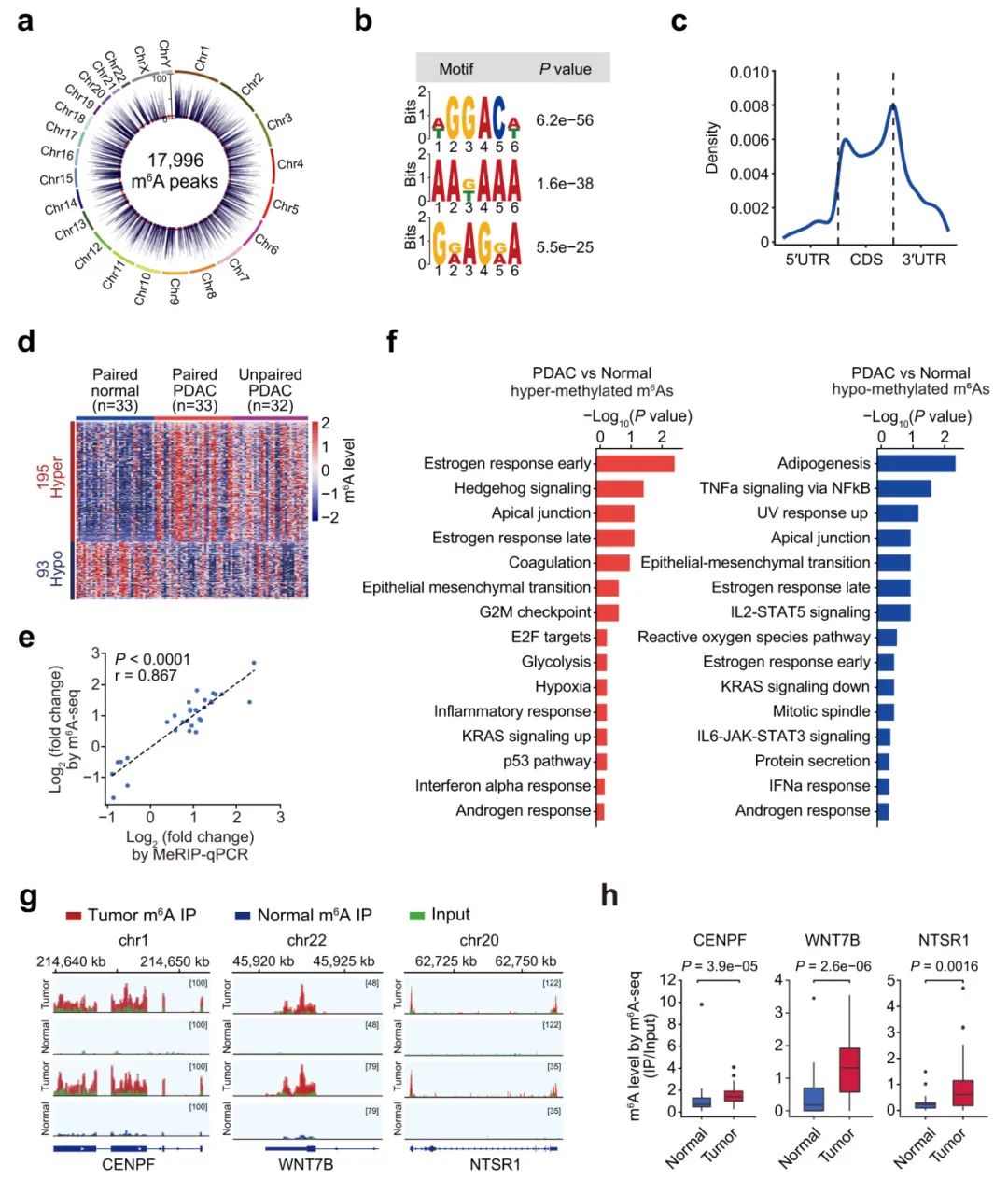
Fig1. PDAC中m6A修饰的全转录组图谱
接着,研究人员根据这些差异m6A峰对PDAC患者进行无监督共识聚类分析,进一步表征了两种PDAC亚型(分别指定为S1和S2),S2 PDAC表现出与S1 PDAC不同的m6A模式,但它们在正常组织中无差异,表明亚型模式是肿瘤特异性的。此外,S1和S2 PDAC样品之间的差异甲基化m6As在S1 PDAC样本和邻近正常组织样本之间没有差异,并且与邻近正常组织和肿瘤组织之间的差异甲基化m6As有很大的重叠,表明S2 PDAC特异性m6A异常调节。随后,研究人员分析了这两种亚型与已知临床因素(如性别、年龄、吸烟状况、饮酒状况、肿瘤分期、分化、血管侵袭和淋巴结转移)的相关性。结果发现,除神经侵袭外均为负相关。进一步研究发现S2 PDAC中Bailey’s 鳞状亚型和Collisson’s典型亚型的频率明显高于S1 PDAC。生存分析显示,S2 PDAC的中位无进展生存期(PFS)时间和总生存期(OS)时间明显短于S1 PDAC。以上结果表明,通过不同的m6A修饰可区分两种PDAC亚型。
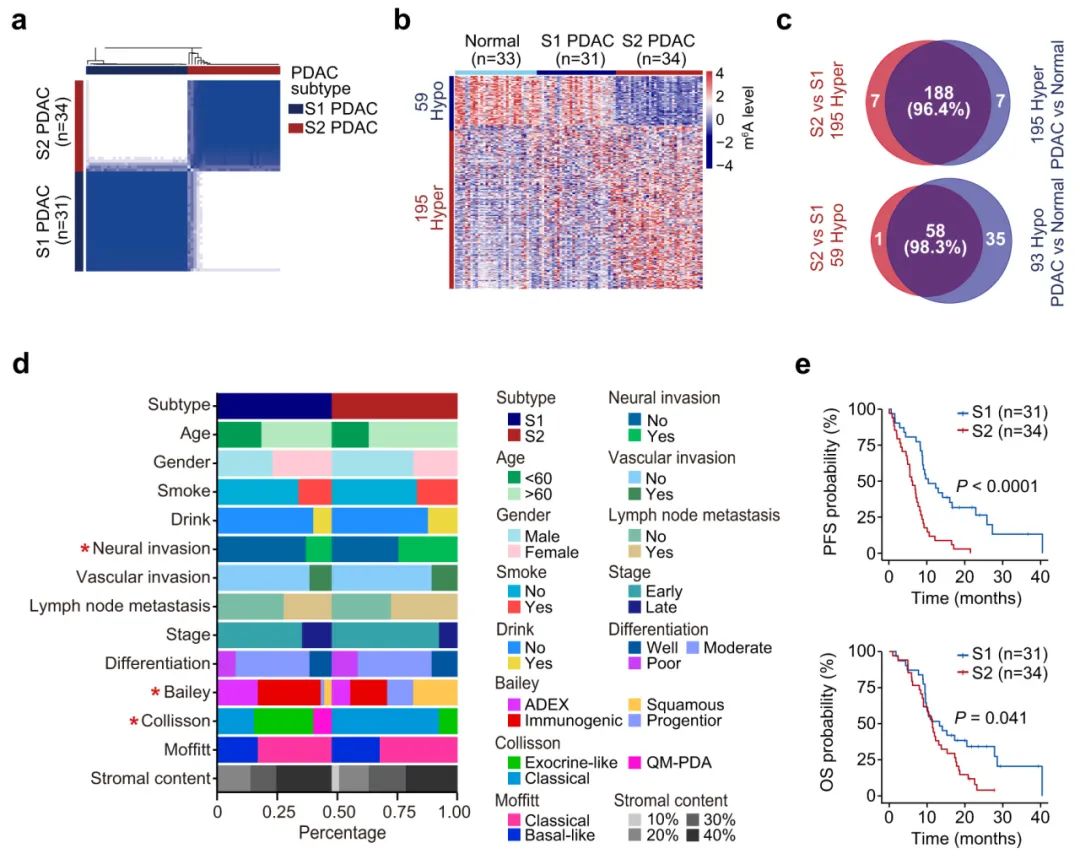
Fig2. 通过转录组范围的m6A修饰对PDAC进行亚型分型
接下来,研究人员探讨了PDAC亚型形成的机制。首先,研究人员检查了S2 PDAC中高甲基化m6A与RNA结合蛋白(RBPs)的相关性。结果发现,CSTF2(剪切刺激因子2)RNA水平与S2 PDAC中高甲基化m6A位点的水平最显著相关,且S2 PDAC中的CSTF2 RNA和蛋白水平高于S1 PDAC。此外,当在PDAC细胞系中(PANC-1和SW1990)敲低CSTF2,分别有86%和88%的差异m6A位点的甲基化水平显著降低;当在相同细胞系中异位过表达CSTF2时,8804和8554个m6A位点被高甲基化,与CSTF2敲低细胞中低甲基化的m6A有72.8%和61.7%重叠。此外,S2 PDAC中64.9%的高甲基化在CSTF2敲低细胞中是低甲基化的。总之,这些结果表明CSTF2可能调节PDAC中mRNA m6A的形成。
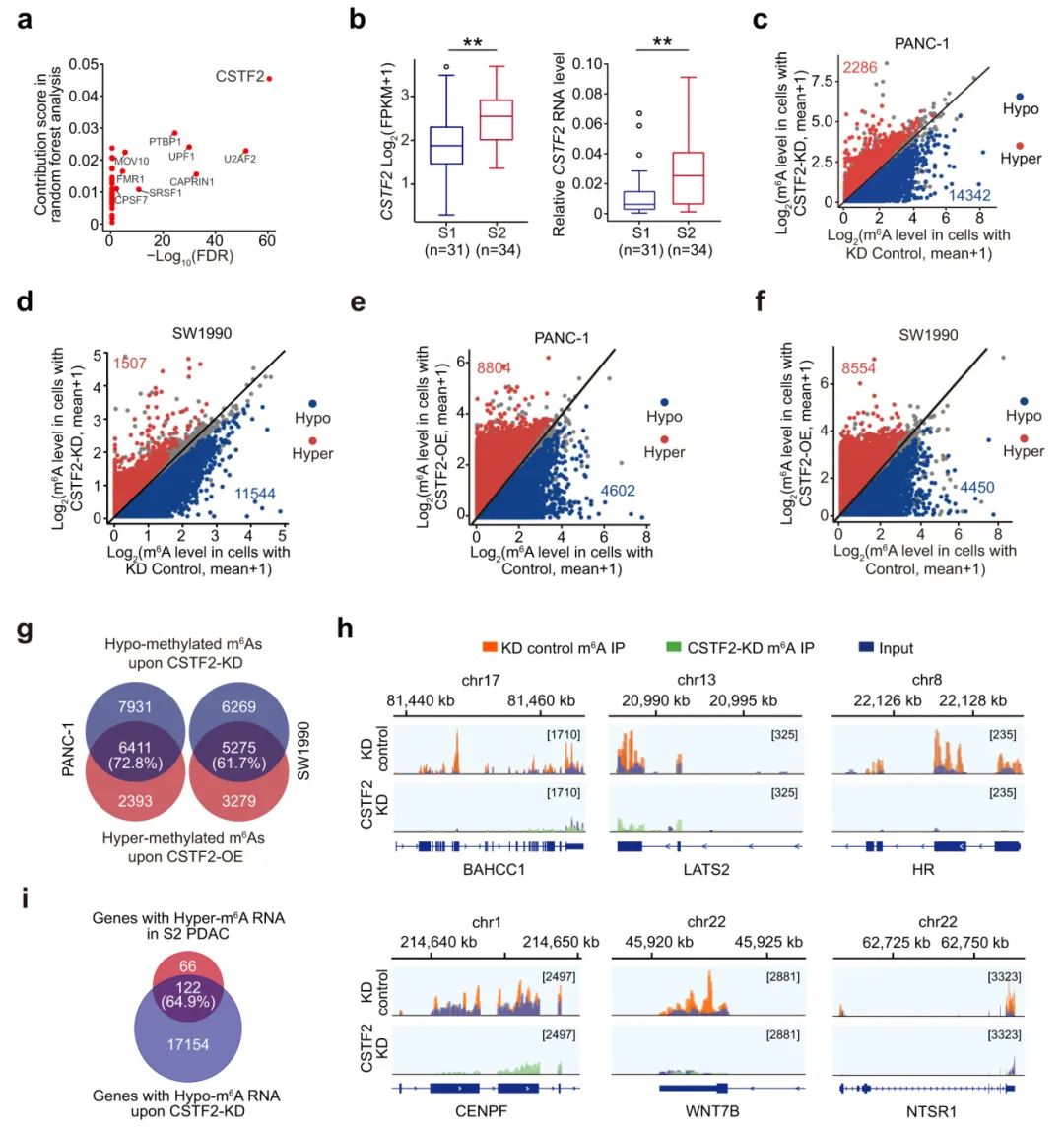
Fig3. CSTF2是S2 PDAC亚型中促进mRNA m6A沉积的关键蛋白
然后,研究人员探讨了CSTF2对PDAC细胞恶性表型的影响。体外实验表明,敲低CSTF2可显著抑制PDAC细胞的增殖、集落形成、细胞周期、迁移和侵袭能力。体内实验显示,CSTF2过表达/沉默显著增强/抑制PDAC肿瘤的生长速度。此外,强制表达CSTF2可促进PDAC细胞的肺转移,而敲低CSTF2则相反。
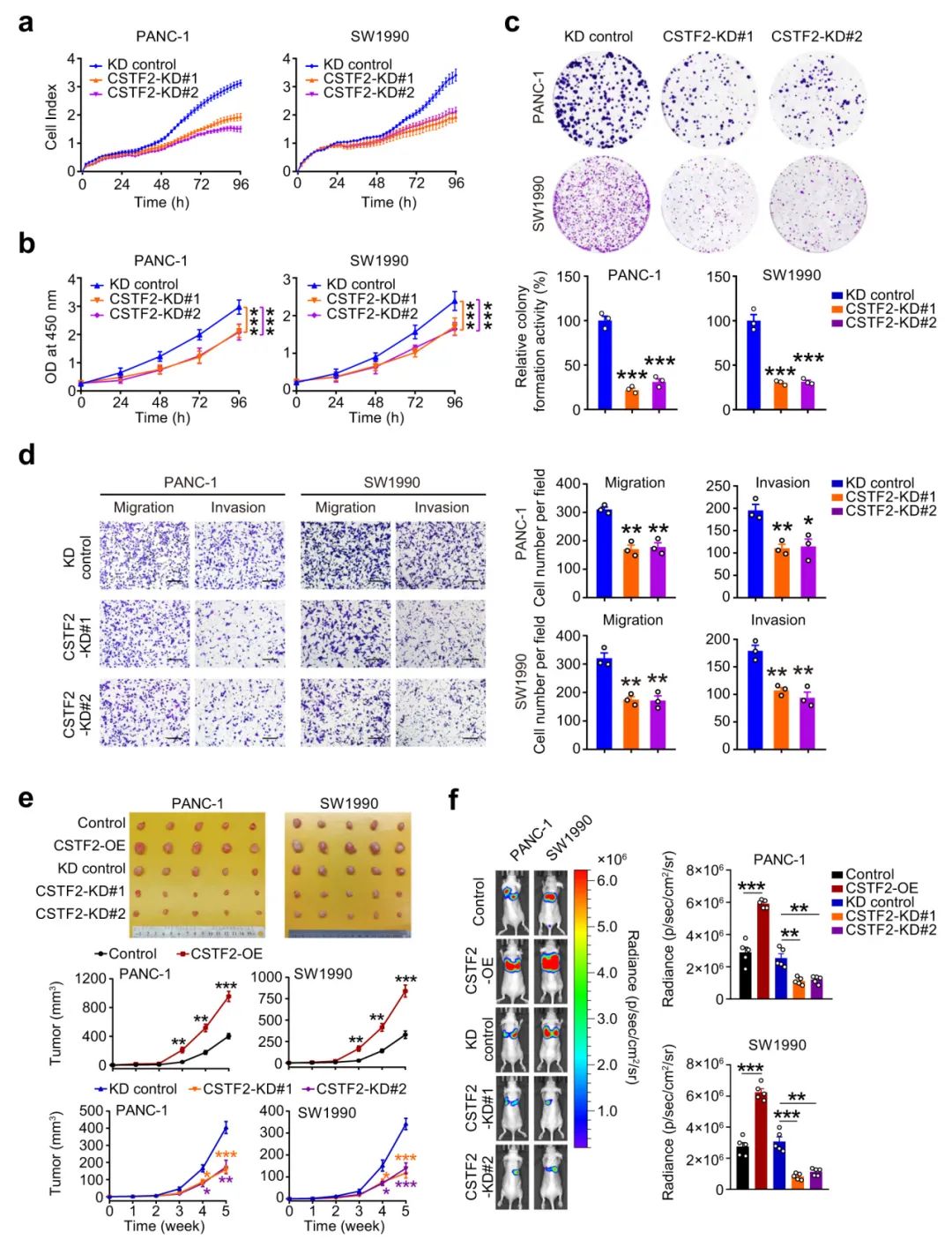
Fig4. 敲低CSTF2可抑制PDAC细胞的增殖和转移
为了探索CSTF2如何介导m6A沉积,研究人员通过分析CLIP测序数据发现,CSTF2 RNA结合位点与RNA中的m6A位点很好地重叠。之前的研究表明CSTF2可能通过MTC和RNA Pol II影响m6A的沉积。因此,研究人员对CSTF2和RNA Pol II进行了CUT&Tag测序,结果显示CSTF2和RNA Pol II的基因组结合位置有很好的重叠。具有Pol II占用的m6A峰在CSTF2敲低时m6A水平的降低明显大于没有Pol II占用的峰。此外,在Pol II占用上表现出实质性变化的基因在CSTF2敲低时也显示出m6A水平的更大降低。另外,研究发现,DNA中的CSTF2结合位点与RNA中的CSTF2结合位点和m6A位点共定位,并且共定位与RNA Pol II相关。以上结果表明,RNA Pol II确实可能在介导CSTF2调控的m6A沉积中发挥作用。

Fig5. RNA Pol II可能在介导CSTF2调控的m6A沉积中发挥作用
先前的研究报道了CSTF2可能在RNA Pol II的延伸中起到限速因子的作用,最近的一项研究表明,延长延伸速率可能有助于RNA Pol II募集m6A writer METTL3。在CSTF2敲低后,研究人员进一步对Pol II和Pol II- ser2p进行了CUT&Tag测序。结果发现,在CSTF2敲低后,低甲基化m6A基因的RNA Pol II和Pol II-Ser2P密度显著降低,而CSTF2非靶基因的RNA Pol II密度不受影响。CSTF2靶基因(如CENPF、WNT7B和NTSR1基因)的代表性基因组轨迹说明了这一点。此外,CSTF2敲低促进了PDAC细胞中新生RNA的合成,而异位过表达CSTF2减弱了新生RNA的合成,证实了CSTF2的作用降低了Pol II的延伸率。进一步的研究发现,PDAC细胞中强制CSTF2表达变化可导致RNA Pol II和METTL3相互作用的实质性变化。
值得注意的是,敲低CSTF2引起的整体m6A水平下降与METTL3敲低引起的m6A水平下降相当,并且METTL3敲低细胞中低甲基化的m6A与CSTF2产生的69%的m6A重叠。CSTF2敲低导致靶转录本m6A区域周围的METTL3结合减少,但CSTF2异位过表达增强了这种相互作用。这些结果有力地支持了CSTF2通过减缓Pol II的延伸来促进m6A沉积,从而促进METTL3的共转录募集。
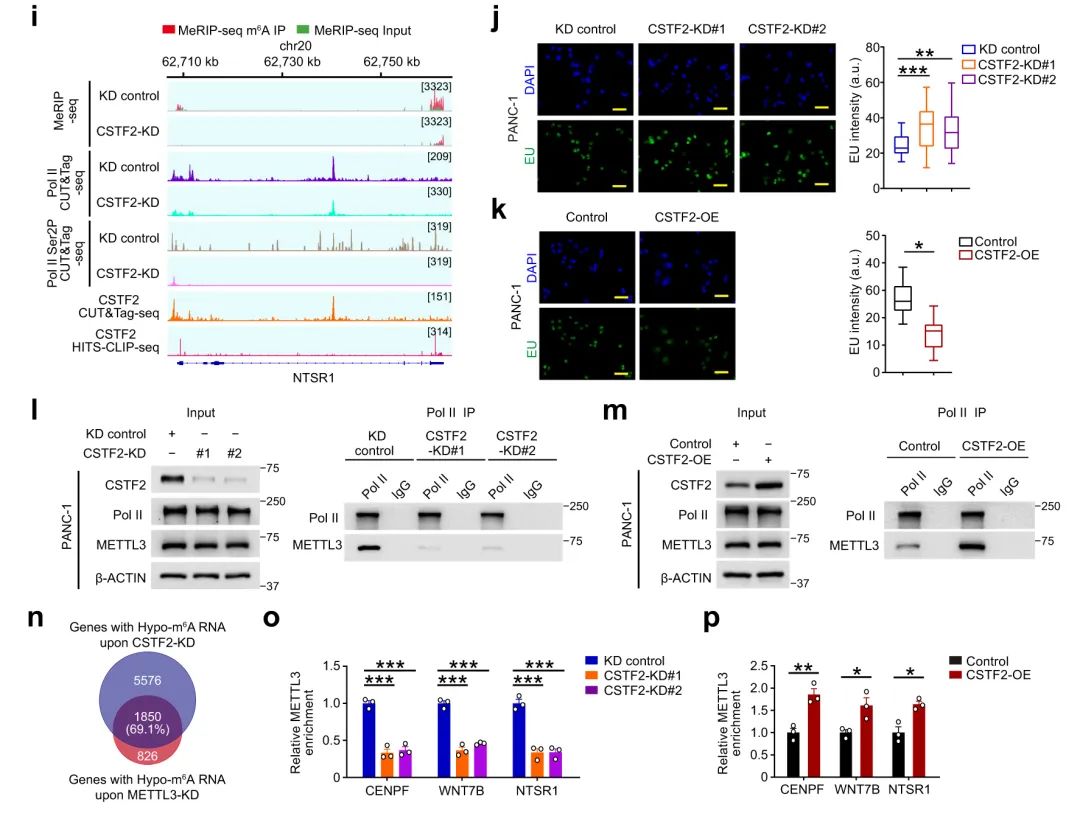
Fig6. CSTF2通过延缓延伸介导m6A沉积
最后,研究人员探讨了m6A对PDAC中宿主RNA水平的影响,结果发现S1和S2 PDAC亚型之间的254个差异甲基化m6As中,有205个m6As(148个RNAs)对其宿主RNA水平有影响。在148个RNAs中,115个RNAs在S2 PDAC中的m6A水平和RNA水平均上调,而33个RNAs的m6A水平和RNA水平均下调。在PDAC细胞中也观察到m6A水平与RNA水平之间的正相关,其中许多RNAs的RNA水平下调在CSTF2敲低时将表现出m6A水平的低甲基化,但只有少数RNAs将显示延长的3'UTR,表明CSTF2调节的m6A可能有助于RNA水平的升高。
此外,研究人员进行了基于dCas13的m6A编辑和gRNA来特异性操纵m6A位点。证实了m6A水平的下调抑制了IGF2BP2的结合,导致mRNA水平和转录本半衰期的下调。强制表达IGF2BP2未能挽救m6A水平下调对转录本mRNA水平和半衰期的影响。综上所述,CSTF2调控的m6A通过IGF2BP2增强了RNA的稳定性。
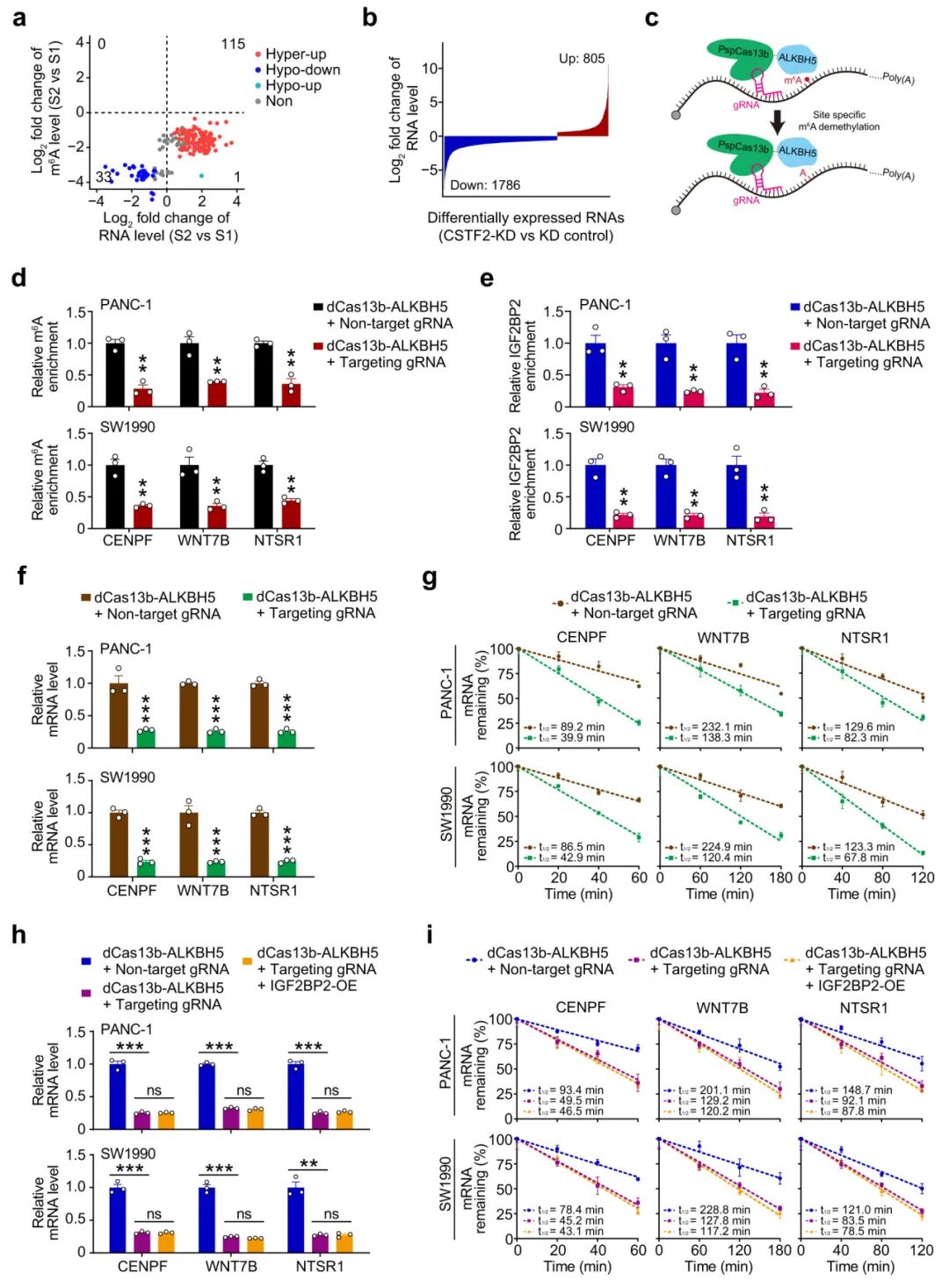
Fig7. 异常的m6A增强mRNA的稳定性
总之,本研究全面破译了PDAC中转录组范围内m6A mRNA修饰的景观。鉴定了CSTF2作为m6A沉积的介质,并驱动两种PDAC亚型的形成。此外,CSTF2调控的m6A甲基化程序主要可以通过m6A稳定的reader IGF2BP2识别,从而促进致癌途径,这表明CSTF2相关的PDAC m6A亚型可以作为一种有前途的治疗策略。
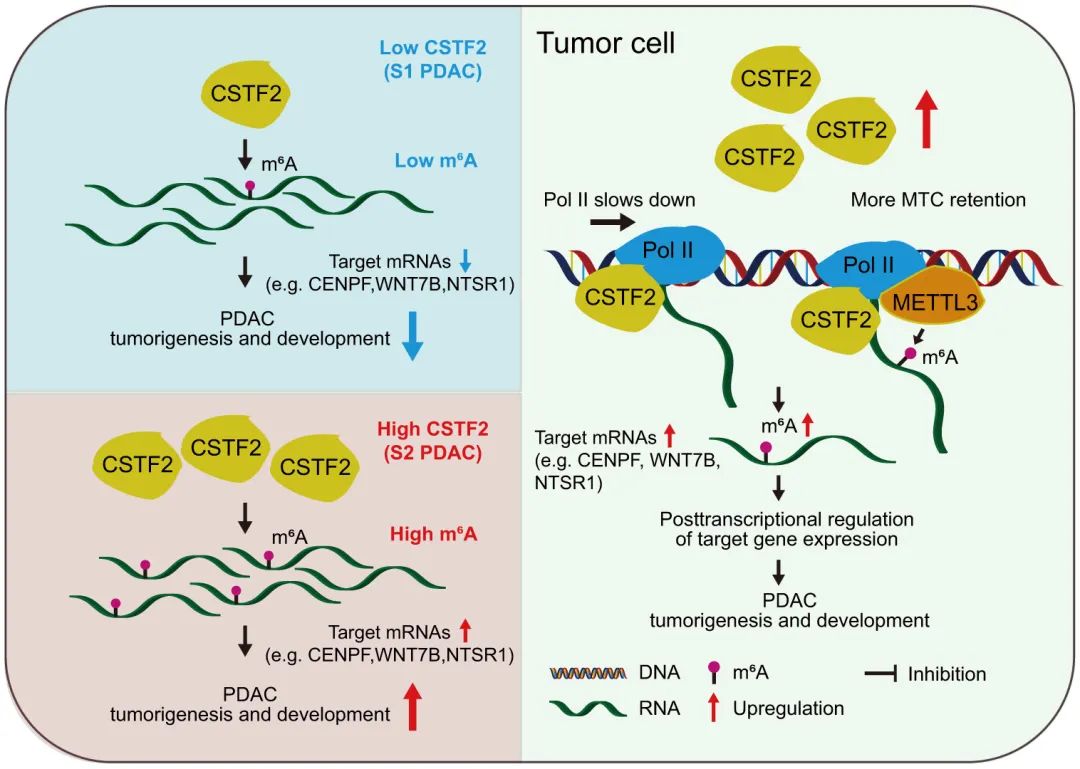
Fig8. CSTF2在RNA m6A沉积和PDAC亚型形成中的作用模型
原文链接:
https://www.nature.com/articles/s41467-023-41861-y
本研究使用到的EU RNA转录活性检测试剂盒由锐博生物提供!更多关于m6A研究的产品或服务,欢迎登陆锐博生物官方网站(www.ribobio.com)进行查询!