推荐产品
公司新闻/正文
lncRNA研究进展盘点丨20230901期
人阅读 发布时间:2023-09-06 11:16
01
肠道微生物群通过长链非编码RNA Snhg9重编程肠道脂质代谢
发表期刊:Science
影响因子:56.9
发表时间:2023年8月25日
肠道微生物群调节哺乳动物脂质的吸收、代谢和储存。本研究报道了微生物群通过抑制小肠上皮细胞中长链非编码RNA(lncRNA)Snhg9(小核仁RNA宿主基因9)的表达来重编程小鼠的肠道脂质代谢。Snhg9通过将PPARγ抑制剂sirtuin 1与CCAR2(细胞周期和凋亡蛋白2)解离,抑制脂质代谢中枢调节因子PPARγ(过氧化物酶体增殖物激活受体γ)的活性。Snhg9在常规小鼠肠上皮中的强制表达损害了脂质吸收,减少体脂,并防止饮食诱导的肥胖。微生物群通过包含骨髓细胞和第3组先天淋巴样细胞的免疫中继来抑制Snhg9表达。因此,本研究结果确定了lncRNA在微生物控制宿主代谢中意料之外的作用。
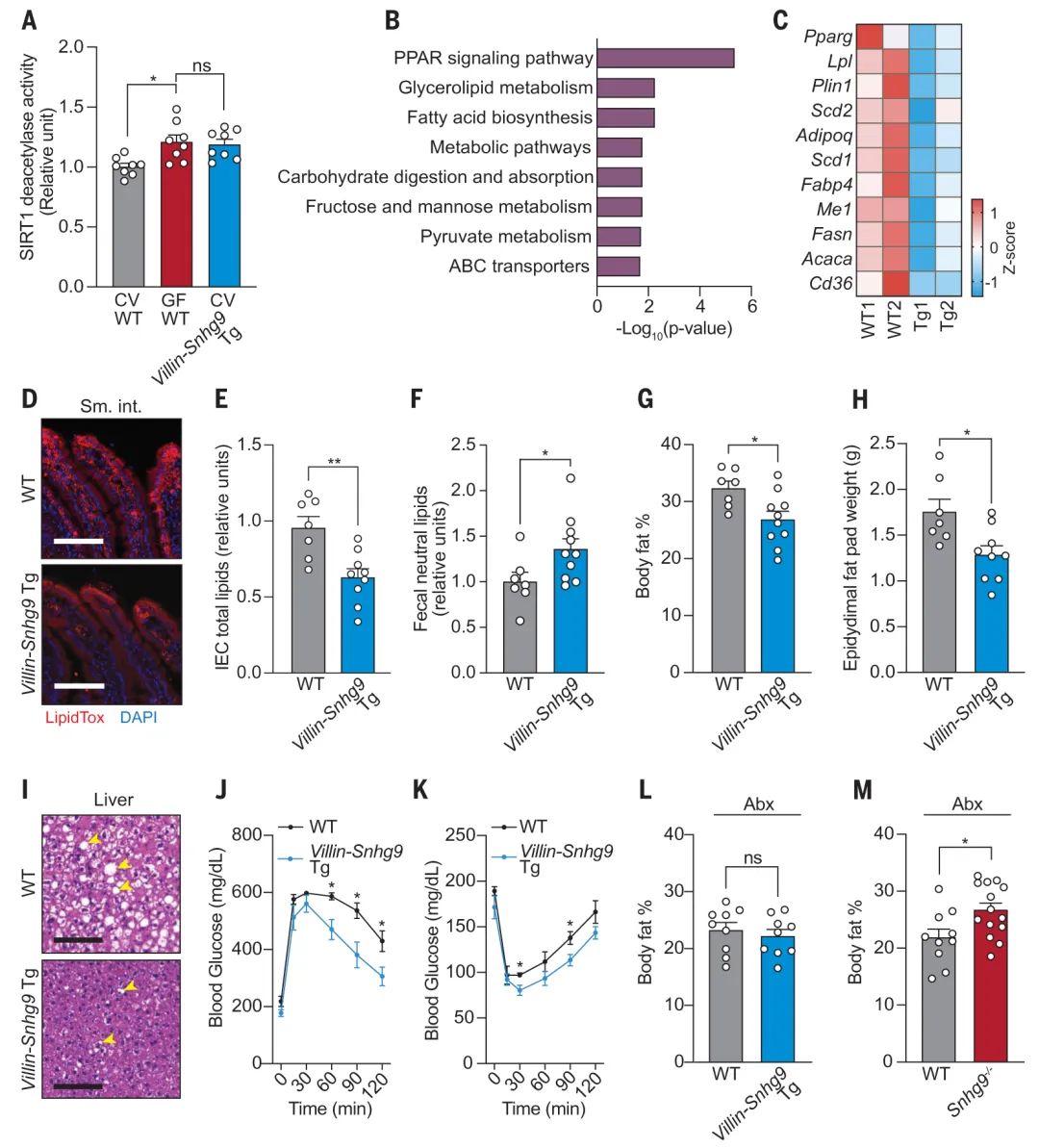
Fig1. Villin-Snhg9转基因小鼠可降低脂质吸收,并保护其免受高脂肪饮食诱导的代谢紊乱
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37616368/
02
DNA损伤诱导的CTBP1-DT lncRNA编码的DDUP蛋白赋予卵巢癌顺铂耐药性
发表期刊:Cell Death Dis
影响因子:9.0
发表时间:2023年8月26日
DNA损伤反应(DDR)信号的持续激活已被证明在癌症化疗失败中起着至关重要的作用。然而,在癌细胞中维持DDR的机制尚不清楚。本研究发现CTBP1-DT lncRNA编码的DDUP微蛋白的表达在顺铂耐药卵巢癌细胞中急剧增加,并且与基于顺铂的治疗反应呈负相关。使用患者来源的人类癌细胞模型,本研究观察到DNA损伤诱导的DDUP病灶在DNA损伤部位维持RAD18/RAD51C和RAD18/PCNA复合物,从而通过双重RAD51C介导的同源重组(HR)和增殖细胞核抗原(PCNA)介导的复制后修复(PRR)机制导致顺铂耐药。值得注意的是,使用ATR抑制剂治疗破坏了DDUP/RAD18的相互作用,并消除了DDUP对延长DNA损伤信号的影响,这导致卵巢癌细胞对体内基于顺铂治疗的超敏反应。总之,本研究提供了对顺铂耐药中DDUP介导的异常DDR信号的见解,并描述了一种用于铂类耐药卵巢癌的潜在新治疗方法。

Fig2. CTBP1-DT lncRNA编码的DDUP赋予卵巢癌顺铂耐药的机制示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37633920/
03
超级增强子驱动的lncRNA LINC00880充当CDK1和PRDX1之间的支架以维持肺腺癌的恶性
发表期刊:Cell Death Dis
影响因子:9.0
发表时间:2023年8月24日
超级增强子(SEs)是与细胞身份和疾病相关的调控元件簇。然而,关于SE相关的长链非编码RNAs(lncRNAs)在肺腺癌(LUAD)中的作用的研究仍然很少。本研究鉴定出了一个SE驱动的lncRNA LINC00880,与正常组织相比,其在LUAD中的表达更高,并且在I期LUAD中表现出更差的预后。研究发现转录因子(TF)FOXP3可以同时占据LINC00880的启动子和SE区域以促进其转录。LINC00880的致癌功能在体外和体内均得到验证。机制上,LINC00880与蛋白质CDK1结合以增加其激酶活性,这依赖于CDK1中pT161的磷酸化状态。LINC00880还促进了CDK1和PRDX1之间的相互作用。此外,LINC00880与PRDX1相互作用,表明LINC00880作为CDK1和PRDX1之间的蛋白质支架形成三元复合物,从而导致PI3K/AKT的激活,促进恶性肿瘤的发生。本研究结果表明,SE相关的lncRNA LINC00880调节CDK1/PRDX1轴以维持LUAD的恶性,从而提供了一个新的治疗靶点。

Fig3. SE相关的lncRNA LINC00880调节CDK1/PRDX1轴以维持LUAD恶性的作用机制
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37620336/
04
m6A介导的lncRNA BLACAT3上调通过YBX3核穿梭和增强NCF2转录促进膀胱癌血管生成和血行转移
发表期刊:Oncogene
影响因子:8.0
发表时间:2023年8月23日
淋巴转移被认为是膀胱癌(BLCa)转移的主要方式,但血行转移占癌症相关死亡的大多数。在过去的二十年中,长链非编码RNAs(lncRNAs)引起了极大的关注,这是开发转移性癌症靶向药物治疗的新希望;然而,参与BLCa血行转移的lncRNAs的潜在机制仍有待阐明。本研究鉴定了一个lncRNA BLCa相关转录本3(BLACAT3),其在BLCa中异常上调,并与肌层浸润性膀胱癌患者的不良预后相关。方法学上采用m6A表观转录组微阵列、RNA测序和质谱(MS)筛选调控轴的关键分子。通过功能实验、动物模型和临床样品,探索BLACAT3在体外和体内BLCa中的作用。机制上,m6A修饰通过稳定RNA结构促进BLACAT3上调。BLACAT3募集YBX3穿梭到细胞核中,协同增强NCF2转录,并通过激活下游NF-κB信号通路促进BLCa血管生成和血行转移。本研究结果将为BLCa患者开发预后预测工具,并为转移性BLCa发现新型治疗生物学靶点。

Fig4. BLACAT3对体内和体外BLCa血管生成和迁移的影响
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37612524/
05
解码长链非编码RNAs在牙周炎中的作用:一个全面综述
发表期刊:Biomed Pharmacother
影响因子:7.5
发表时间:2023年8月22日
牙周炎是一种炎症性疾病,其特征是牙槽骨和邻近牙周韧带的病理性丧失。它被认为是一种带来巨大健康负担的疾病,发病率为20-50%。牙周炎的病因是多因素的,遗传因素约占重症病例的一半。研究表明,长链非编码RNAs(lncRNAs)在牙周炎发病机制中起着关键作用。越来越多的证据表明,lncRNAs具有独特的调节机制,使其能够控制牙周细胞中的许多重要过程,包括成骨分化、炎症、增殖、细胞凋亡和自噬。本文综述了lncRNAs在牙周炎发病机制中的不同作用,阐明了疾病发展的潜在机制。通过强调lncRNAs作为生物标志物和治疗靶点的潜力,本综述为牙周炎的诊断和治疗提供了新的视角,为进一步研究基于lncRNA的治疗方法铺平了道路。

Fig5. lncRNAs在牙周炎中的作用
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37619483/










