广州市锐博生物科技有限公司品牌商
18 年
手机商铺
- NaN
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
- 3.7
推荐产品
公司新闻/正文
lncRNA研究进展盘点丨20230817期
646 人阅读发布时间:2023-08-21 09:18
01
发表期刊:Signal Transduct Target Ther
影响因子:39.3
发表时间:2023年8月14日
正常高密度脂蛋白(nHDL)可以诱导健康个体的血管生成。然而,冠状动脉疾病患者的HDL经历各种改变,变得功能障碍(dHDL),并失去其促进血管生成的能力。本研究鉴定了一个长链非编码RNA HDRACA,其参与HDL对血管生成的调节。研究表明,nHDL结合的S1P通过与S1P受体1(S1P1)相互作用来激活含有WW结构域的E3泛素蛋白连接酶2(WWP2),从而促进泛素化介导的Kruppel样因子5(KLF5)降解,抑制HDRACA的转录,并下调内皮细胞中HDRACA的表达。相比之下,S1P水平低于nHDL的dHDL在降低HDRACA表达方面效果要差得多。HDRACA能够与Ras相互作用蛋白1(RAIN)结合以阻碍RAIN与vigilin之间的相互作用,导致vigilin蛋白与增殖细胞核抗原(PCNA)mRNA之间的结合增加,最终导致PCNA表达降低,并抑制血管生成。人HDRACA在后肢缺血小鼠模型中的表达抑制了血管生成的恢复。综上所述,这些发现表明HDRACA参与HDL对血管生成的调节,nHDL抑制HDRACA的表达诱导血管生成,而dHDL在抑制HDRACA表达方面的效果要差得多,这就解释了dHDL刺激血管生成能力下降的原因。

Fig1. HDL-HDRACA调控机制示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37574469/
02
发表期刊:Nucleic Acids Res
影响因子:14.9
发表时间:2023年8月10日
包括MALAT1在内的核保留长链非编码RNAs(lncRNAs)已成为转录、可变剪接和染色质组织等许多分子过程的关键调节因子。本研究报道了位于MALAT1的3'区域中存在三个保守且热力学稳定的RNA G-四链体(rG4s)。使用rG4结构域特异性RNA pull-down,然后进行质谱和RNA免疫沉淀,本研究证明了MALAT1 rG4结构与两种核仁蛋白,核仁素(NCL)和核仁磷酸蛋白(NPM)特异性结合。通过成像,研究人员发现MALAT1 rG4s促进了NCL和NPM向核斑点的定位,而破坏rG4结构的特定G-to-A突变损害了斑点中NCL和NPM的定位。体外生物物理研究证实,NCL的截短体(ΔNCL)与所有三种rG4s紧密结合。总体而言,本研究揭示了MALAT1中新的rG4s,确定了它们被NCL和NPM特异性识别,并表明破坏rG4s可以消除这些蛋白质向核斑点的定位。
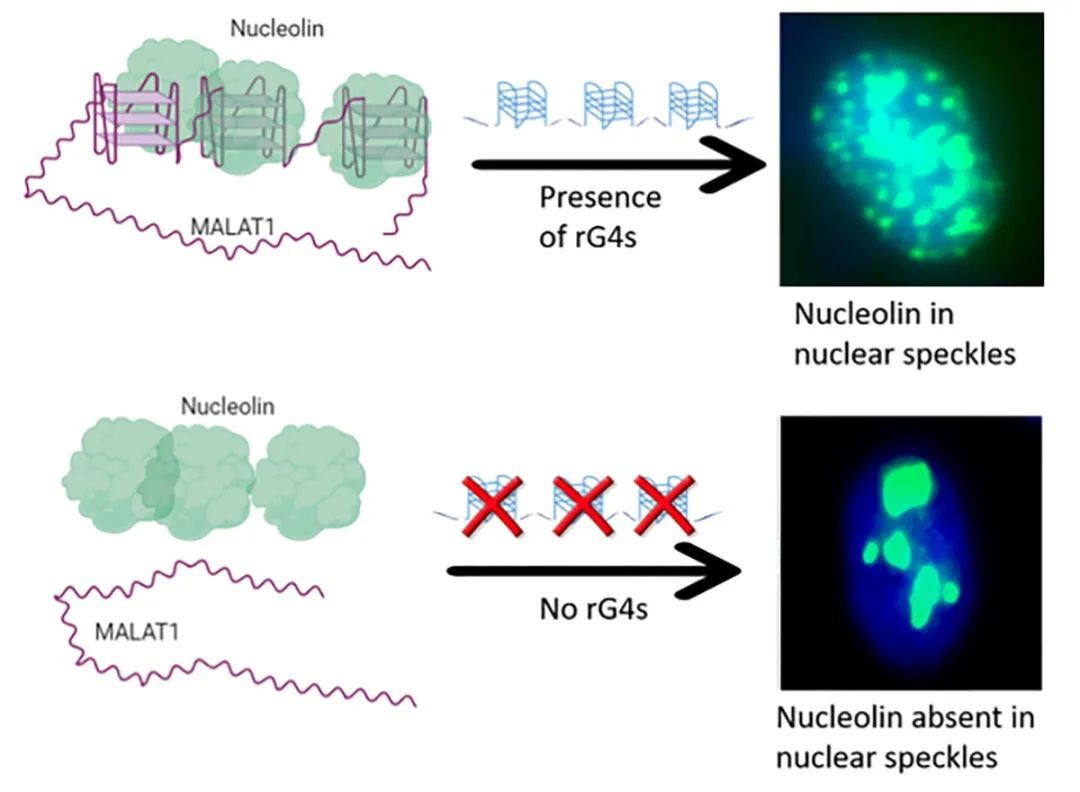
Fig2. 研究模型示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37558241/
03
发表期刊:Int J Oral Sci
影响因子:14.9
发表时间:2023年8月9日
正畸诱导牙根吸收(OIRR)是正畸治疗期间的一个严重并发症。刺激牙骨质修复是治疗OIRR的基本方法。甲状旁腺激素(PTH)可能是OIRR的潜在治疗药物,但其作用仍缺乏直接证据,其潜在机制尚不清楚。本研究旨在探索长链非编码RNAs(lncRNAs)在介导间歇性PTH的合成代谢作用和促进牙骨质修复中的潜在作用,因为鉴定lncRNA与疾病的关联可以为疾病的诊断和治疗提供有价值的见解。本研究发现间歇性PTH通过调节Wnt通路调节永生化小鼠成牙骨质细胞OCCM-30的细胞增殖和矿化。在体内,每天给药PTH足以通过局部抑制Wnt/β-catenin信号来加速根系再生。通过RNA微阵列分析,lncRNA LITTIP(间歇性PTH下LGR6基因间转录本)被鉴定为间歇性PTH下牙骨质发生的关键调节因子。ChIRP和RIP实验显示,LITTIP与富含亮氨酸的重复G蛋白偶联受体6(LGR6)和异质核核糖核蛋白K(HnRNPK)蛋白的mRNA结合。进一步的共转染实验证实,LITTIP在LITTIP/Lgr6/HnRNPK复合物的形成中发挥了结构作用。此外,LITTIP能够通过RNA结合蛋白HnRNPK促进LGR6的表达。总的来说,本研究结果表明,间歇性PTH给药通过抑制Wnt途径加速根系再生。lncRNA LITTIP通过HnRNPK促进的LGR6高表达来激活Wnt/β-catenin信号,被鉴定为负调节牙骨质发生。

Fig3. LITTIP通过LITTIP结合蛋白HnRNPK促进LGR6表达的模型图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37558690/
04
发表期刊:Cell Death & Disease
影响因子:9.0
发表时间:2023年8月15日
异常的5-甲基胞嘧啶(m5C)甲基化已被证明与胃癌的发生、进展和预后密切相关。失调的长链非编码RNAs(lncRNAs)参与了癌症的各种生物学过程。然而,迄今为止,m5C甲基化的lncRNAs在胃癌(GC)中的研究很少。本研究发现RNA胞嘧啶-C(5)-甲基转移酶(NSUN2)在GC中上调,高NSUN2表达与预后不良有关。NR_033928被鉴定为GC中NSUN2甲基化和上调的lncRNA。功能上,NR_033928通过与IGF2BP3 / HUR复合物相互作用来上调谷氨酰胺酶(GLS)的表达,以促进GLS mRNA的稳定性。谷氨酰胺代谢物α-KG的增加,通过增强其启动子5-羟甲基胞嘧啶(hm5C)去甲基化来上调NR_033928的表达。总之,本研究结果表明,NSUN2-甲基化的NR_033928促进了GC进展,可能是GC的潜在预后和治疗靶点。
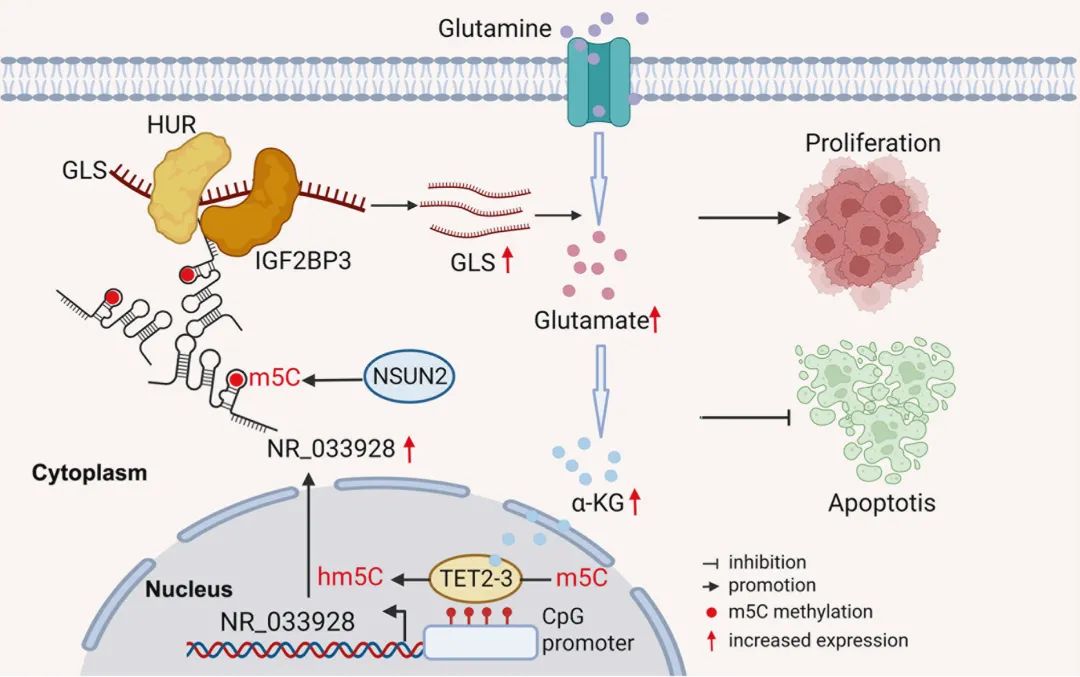
Fig4. NR_033928在GC中的功能示意图
原文链接:
https://www.nature.com/articles/s41419-023-06049-8
05
LncRNA DGCR5编码的多肽RIP通过抑制BMSCs中β-catenin的核定位来加重SONFH
发表期刊:Cell Rep
影响因子:8.8
发表时间:2023年8月12日
骨髓间充质干细胞(BMSCs)的分化命运影响类固醇诱导的股骨头骨坏死(SONFH)的进展。本研究发现lncRNA DGCR5编码一种102个氨基酸的多肽RIP(Rac1灭活肽),该多肽促进BMSCs的成脂分化并加剧SONFH的进展。RIP,而不是lncRNA DGCR5,与RAC1的N末端基序结合,并使RAC1/PAK1级联失活,导致β-catenin的Ser675磷酸化降低。最终,β-catenin的核定位减少,BMSCs的分化平衡向脂肪生成谱系倾斜。在大鼠股骨头中,RIP的过表达导致小梁骨紊乱和脂肪细胞积聚,这可以通过过表达RAC1来挽救。这一发现扩大了lncRNA在BMSCs中的调节作用,并表明RIP是一个潜在的治疗靶点。
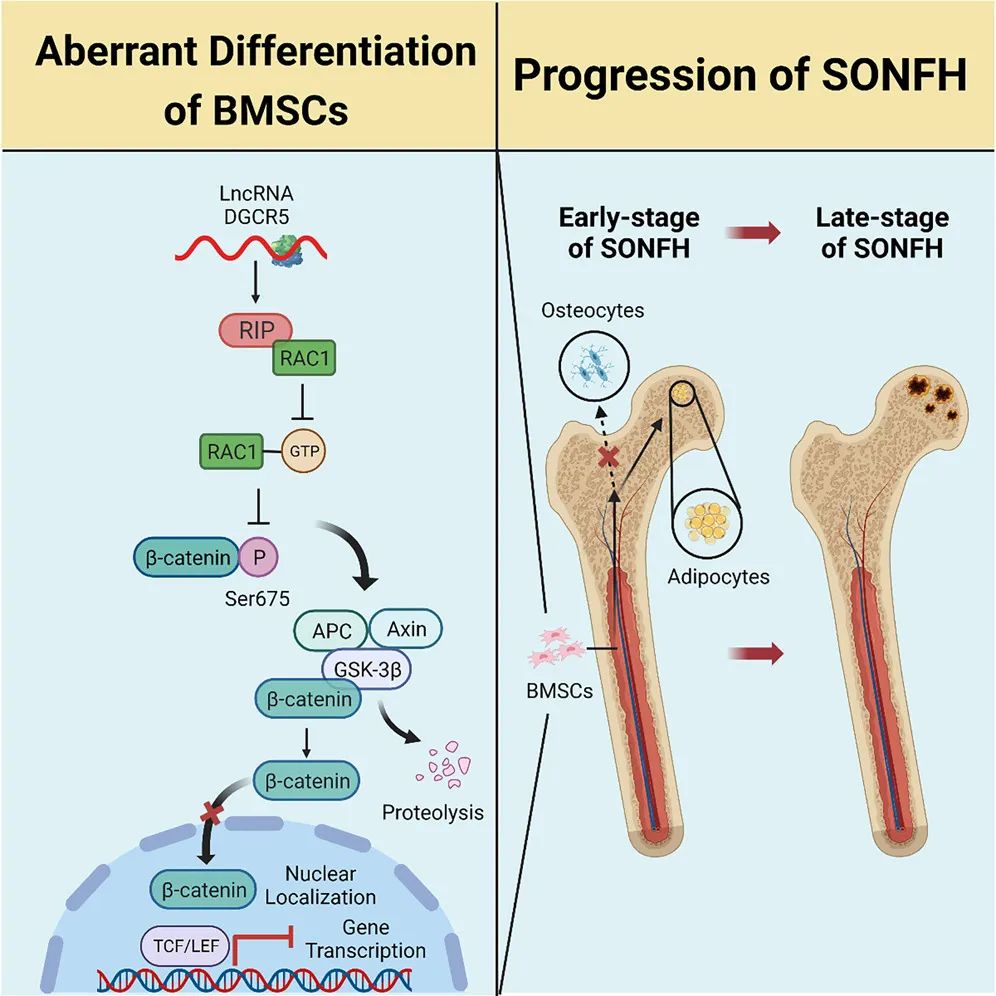
Fig5. 作用模型示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37573506/