推荐产品
公司新闻/正文
Cancer Research丨circFNDC3B加速OSCC血管形成和转移
人阅读 发布时间:2023-04-10 09:14
口腔癌,主要是口腔鳞状细胞癌(OSCC),是第八大最常见的癌症类型,仅在 2020 年,全球就有170000人死亡,新增病例超过370000例。尽管近年来OSCC的诊断和治疗取得了显著进展,但由于肿瘤转移率高,患者的5年生存率仍低于50%,颈淋巴结(LN)转移的存在被认为是OSCC最重要的预后决定因素。然而,导致OSCC通过淋巴管扩散的机制在很大程度上仍然未知。因此,迫切需要研究鉴定潜在生物标志物和治疗靶点的潜在机制,以提高受影响患者的生存率。
LN转移是OSCC的一种主要转移模式,是一个涉及EMT和EMT中间状态(p-EMT)的多步骤过程,与迁移、侵袭和协调转移性肿瘤微环境(TME)如血管生成和淋巴管生成相关。值得注意的是,淋巴管生成是转移进展的关键决定因素,也是患者预后的一个有希望的预测因素。PROX1和SOX18转录因子通过控制内皮细胞分支和扩散的起始来调节淋巴管生成过程。高度转移的肿瘤细胞也可以形成类似于淋巴管的结构,与原生淋巴结构融合,从而促进转移性扩散。此外,淋巴管密度可以预测OSCC患者的无转移生存期。近年来,越来越多的证据强调了环状RNAs(circRNAs)通过其转录和转录后调节活性在淋巴管生成、转移和相关致癌过程中发挥作用,而circRNAs在OSCC中的生理功能尚未完全确定。
circRNAs是一种具有共价闭环结构的非编码RNAs。生物信息学技术已经导致了对成千上万种不同circRNAs的组织特异性表达谱进行表征。虽然产生circRNAs所需的前体RNAs的反向剪接效率低于线性剪接,使得circRNAs的转录水平相对于亲本基因的转录水平降低,但由于其固有的核酸外切酶抗性,circRNAs非常稳定并在细胞内持续存在。这种稳定性导致临床对利用circRNAs作为不同疾病的特异性生物标志物的兴趣日益浓厚。从机制上讲,circRNAs可以螯合互补的microRNAs(miRNAs),从而改变基因表达,如circUHRF1,其通过螯合miR-526b-5p和促进c-Myc上调来驱动OSCC的发展。circRNAs还可以与RNA结合蛋白(RBPs)相互作用,以改变靶基因转录和稳定性,或促进酶共定位。例如,circFoxo3在乳腺癌中促进MDM2介导的p53泛素化和降解。在某些情况下,circRNAs来源的多肽也可以调节某些疾病。circ-LINC-PINT来源的FBXW-185aa可以通过与PAF1c相互作用来抑制几种癌基因的转录伸长,进而抑制胶质母细胞瘤的发展。因此,探索OSCC中的特定circRNAs功能可能为OSCC患者提供更好的诊断和治疗。
FNDC3B(Ⅲ型纤维连接蛋白结构域蛋白3B)基因编码一种主要在内质网(ER)膜上发现的蛋白质,该蛋白质与细胞迁移和粘附有关。研究发现FNDC3B在宫颈癌、鼻咽癌和口腔癌中异常调节。近日,Cancer Research(IF13.312)期刊发表了一篇题为circFNDC3B accelerates vasculature formation and metastasis in oral squamous cell carcinoma的研究论文,报道了一个源自FNDC3B的circRNA(hsa_circ_0001361,circFNDC3B)在OSCC中显著上调并与淋巴结转移相关。揭示了circFNDC3B通过调节多种促癌信号通路来增强癌细胞转移能力和促进血管形成,从而驱动OSCC淋巴结转移的作用机制。暗示circFNDC3B可能是减少OSCC转移的潜在靶标。
首先,研究人员采用GSE131182和GSE197138数据集分析成对OSCC样品中的circRNAs表达,分别鉴定出624个和415个过表达circRNAs。其中,共同上调的circRNAs有29个,包括hsa_circ_0001361、hsa_circ_0002805、hsa_circ_0089489。qRT-PCR检测显示hsa_circ_0001361在OSCC细胞系和癌组织中显著上调,且其过表达与无复发生存率差呈正相关。FISH实验显示,hsa_circ_0001361在LN转移的原发肿瘤中显著上调,并与转移性LN中的hsa_circ_0001361表达呈正相关。表明hsa_circ_0001361在口腔鳞状细胞癌组织和细胞中高度表达,并与LN转移相关。
随后,研究人员通过circBase数据库分析了hsa_circ_0001361的结构,发现215个核苷酸circRNA编码在chr3:171830241-171851336,是FNDC3B外显子2和3反向剪接的结果,故命名为circFNDC3B。进一步的qRT-PCR、Sanger测序、RNase R消化实验、RNA稳定性检测证实了circFNDC3B是OSCC中高度稳定的circRNA。核质分离和FISH实验显示circFNDC3B主要位于细胞质中。

Fig1. OSCC中hsa_circ_0001361的鉴定和表征
接下来的功能研究显示,敲低circFNDC3B显著抑制了OSCC细胞的迁移、侵袭、EMT和转移,而过表达circFNDC3B则得到相反的结果。此外,鉴于血管生成和淋巴管生成在癌的转移中起着至关重要的作用,研究人员进一步探讨了circFNDC3B是否促进了血管生成和淋巴管生成。结果证实了circFNDC3B在OSCC中显著促进了血管生成和淋巴管生成。

Fig2. circFNDC3B加速OSCC细胞的迁移、侵袭、EMT和转移
为了研究circFNDC3B促进OSCC进展的机制,研究人员使用生物素化circFNDC3B特异性探针进行RNA pulldown实验。结果显示circFNDC3B在OSCC细胞中与RNA结合蛋白FUS结合。进一步的研究发现,circFNDC3B可促进泛素介导的FUS降解,然后调节HIF1A和VEGFA的表达,进而增强TME中的血管生成。此外,circFNDC3B螯合miR-181c-5p以促进淋巴内皮细胞命运调节因子PROX1和部分EMT标志物Serpine1的上调,从而驱动TME的转移性肿瘤活性和淋巴管生成。
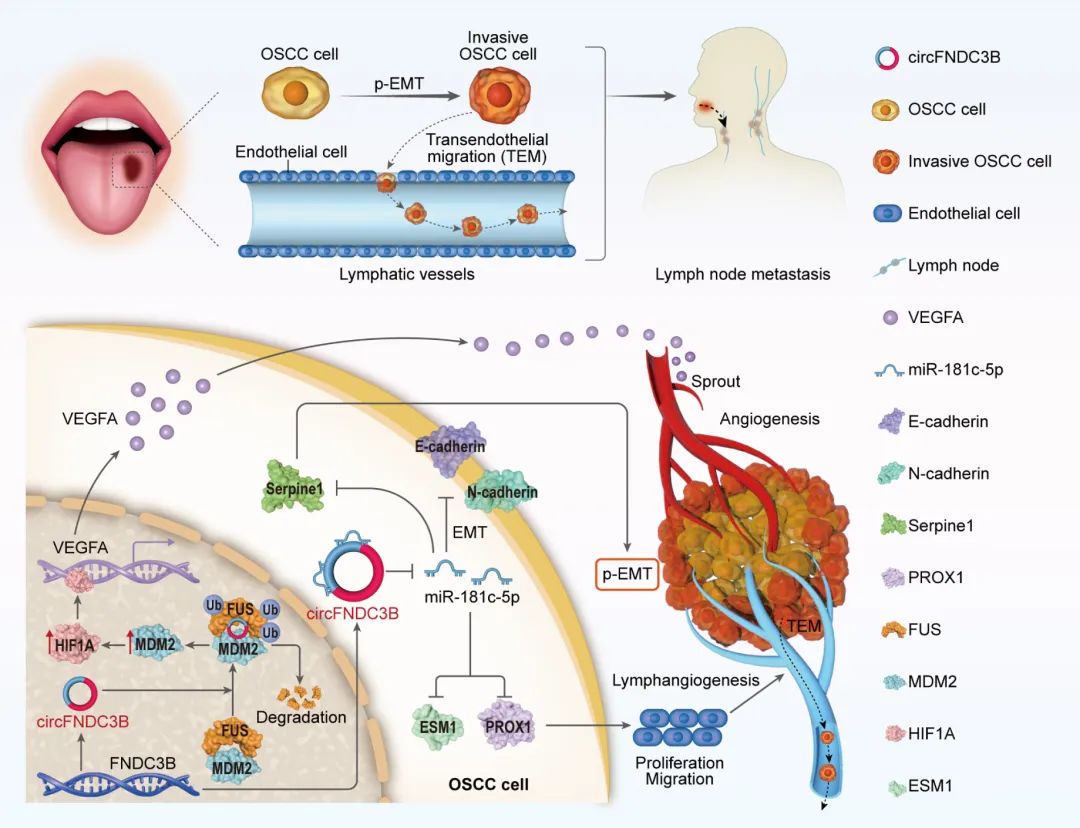
Fig3. circFNDC3B促进OSCC进展的机制模型图
最后,研究人员进行了体内功能验证实验,结果显示circFNDC3B敲低与较低的LN体积有关,而与对照细胞植入相比,其过表达增加了LN微转移。随后的免疫荧光染色表明,sh-circFNDC3B组淋巴管生成和血管生成的标志物下调,而LV-circFNDC3B组表达上调。此外,为了进一步探索VEGFA和miR-181c-5p在circFNDC3B介导的OSCC转移中的作用,研究人员将贝伐珠单抗(BEV)和miR-181c-5p antagomir用于舌癌模型。结果显示,BEV联合sh-circFNDC3B抑制TME和转移性LN的血管生成,而miR-181c-5p antagomir加重了LV-circFNDC3B促进肿瘤相关淋巴管生成和LN转移的作用。这些结果表明circFNDC3B通过促进转移性TME中的血管生成/淋巴管生成来增强OSCC的转移。
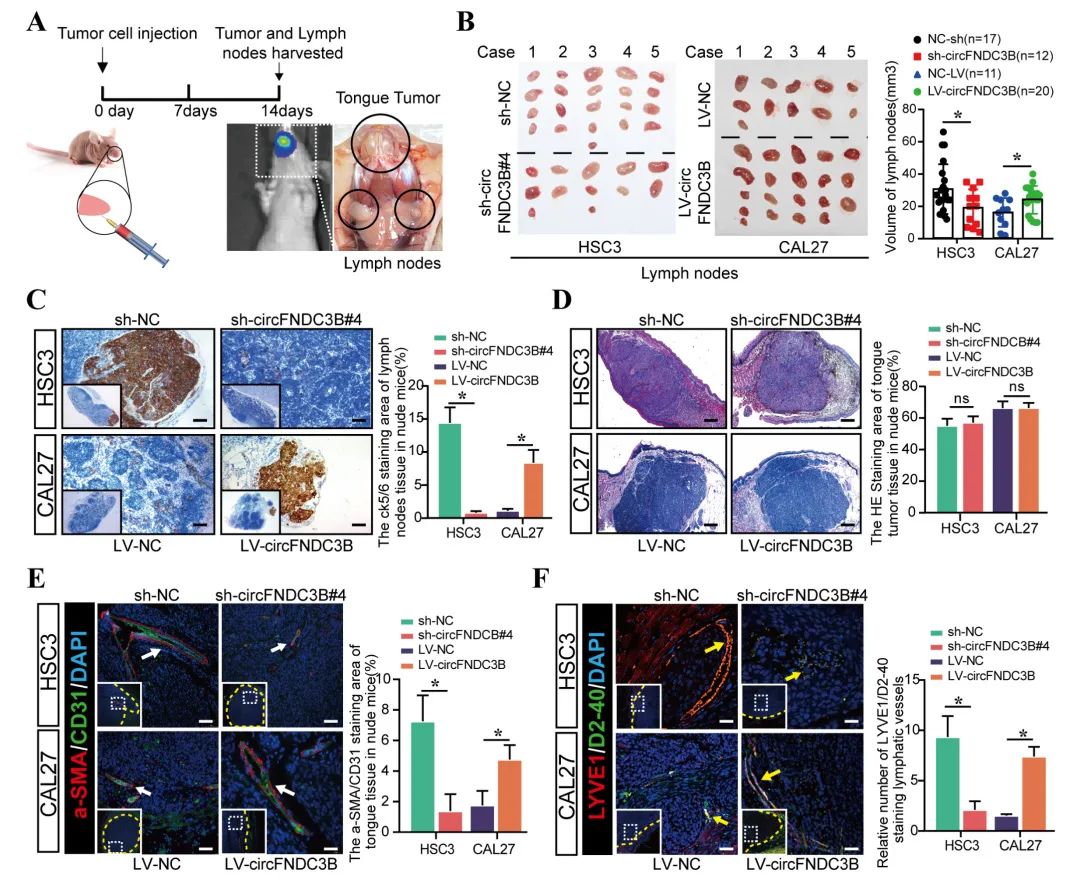
Fig4. circFNDC3B增强OSCC的体内转移和相关新生血管形成
总之,本研究证明了circFNDC3B作为癌基因在OSCC中具有多效性功能,一方面增强了OSCC细胞的侵袭和转移能力,另一方面促进了肿瘤微环境中的血管生成和淋巴管生成。circFNDC3B通过与RBPs相互作用和充当microRNAs海绵,分别调节细胞核中的FUS/MDM2/HIF1A/VEGFA轴和细胞质中的miR-181c-5p/Serpine1/PROX1轴。本研究拓宽了circRNAs在促进癌症转移方面的知识,并提出了circFNDC3B可以成为OSCC诊断和治疗的潜在靶点的新见解。
原文链接:https://europepmc.org/article/med/36811957
本研究中使用到的动物用miRNA antagomir、生物素标记RNA探针、FISH探针与试剂盒均由锐博生物提供! 即日起-4月30日,在线订购miRNA antagomir≥1mg,可享受5折特价优惠 ,更多促销信息欢迎登陆锐博生物官网www.ribobio.com进行查看!










