推荐产品
公司新闻/正文
lncRNA研究进展盘点(20220722)
人阅读 发布时间:2022-07-22 09:38
LncRNA CTBP1-DT-encoded microprotein DDUP sustains DNA damage response signalling to trigger dual DNA repair mechanisms
LncRNA CTBP1-DT编码的蛋白DDUP维持DNA损伤响应信号以触发双重DNA修复机制
发表期刊:Nucleic Acids Res
影响因子:19.160
发表时间:2022年7月18日
通过在受损部位保留DDR因子来维持DNA损伤响应(DDR)信号对于传输损伤感应和修复信号非常重要。本研究发现 DNA 损伤引发了lncRNA CTBP1-DT中核糖体与IRES区域的关联,克服了上游开放阅读框(uORF)的负面影响,并通过一种帽非依赖性的翻译机制诱导了微蛋白DDUP(DNA损伤上调蛋白)的翻译。激活的ATR激酶介导的DDUP磷酸化诱导了剧烈的“dense-to-loose”的构象变化,从而在受损部位维持了RAD18/RAD51C和RAD18/PCNA复合物,并启动了RAD51C介导的同源重组和PCNA介导的复制后修复机制。重要的是,用ATR抑制剂治疗消除了DDUP对RAD51C和PCNA染色质保留的影响,从而导致癌细胞对DNA损伤化疗药物过敏。总之,本研究结果揭示了DDR维持的一个合理机制,并可能代表一种有吸引力的治疗策略,以改善基于DNA损伤的抗癌疗法。
原文链接:https://pubmed.ncbi.nlm.nih.gov/35849344/
The HHIP-AS1 lncRNA promotes tumorigenicity through stabilization of dynein complex 1 in human SHH-driven tumors
HHIP-AS1 lncRNA通过稳定人SHH驱动肿瘤中的动力蛋白复合物1来促进致瘤性
发表期刊:Nat Commun
影响因子:17.694
发表时间:2022年7月13日
大多数lncRNAs显示出物种特异性的表达模式,这表明癌症的动物模型可能只是不完全地再现了人类lncRNAs与致癌通路之间的调控相互作用。在这些通路中,Sonic Hedgehog(SHH)信号在几种人类癌症实体中被异常激活。本研究揭示了灵长类动物特异性lncRNA HHIP-AS1(HedgeHog相互作用蛋白-反义1)的异常表达是SHH驱动肿瘤(包括髓母细胞瘤和横纹肌样瘤)的一个标志。HHIP-AS1是由与SHH调节因子HHIP共享的双向启动子主动转录的。体内外敲低HHIP-AS1可诱导有丝分裂纺锤体失调,从而损害致瘤性。机制上,HHIP-AS1直接与DYNC1I2(胞浆动力蛋白1中间链2)mRNA结合,并通过hsa-miR-425-5p减弱其降解。研究人员发现HHIP-AS1和DYNC1I2中的相应调节元件在小鼠中都不是进化保守的。总之,本研究发现了一种lncRNA介导的机制,该机制能够在人类肿瘤中实现SHH通路激活发挥促有丝分裂作用。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35831316/
PDIA3P1 promotes Temozolomide resistance in glioblastoma by inhibiting C/EBPβ degradation to facilitate proneural-to-mesenchymal transition
PDIA3P1通过抑制C/EBPβ降解来促进原神经-间质转化,从而促进胶质母细胞瘤对替莫唑胺的耐药性
发表期刊:J Exp Clin Cancer Res
影响因子:12.658
发表时间:2022年7月15日
背景:对替莫唑胺(TMZ)的耐药性是预防胶质母细胞瘤(GBM)术后复发的主要障碍。尽管长链非编码RNAs(lncRNAs)在GBM中发挥多种作用,但调节TMZ耐药的lncRNAs尚未明确阐明。本研究旨在鉴定可能影响TMZ治疗敏感性的lncRNAs,并探索新的治疗策略来克服GBM中TMZ耐药性。
结果:本研究鉴定了一个lncRNA PDIA3P1,其在TMZ耐药的GBM细胞系中表达上调。过表达PDIA3P1促进了TMZ耐药的获得,而敲低PDIA3P1恢复了TMZ敏感性。PDIA3P1在MES-GBM中上调,促进GSCs中的PMT进展,并导致GBMs对TMZ治疗更具耐药性。机制上,PDIA3P1破坏了C/EBPβ-MDM2复合物并通过阻止MDM2介导的泛素化来稳定C/EBPβ蛋白。PDIA3P1的表达以时间和浓度依赖性的方式上调以响应TMZ处理,而TMZ诱导的PDIA3P1上调是通过p38α-MAPK信号通路介导的。NEF是一种特异性靶向具有出色血脑屏障(BBB)渗透性的p38α的小分子药物。当与特定浓度的TMZ合用时,NEF阻断了TMZ响应的PDIA3P1上调并产生协同效应。TMZ和NEF的组合在体外和体内均表现出优异的协同抗肿瘤作用。
结论:PDIA3P1通过稳定C/EBPβ促进PMT,降低GBM细胞对TMZ治疗的敏感性。NEF抑制TMZ响应的PDIA3P1上调,NEF与TMZ联合可提供更好的抗肿瘤作用。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35836243/
Long non-coding RNA EVADR induced by Fusobacterium nucleatum infection promotes colorectal cancer metastasis
具核梭杆菌(F. nucleatum)感染诱导的lncRNA EVADR促进结直肠癌转移
发表期刊:Cell Reports
影响因子:9.995
发表时间:2022年7月19日
具核梭杆菌(F. nucleatum)和长链非编码RNA(lncRNA)EVADR均与结直肠癌(CRC)相关,但它们与结直肠癌转移的关系以及EVADR促进结直肠癌转移的机制尚不清楚。本研究报道了F. nucleatum促进结直肠癌细胞向肝脏和肺转移,并且可以在小鼠模型的CRC转移定植中检测到。此外,F. nucleatum上调EVADR的表达,这可以增加CRC细胞在体内和体外的转移能力。机制上,EVADR升高可作为Y-box结合蛋白1(YBX1)的模块化支架,直接增强上皮-间质转化(EMT)相关因子(如Snail、Slug和Zeb1)的翻译。这些发现表明,由F. nucleatum诱导的EVADR通过YBX1依赖性翻译促进结直肠癌转移。EVADR-YBX1轴可能有助于预防和治疗具有F. nucleatum相关CRC转移的患者。

原文链接:https://www.cell.com/cell-reports/fulltext/S2211-1247(22)00933-0
Modular scaffolding by lncRNA HOXA10-AS promotes oral cancer progression
lncRNA HOXA10-AS的模块化支架促进口腔癌进展
发表期刊:Cell Death Dis
影响因子:9.685
发表时间:2022年7月20日
最近的研究表明,长链非编码RNAs(lncRNAs)是多种生物过程的关键基因调节因子,尽管它们缺乏蛋白质编码能力。越来越多的证据表明,lncRNAs在介导细胞信号通路,尤其是与肿瘤发生相关的信号通路方面具有重要意义。因此,lncRNAs已成为癌症发展和恶性肿瘤的新型功能调节因子和指标。最近的转录组学分析已经鉴定出一种肿瘤偏向表达的lncRNA,即HOXA10-AS转录本,其表达与患者生存相关。基于功能细胞的分析表明,HOXA10-AS转录本在调节口腔癌生长和转移中是必不可少的。LncRNA表达也与药物敏感性有关。本研究鉴定了HOXA10-AS作为TP63 mRNA加工的模块化支架,并参与调节癌症的生长。这些发现为lncRNA介导的分子调控提供了功能解释,突出了lncRNA转录组在癌症生物学中的重要性。

原文链接:https://www.nature.com/articles/s41419-022-05071-6
LncRNA CTBP1-DT编码的蛋白DDUP维持DNA损伤响应信号以触发双重DNA修复机制
发表期刊:Nucleic Acids Res
影响因子:19.160
发表时间:2022年7月18日
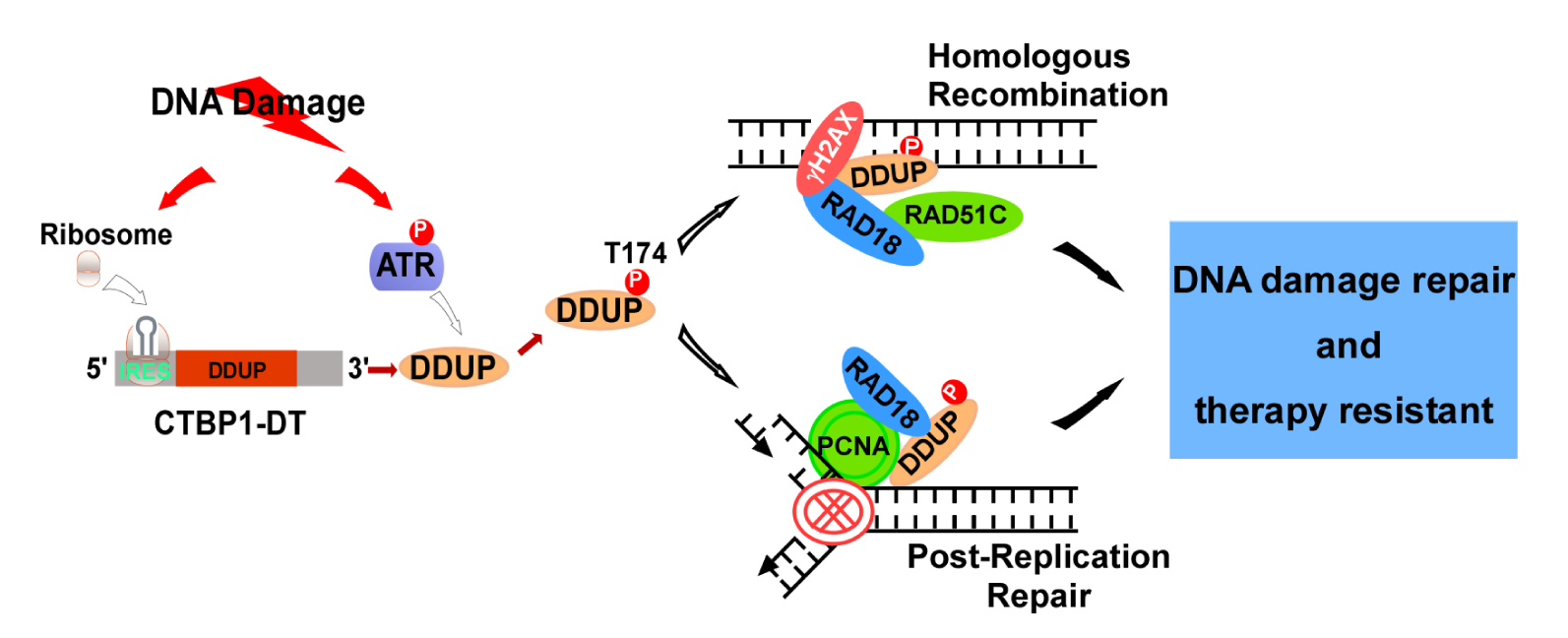
通过在受损部位保留DDR因子来维持DNA损伤响应(DDR)信号对于传输损伤感应和修复信号非常重要。本研究发现 DNA 损伤引发了lncRNA CTBP1-DT中核糖体与IRES区域的关联,克服了上游开放阅读框(uORF)的负面影响,并通过一种帽非依赖性的翻译机制诱导了微蛋白DDUP(DNA损伤上调蛋白)的翻译。激活的ATR激酶介导的DDUP磷酸化诱导了剧烈的“dense-to-loose”的构象变化,从而在受损部位维持了RAD18/RAD51C和RAD18/PCNA复合物,并启动了RAD51C介导的同源重组和PCNA介导的复制后修复机制。重要的是,用ATR抑制剂治疗消除了DDUP对RAD51C和PCNA染色质保留的影响,从而导致癌细胞对DNA损伤化疗药物过敏。总之,本研究结果揭示了DDR维持的一个合理机制,并可能代表一种有吸引力的治疗策略,以改善基于DNA损伤的抗癌疗法。

Fig1. lncRNA编码的DDUP通过调控PCNA单泛素化和RAD18在DNA损伤位点的保留来协调DNA损伤修复的模型示意图
原文链接:https://pubmed.ncbi.nlm.nih.gov/35849344/
The HHIP-AS1 lncRNA promotes tumorigenicity through stabilization of dynein complex 1 in human SHH-driven tumors
HHIP-AS1 lncRNA通过稳定人SHH驱动肿瘤中的动力蛋白复合物1来促进致瘤性
发表期刊:Nat Commun
影响因子:17.694
发表时间:2022年7月13日
大多数lncRNAs显示出物种特异性的表达模式,这表明癌症的动物模型可能只是不完全地再现了人类lncRNAs与致癌通路之间的调控相互作用。在这些通路中,Sonic Hedgehog(SHH)信号在几种人类癌症实体中被异常激活。本研究揭示了灵长类动物特异性lncRNA HHIP-AS1(HedgeHog相互作用蛋白-反义1)的异常表达是SHH驱动肿瘤(包括髓母细胞瘤和横纹肌样瘤)的一个标志。HHIP-AS1是由与SHH调节因子HHIP共享的双向启动子主动转录的。体内外敲低HHIP-AS1可诱导有丝分裂纺锤体失调,从而损害致瘤性。机制上,HHIP-AS1直接与DYNC1I2(胞浆动力蛋白1中间链2)mRNA结合,并通过hsa-miR-425-5p减弱其降解。研究人员发现HHIP-AS1和DYNC1I2中的相应调节元件在小鼠中都不是进化保守的。总之,本研究发现了一种lncRNA介导的机制,该机制能够在人类肿瘤中实现SHH通路激活发挥促有丝分裂作用。

Fig2. HHIP-AS1缺失可延长SHH驱动的体内脑肿瘤模型的生存期
原文链接:https://pubmed.ncbi.nlm.nih.gov/35831316/
PDIA3P1 promotes Temozolomide resistance in glioblastoma by inhibiting C/EBPβ degradation to facilitate proneural-to-mesenchymal transition
PDIA3P1通过抑制C/EBPβ降解来促进原神经-间质转化,从而促进胶质母细胞瘤对替莫唑胺的耐药性
发表期刊:J Exp Clin Cancer Res
影响因子:12.658
发表时间:2022年7月15日
背景:对替莫唑胺(TMZ)的耐药性是预防胶质母细胞瘤(GBM)术后复发的主要障碍。尽管长链非编码RNAs(lncRNAs)在GBM中发挥多种作用,但调节TMZ耐药的lncRNAs尚未明确阐明。本研究旨在鉴定可能影响TMZ治疗敏感性的lncRNAs,并探索新的治疗策略来克服GBM中TMZ耐药性。
结果:本研究鉴定了一个lncRNA PDIA3P1,其在TMZ耐药的GBM细胞系中表达上调。过表达PDIA3P1促进了TMZ耐药的获得,而敲低PDIA3P1恢复了TMZ敏感性。PDIA3P1在MES-GBM中上调,促进GSCs中的PMT进展,并导致GBMs对TMZ治疗更具耐药性。机制上,PDIA3P1破坏了C/EBPβ-MDM2复合物并通过阻止MDM2介导的泛素化来稳定C/EBPβ蛋白。PDIA3P1的表达以时间和浓度依赖性的方式上调以响应TMZ处理,而TMZ诱导的PDIA3P1上调是通过p38α-MAPK信号通路介导的。NEF是一种特异性靶向具有出色血脑屏障(BBB)渗透性的p38α的小分子药物。当与特定浓度的TMZ合用时,NEF阻断了TMZ响应的PDIA3P1上调并产生协同效应。TMZ和NEF的组合在体外和体内均表现出优异的协同抗肿瘤作用。
结论:PDIA3P1通过稳定C/EBPβ促进PMT,降低GBM细胞对TMZ治疗的敏感性。NEF抑制TMZ响应的PDIA3P1上调,NEF与TMZ联合可提供更好的抗肿瘤作用。

Fig3. 工作模型图显示PDIA3P1在促进GBM细胞TMZ抗性中起关键作用
原文链接:https://pubmed.ncbi.nlm.nih.gov/35836243/
Long non-coding RNA EVADR induced by Fusobacterium nucleatum infection promotes colorectal cancer metastasis
具核梭杆菌(F. nucleatum)感染诱导的lncRNA EVADR促进结直肠癌转移
发表期刊:Cell Reports
影响因子:9.995
发表时间:2022年7月19日
具核梭杆菌(F. nucleatum)和长链非编码RNA(lncRNA)EVADR均与结直肠癌(CRC)相关,但它们与结直肠癌转移的关系以及EVADR促进结直肠癌转移的机制尚不清楚。本研究报道了F. nucleatum促进结直肠癌细胞向肝脏和肺转移,并且可以在小鼠模型的CRC转移定植中检测到。此外,F. nucleatum上调EVADR的表达,这可以增加CRC细胞在体内和体外的转移能力。机制上,EVADR升高可作为Y-box结合蛋白1(YBX1)的模块化支架,直接增强上皮-间质转化(EMT)相关因子(如Snail、Slug和Zeb1)的翻译。这些发现表明,由F. nucleatum诱导的EVADR通过YBX1依赖性翻译促进结直肠癌转移。EVADR-YBX1轴可能有助于预防和治疗具有F. nucleatum相关CRC转移的患者。

Fig4. F. nucleatum通过lncRNA EVADR-YBX1轴促进CRC转移的机制模型
原文链接:https://www.cell.com/cell-reports/fulltext/S2211-1247(22)00933-0
Modular scaffolding by lncRNA HOXA10-AS promotes oral cancer progression
lncRNA HOXA10-AS的模块化支架促进口腔癌进展
发表期刊:Cell Death Dis
影响因子:9.685
发表时间:2022年7月20日
最近的研究表明,长链非编码RNAs(lncRNAs)是多种生物过程的关键基因调节因子,尽管它们缺乏蛋白质编码能力。越来越多的证据表明,lncRNAs在介导细胞信号通路,尤其是与肿瘤发生相关的信号通路方面具有重要意义。因此,lncRNAs已成为癌症发展和恶性肿瘤的新型功能调节因子和指标。最近的转录组学分析已经鉴定出一种肿瘤偏向表达的lncRNA,即HOXA10-AS转录本,其表达与患者生存相关。基于功能细胞的分析表明,HOXA10-AS转录本在调节口腔癌生长和转移中是必不可少的。LncRNA表达也与药物敏感性有关。本研究鉴定了HOXA10-AS作为TP63 mRNA加工的模块化支架,并参与调节癌症的生长。这些发现为lncRNA介导的分子调控提供了功能解释,突出了lncRNA转录组在癌症生物学中的重要性。

Fig5. HOXA10-AS 转录本作为TP63 RNA加工的模块化支架
原文链接:https://www.nature.com/articles/s41419-022-05071-6










