推荐产品
公司新闻/正文
lncRNA新研究进展盘点(20220317)
人阅读 发布时间:2022-03-17 09:08
Transcriptional kinetics and molecular functions of long noncoding RNAs
长链非编码RNAs的转录动力学和分子功能
发表期刊:Nature Genetics
影响因子:38.330
发表时间:2022年3月3日
越来越多的长链非编码RNAs(lncRNAs)已被实验证实具有重要的功能,但对它们的转录动力学知之甚少,确定它们的调控作用仍然具有挑战性。本研究使用等位基因敏感的单细胞RNA测序证明了与信使RNAs相比,lncRNAs在两次转录爆发之间的持续时间是信使RNAs的两倍。此外,研究人员观察到lncRNA表达的细胞间变异性增加,这是由于较低频率的爆发产生了更多的RNA分子。利用异步生长细胞的异质性,研究人员鉴定并通过实验验证了具有细胞状态特异性功能的lncRNAs,这些功能涉及细胞周期进程和细胞凋亡。最后,研究人员确定了具有顺式功能的lncRNAs,并发现这些lncRNAs的敲低可以调节附近蛋白质编码基因的转录爆发频率或大小。总之,本研究确定了lncRNAs的不同转录调控,并证明了lncRNAs在调节mRNA转录爆发中的作用。
原文链接:https://pubmed.ncbi.nlm.nih.gov/35241826/
Interaction of lncRNA MIR100HG with hnRNPA2B1 facilitates m 6 A-dependent stabilization of TCF7L2 mRNA and colorectal cancer progression
lncRNA MIR100HG与hnRNPA2B1的相互作用促进TCF7L2 mRNA的m6A依赖性稳定和结直肠癌进展
发表期刊:Mol Cancer
影响因子:27.401
发表时间:2022年3月12日
研究背景:上皮间充质转化(EMT)是一个与转移和耐药性相关的过程,其中非编码RNAs(ncRNAs)发挥着关键作用。之前的研究表明,嵌入ncRNA宿主基因MIR100HG第三个内含子中的miR-100和miR-125b在结直肠癌(CRC)中赋予对西妥昔单抗【一种抗表皮生长因子受体(EGFR)单克隆抗体】的耐药性。然而,MIR100HG转录本本身是否在西妥昔单抗耐药或EMT中发挥作用尚不清楚。
研究结果:MIR100HG的表达与EMT标志物密切相关,是EMT的正向调节因子。MIR100HG在体外和体内均能维持西妥昔单抗耐药并促进CRC细胞的侵袭和转移。hnRNPA2B1被鉴定为MIR100HG的结合分子。机制上讲,MIR100HG通过与hnRNPA2B1相互作用维持了TCF7L2 的mRNA稳定性,TCF7L2是Wnt/β-catenin信号传导的主要转录共激活因子。hnRNPA2B1在MIR100HG存在的情况下识别TCF7L2 mRNA的N6-甲基腺苷(m6A)位点。反过来,TCF7L2激活MIR100HG的转录,形成前馈调节环。MIR100HG/hnRNPA2B1/TCF7L2轴在出现局部或远处转移或与西妥昔单抗耐药相关疾病进展的CRC患者标本中得到增强。
研究结论:MIR100HG和hnRNPA2B1相互作用通过调节TCF7L2 mRNA的稳定性来控制CRC中Wnt信号的转录活性。本研究结果确定MIR100HG是CRC中的一种有效的EMT诱导剂,可能通过激活MIR100HG/hnRNPA2B1/TCF7L2反馈回路导致西妥昔单抗耐药和转移。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35279145/
Long non-coding RNA LINC00680 functions as a ceRNA to promote esophageal squamous cell carcinoma progression through the miR-423-5p/PAK6 axis
长链非编码RNA LINC00680作为ceRNA通过miR-423-5p/PAK6轴促进食管鳞状细胞癌进展
发表期刊:Mol Cancer
影响因子:27.401
发表时间:2022年3月7日
研究背景:食管鳞状细胞癌(ESCC)是世界范围内常见的侵袭性恶性肿瘤,临床预后较差。据报道,越来越多的长链非编码RNAs(lncRNAs)与癌症发展有关。然而,在ESCC中发挥作用的lncRNAs及其潜在的分子机制在很大程度上仍然未知。
研究结果:转录组分析显示,大量lncRNAs在ESCC组织中失调。值得注意的是,LINC00680是高表达的,并且LINC00680的上调与大肿瘤、晚期肿瘤分期和不良预后相关。功能上,LINC00680的敲低在体外抑制了ESCC细胞的增殖、集落形成、迁移和侵袭,并在体内抑制肿瘤生长。机制上,LINC00680被发现作为一种ceRNA,通过充当miR-423-5p海绵来调节ESCC细胞中PAK6(p21活化激酶6)的表达。在PAK6恢复和miR-423-5p抑制后,LINC00680敲低诱导的细胞活力和运动抑制显著逆转。此外,靶向LINC00680的ASO在体外和体内都显著抑制了ESCC。
研究结论:总之,本研究确定了一种ESCC中的致癌lncRNA LINC00680,其通过充当miR-423-5p海绵发挥ceRNA作用,从而促进PAK6表达和随后的ESCC进展。暗示了LINC00680/miR-423-5p/PAK6轴可作为一个有前景的ESCC诊断和预后生物标志物和治疗靶点。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35255921/
Loss of NPPA-AS1 promotes heart regeneration by stabilizing SFPQ-NONO heteromer-induced DNA repair
NPPA-AS1的缺失通过稳定SFPQ-NONO异聚体诱导的DNA修复促进心脏再生
发表期刊:Basic Res Cardiol
影响因子:17.165
发表时间:2022年3月5日
长链非编码RNA(lncRNA)在内源性心脏再生中的作用在很大程度上仍然不清楚。哺乳动物心肌细胞能够在出生后的一段时间内再生。这一事实允许探索关键lncRNAs在调节心脏再生中的作用。通过新生小鼠左心室心尖切除(AR)的心脏再生模型,本研究鉴定了一种名为NPPA-AS1(natriuretic peptide A antisense RNA 1)的lncRNA,其负调控心肌细胞增殖。在新生小鼠中,NPPA-AS1缺失不影响心脏发育,但足以延长AR后的出生后再生窗口。在成年小鼠中,NPPA-AS1缺失可改善心肌梗塞(MI)后的心脏功能并减少梗塞面积,这与心肌细胞增殖的显著改善有关。进一步分析表明,NPPA-AS1与DNA修复相关的分子SFPQ(脯氨酸/谷氨酰胺富含性剪接因子)相互作用。双链DNA断裂修复需要SFPQ和NONO(含非POU域八聚体结合蛋白)的异聚体,但由于SFPQ和NONO的结合位点重叠,NPPA-AS1与SFPQ竞争性结合。NPPA-AS1缺失促进了SFPQ-NONO异聚体的结合,减少了DNA损伤,并激活了心肌细胞细胞周期的重新进入。总之,NPPA-AS1的缺失通过稳定SFPQ-NONO异聚体诱导的DNA修复来促进心肌细胞增殖,并对成年小鼠的MI发挥治疗作用。因此,NPPA-AS1可能是刺激心脏再生治疗MI的新靶点。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35247074/
Cancer-associated fibroblast-induced lncRNA UPK1A-AS1 confers platinum resistance in pancreatic cancer via efficient double-strand break repair
癌症相关成纤维细胞诱导的lncRNA UPK1A-AS1通过有效的双链断裂修复赋予胰腺癌铂类耐药性
发表期刊:Oncogene
影响因子:9.867
发表时间:2022年3月9日
胰腺导管腺癌(PDAC)的肿瘤基质以大量且异质性的癌症相关成纤维细胞(CAFs)为特征,这些成纤维细胞与化疗耐药性密切相关。然而,CAFs在化学抗性中的潜在机制尚不清楚。本研究发现CAFR是来自铂耐药PDAC患者的CAF亚群,其呈现iCAF表型,并且比从铂敏感PDAC患者中分离的CAFS产生更多的IL8。CAFR衍生的IL8促进PDAC中的奥沙利铂化疗耐药。基于对CAF-CM孵育的肿瘤细胞进行长链非编码RNA(lncRNA)表达谱分析,本研究发现UPK1A-AS1的表达直接由IL8/NF-kappa B信号诱导,可作为一种促化学抗性的lncRNA,在活性IL8诱导的奥沙利铂耐药中起着关键作用。值得注意的是,阻断UPK1A-AS1表达的激活会增加体内肿瘤细胞对奥沙利铂的敏感性。机制上,UPK1A-AS1加强了Ku70和Ku80之间的相互作用,以促进非同源末端连接(NHEJ),从而增强DNA双链断裂(DSB)修复。临床上,UPK1A-AS1表达与晚期PDAC患者的IL8表达、较差的化疗反应和较短的无进展生存(PFS)时间呈正相关。总的来说,本研究揭示了lncRNA介导的CAF来源的旁分泌IL8依赖性奥沙利铂耐药机制,并强调UPK1A-AS1是一个潜在的治疗靶点。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35264742/
长链非编码RNAs的转录动力学和分子功能
发表期刊:Nature Genetics
影响因子:38.330
发表时间:2022年3月3日
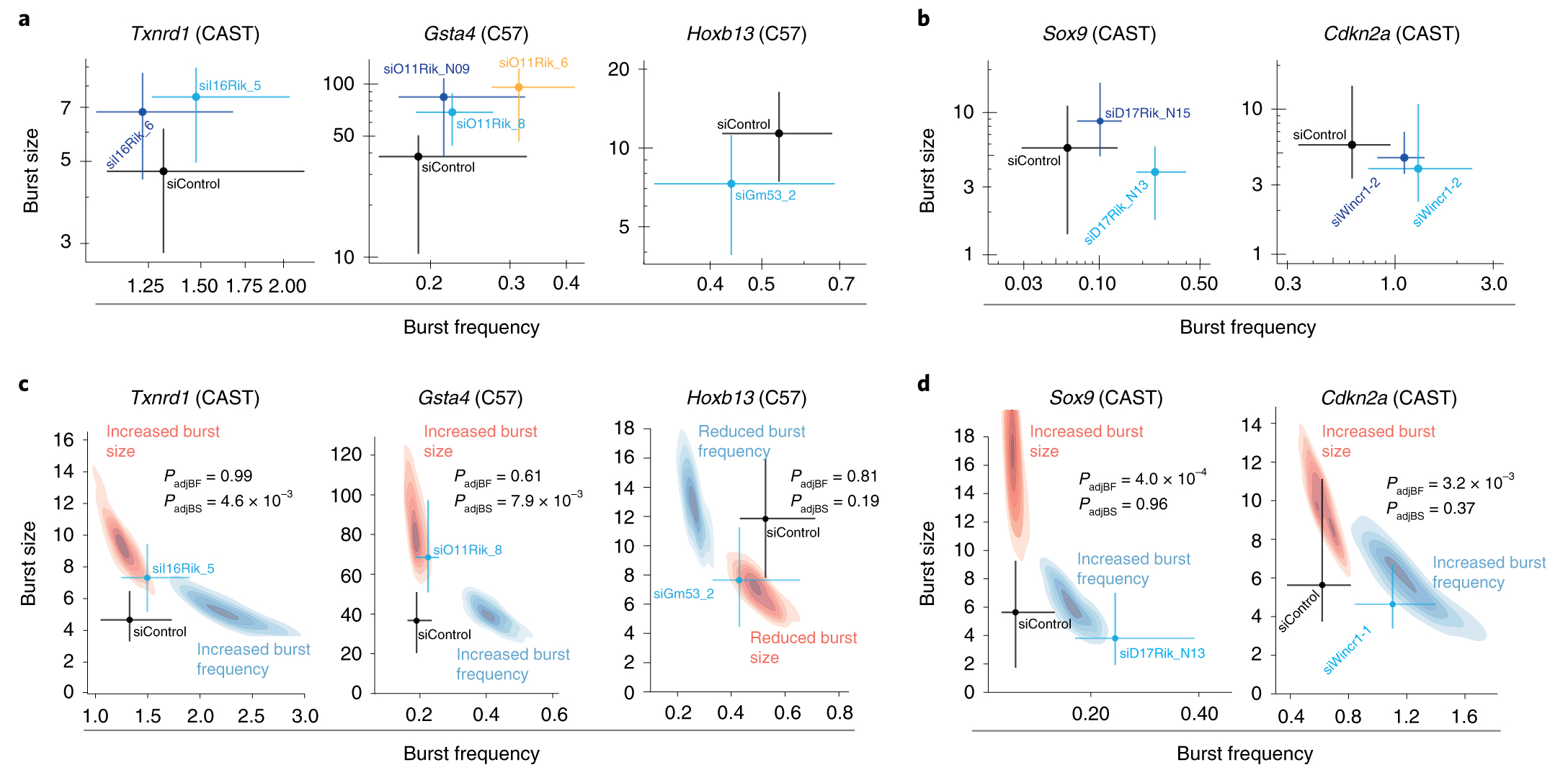
越来越多的长链非编码RNAs(lncRNAs)已被实验证实具有重要的功能,但对它们的转录动力学知之甚少,确定它们的调控作用仍然具有挑战性。本研究使用等位基因敏感的单细胞RNA测序证明了与信使RNAs相比,lncRNAs在两次转录爆发之间的持续时间是信使RNAs的两倍。此外,研究人员观察到lncRNA表达的细胞间变异性增加,这是由于较低频率的爆发产生了更多的RNA分子。利用异步生长细胞的异质性,研究人员鉴定并通过实验验证了具有细胞状态特异性功能的lncRNAs,这些功能涉及细胞周期进程和细胞凋亡。最后,研究人员确定了具有顺式功能的lncRNAs,并发现这些lncRNAs的敲低可以调节附近蛋白质编码基因的转录爆发频率或大小。总之,本研究确定了lncRNAs的不同转录调控,并证明了lncRNAs在调节mRNA转录爆发中的作用。

Fig1. lncRNAs对转录爆发的影响
原文链接:https://pubmed.ncbi.nlm.nih.gov/35241826/
Interaction of lncRNA MIR100HG with hnRNPA2B1 facilitates m 6 A-dependent stabilization of TCF7L2 mRNA and colorectal cancer progression
lncRNA MIR100HG与hnRNPA2B1的相互作用促进TCF7L2 mRNA的m6A依赖性稳定和结直肠癌进展
发表期刊:Mol Cancer
影响因子:27.401
发表时间:2022年3月12日
研究背景:上皮间充质转化(EMT)是一个与转移和耐药性相关的过程,其中非编码RNAs(ncRNAs)发挥着关键作用。之前的研究表明,嵌入ncRNA宿主基因MIR100HG第三个内含子中的miR-100和miR-125b在结直肠癌(CRC)中赋予对西妥昔单抗【一种抗表皮生长因子受体(EGFR)单克隆抗体】的耐药性。然而,MIR100HG转录本本身是否在西妥昔单抗耐药或EMT中发挥作用尚不清楚。
研究结果:MIR100HG的表达与EMT标志物密切相关,是EMT的正向调节因子。MIR100HG在体外和体内均能维持西妥昔单抗耐药并促进CRC细胞的侵袭和转移。hnRNPA2B1被鉴定为MIR100HG的结合分子。机制上讲,MIR100HG通过与hnRNPA2B1相互作用维持了TCF7L2 的mRNA稳定性,TCF7L2是Wnt/β-catenin信号传导的主要转录共激活因子。hnRNPA2B1在MIR100HG存在的情况下识别TCF7L2 mRNA的N6-甲基腺苷(m6A)位点。反过来,TCF7L2激活MIR100HG的转录,形成前馈调节环。MIR100HG/hnRNPA2B1/TCF7L2轴在出现局部或远处转移或与西妥昔单抗耐药相关疾病进展的CRC患者标本中得到增强。
研究结论:MIR100HG和hnRNPA2B1相互作用通过调节TCF7L2 mRNA的稳定性来控制CRC中Wnt信号的转录活性。本研究结果确定MIR100HG是CRC中的一种有效的EMT诱导剂,可能通过激活MIR100HG/hnRNPA2B1/TCF7L2反馈回路导致西妥昔单抗耐药和转移。

Fig2. lncRNA MIR100HG与hnRNPA2B1的相互作用促进TCF7L2 mRNA的m6A依赖性稳定和结直肠癌进展的机制模型示意图
原文链接:https://pubmed.ncbi.nlm.nih.gov/35279145/
Long non-coding RNA LINC00680 functions as a ceRNA to promote esophageal squamous cell carcinoma progression through the miR-423-5p/PAK6 axis
长链非编码RNA LINC00680作为ceRNA通过miR-423-5p/PAK6轴促进食管鳞状细胞癌进展
发表期刊:Mol Cancer
影响因子:27.401
发表时间:2022年3月7日
研究背景:食管鳞状细胞癌(ESCC)是世界范围内常见的侵袭性恶性肿瘤,临床预后较差。据报道,越来越多的长链非编码RNAs(lncRNAs)与癌症发展有关。然而,在ESCC中发挥作用的lncRNAs及其潜在的分子机制在很大程度上仍然未知。
研究结果:转录组分析显示,大量lncRNAs在ESCC组织中失调。值得注意的是,LINC00680是高表达的,并且LINC00680的上调与大肿瘤、晚期肿瘤分期和不良预后相关。功能上,LINC00680的敲低在体外抑制了ESCC细胞的增殖、集落形成、迁移和侵袭,并在体内抑制肿瘤生长。机制上,LINC00680被发现作为一种ceRNA,通过充当miR-423-5p海绵来调节ESCC细胞中PAK6(p21活化激酶6)的表达。在PAK6恢复和miR-423-5p抑制后,LINC00680敲低诱导的细胞活力和运动抑制显著逆转。此外,靶向LINC00680的ASO在体外和体内都显著抑制了ESCC。
研究结论:总之,本研究确定了一种ESCC中的致癌lncRNA LINC00680,其通过充当miR-423-5p海绵发挥ceRNA作用,从而促进PAK6表达和随后的ESCC进展。暗示了LINC00680/miR-423-5p/PAK6轴可作为一个有前景的ESCC诊断和预后生物标志物和治疗靶点。

Fig3. ESCC中LINC00680功能模型示意图
原文链接:https://pubmed.ncbi.nlm.nih.gov/35255921/
Loss of NPPA-AS1 promotes heart regeneration by stabilizing SFPQ-NONO heteromer-induced DNA repair
NPPA-AS1的缺失通过稳定SFPQ-NONO异聚体诱导的DNA修复促进心脏再生
发表期刊:Basic Res Cardiol
影响因子:17.165
发表时间:2022年3月5日
长链非编码RNA(lncRNA)在内源性心脏再生中的作用在很大程度上仍然不清楚。哺乳动物心肌细胞能够在出生后的一段时间内再生。这一事实允许探索关键lncRNAs在调节心脏再生中的作用。通过新生小鼠左心室心尖切除(AR)的心脏再生模型,本研究鉴定了一种名为NPPA-AS1(natriuretic peptide A antisense RNA 1)的lncRNA,其负调控心肌细胞增殖。在新生小鼠中,NPPA-AS1缺失不影响心脏发育,但足以延长AR后的出生后再生窗口。在成年小鼠中,NPPA-AS1缺失可改善心肌梗塞(MI)后的心脏功能并减少梗塞面积,这与心肌细胞增殖的显著改善有关。进一步分析表明,NPPA-AS1与DNA修复相关的分子SFPQ(脯氨酸/谷氨酰胺富含性剪接因子)相互作用。双链DNA断裂修复需要SFPQ和NONO(含非POU域八聚体结合蛋白)的异聚体,但由于SFPQ和NONO的结合位点重叠,NPPA-AS1与SFPQ竞争性结合。NPPA-AS1缺失促进了SFPQ-NONO异聚体的结合,减少了DNA损伤,并激活了心肌细胞细胞周期的重新进入。总之,NPPA-AS1的缺失通过稳定SFPQ-NONO异聚体诱导的DNA修复来促进心肌细胞增殖,并对成年小鼠的MI发挥治疗作用。因此,NPPA-AS1可能是刺激心脏再生治疗MI的新靶点。

Fig4. NPPA-AS1缺失促进SFPQ-NONO异聚体的结合,减少DNA损伤,并激活心肌细胞细胞周期再进入的模型示意图
原文链接:https://pubmed.ncbi.nlm.nih.gov/35247074/
Cancer-associated fibroblast-induced lncRNA UPK1A-AS1 confers platinum resistance in pancreatic cancer via efficient double-strand break repair
癌症相关成纤维细胞诱导的lncRNA UPK1A-AS1通过有效的双链断裂修复赋予胰腺癌铂类耐药性
发表期刊:Oncogene
影响因子:9.867
发表时间:2022年3月9日
胰腺导管腺癌(PDAC)的肿瘤基质以大量且异质性的癌症相关成纤维细胞(CAFs)为特征,这些成纤维细胞与化疗耐药性密切相关。然而,CAFs在化学抗性中的潜在机制尚不清楚。本研究发现CAFR是来自铂耐药PDAC患者的CAF亚群,其呈现iCAF表型,并且比从铂敏感PDAC患者中分离的CAFS产生更多的IL8。CAFR衍生的IL8促进PDAC中的奥沙利铂化疗耐药。基于对CAF-CM孵育的肿瘤细胞进行长链非编码RNA(lncRNA)表达谱分析,本研究发现UPK1A-AS1的表达直接由IL8/NF-kappa B信号诱导,可作为一种促化学抗性的lncRNA,在活性IL8诱导的奥沙利铂耐药中起着关键作用。值得注意的是,阻断UPK1A-AS1表达的激活会增加体内肿瘤细胞对奥沙利铂的敏感性。机制上,UPK1A-AS1加强了Ku70和Ku80之间的相互作用,以促进非同源末端连接(NHEJ),从而增强DNA双链断裂(DSB)修复。临床上,UPK1A-AS1表达与晚期PDAC患者的IL8表达、较差的化疗反应和较短的无进展生存(PFS)时间呈正相关。总的来说,本研究揭示了lncRNA介导的CAF来源的旁分泌IL8依赖性奥沙利铂耐药机制,并强调UPK1A-AS1是一个潜在的治疗靶点。

Fig5. CAFR来源的IL8在PDAC细胞中介导UPK1A -AS1活化以诱导奥沙利铂耐药的模型示意图
原文链接:https://pubmed.ncbi.nlm.nih.gov/35264742/










