推荐产品
公司新闻/正文
lncRNA研究进展盘点丨20230411期
人阅读 发布时间:2023-04-11 08:51
01
HOTAIR:一种潜在的乳腺癌转移、耐药和预后调节因子
发表期刊:Mol Cancer
影响因子:41.444
发表时间:2023年3月30日
HOX转录本反义基因间RNA(HOTAIR)是一种致癌的非编码RNA,其表达与包括乳腺癌(BC)在内的多种癌症的肿瘤分级和预后密切相关。HOTAIR通过充当海绵和表观遗传机制调节各种靶基因,并控制各种致癌细胞和信号机制,包括转移和耐药性。在BC细胞中,HOTAIR表达受多种转录和表观遗传机制的调节。本文描述了癌症发展过程中控制HOTAIR表达的调控机制,并探讨了HOTAIR如何驱动BC的发展、转移和耐药性。文章最后重点介绍了HOTAIR在BC管理、治疗和预后中的作用,强调了其潜在的治疗应用。
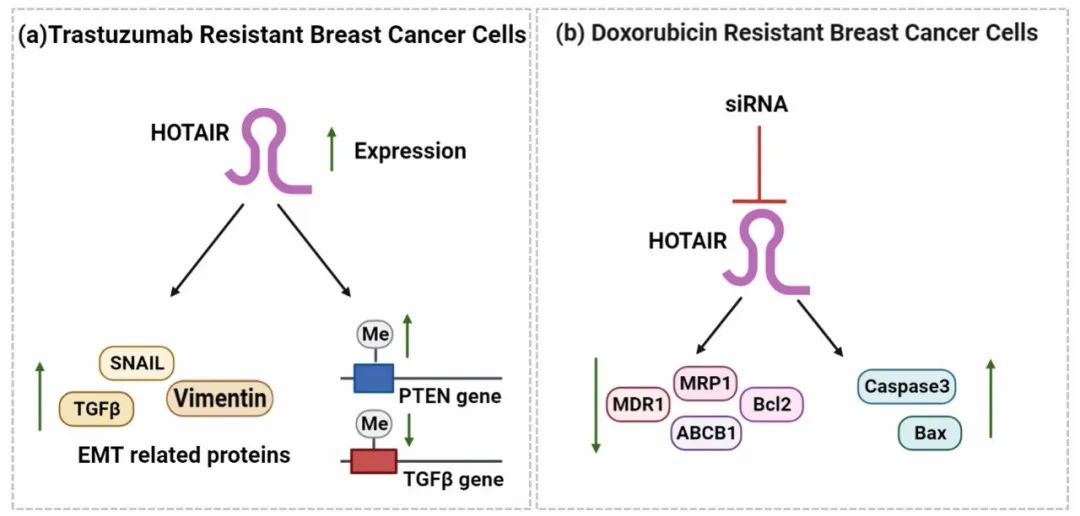
Fig1. HOTAIR在曲妥珠单抗耐药BC细胞中过表达,并上调EMT相关蛋白SNAIL、TGFß和vimentin的表达
原文链接:
https://pubmed.ncbi.nlm.nih.gov/36997931/
02
长链非编码RNA HITT与RGS2协调抑制T细胞免疫中的PD-L1翻译
发表期刊:J Clin Invest
影响因子:19.456
发表时间:2023年4月4日
程序性死亡配体1(PD-L1)是一种在人类癌症中经常表达的免疫检查点蛋白,通过与活化T细胞上的PD-1结合来促进免疫逃避。揭示PD-L1表达的机制对于理解免疫抑制微环境的影响至关重要,对于重新增强抗肿瘤免疫力也至关重要。然而,PD-L1是如何被调节的,特别是在翻译水平上,在很大程度上仍然未知。本研究发现一个lncRNA HITT(HIF-1α inhibitor at translation level)在干扰素γ刺激下被E2F1反式激活。其与RGS2(Regulator of G Protein Signalling 2)结合并协调与PD-L1的5'非翻译区(UTR)结合,导致PD-L1翻译减少。HITT表达在体外和体内均以PD-L1依赖性方式增强T细胞介导的细胞毒性。在乳腺癌组织中也检测到HITT/PD-L1、RGS2/PD-L1表达之间的临床相关性。总之,这些发现证明了HITT在抗肿瘤T细胞免疫中的作用,突出了HITT的激活作为一种增强癌症免疫治疗的潜在治疗策略。

Fig2. RGS2/HITT/PD-L1调节癌细胞和T细胞之间相互作用从而调节肿瘤免疫的示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37014700/
03
APOE介导的lncRNA MEG3抑制可保护人类心血管细胞免受慢性炎症
发表期刊:Protein & Cell
影响因子:15.328
发表时间:2023年4月3日
心血管疾病(CVD)是全世界死亡的主要原因。因此,诊断和治疗CVD仍然是临床医生的前沿,而在临床前模型中确定可靶向的疾病机制是研究人员和药物开发人员的重点领域。多态性蛋白载脂蛋白E(APOE)是脂质转运和代谢的核心,其亚型作为人类心血管疾病和神经退行性疾病的重要预测因子的作用已得到广泛认可。血浆APOE主要由肝细胞产生,约占全身APOE产生量的75%,在单核细胞/巨噬细胞、脂肪细胞、中胚层细胞和中枢神经系统中发挥重要作用。然而,尽管APOE在不同的哺乳动物细胞中广泛表达,但对其功能作用的研究主要集中在其细胞外分泌形式上,因此对于APOE在与人类心血管疾病密切相关的细胞类型中,特别是其他细胞间形式的具体作用仍知之甚少。本研究基于对人类干细胞衍生模型进行体外实验的研究,提出了APOE在保护多种人类心血管细胞免受细胞凋亡和慢性炎症方面的关键作用。机制上,本研究数据支持APOE作为人类心血管细胞保护因子发挥作用,至少部分是通过转录抑制MEG3来实现的,其激活与CVD样表型相关。本研究对人类心血管细胞中APOE的一种新型保护机制的表征,为CVD的机制提供了新的见解,并可能有助于为心血管疾病干预策略的发展提供信息。细胞外分泌型APOE、细胞质型APOE和核型APOE哪一种形式更具体地参与MEG3的调控和心血管细胞的保护,还需要进一步的研究。

Fig3. APOE缺乏诱导的MEG3异常表达对心血管细胞有不良影响
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37010884/
04
AC092894.1下调通过USP3/AR/RASGRP3轴促进结直肠癌奥沙利铂耐药
发表期刊:BMC Med
影响因子:11.150
发表时间:2023年4月3日
背景:奥沙利铂耐药是一个复杂的过程,一直是结直肠癌治疗过程中最不利的因素之一。最近,长链非编码RNAs(lncRNAs)已成为治疗化学耐药性的新型分子,但对其介导的特定分子机制知之甚少。
结果:AC092894.1表达已被证明在整个奥沙利铂诱导的耐药CRC细胞中急剧下调。体内和体外实验表明,AC092894.1具有逆转化学耐药性的功能。机制研究表明,AC092894.1作为支架分子,通过USP3介导AR的去泛素化,从而增加RASGRP3的转录。最后,MAPK信号通路的持续激活诱导了CRC细胞的凋亡。
结论:本研究确定了AC092894.1为CRC化学耐药的抑制因子,并揭示了靶向AC092894.1/USP3/AR/RASGRP3信号轴是治疗奥沙利铂耐药的一种新选择。

Fig4. AC092894.1调节CRC中奥沙利铂耐药的模型示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37013584/
05
CD56bright NK细胞中外泌体可转移的lncRNA EPB41L4A-AS1升高通过抑制细胞糖酵解导致神经母细胞瘤患者的NK功能受损
发表期刊:Clin Immunol
影响因子:10.190
发表时间:2023年4月4日
NK细胞是神经母细胞瘤(NB)监测和根除的关键免疫成分之一。葡萄糖代谢作为NK激活的主要燃料来源受到精细的调节。本研究数据显示,NB中的NK激活减少和CD56bright亚群不成比例地增加。进一步的研究表明,NB中的NK细胞在CD56bright NK亚群中表现出糖酵解停滞,并伴随着长链非编码RNA(lncRNA)EPB41L4A-AS1(已知的糖酵解调节的关键参与者)表达升高。此外,本研究重现了lncRNA EPB41L4A-AS1的抑制功能。有趣的是,本研究结果表明,外泌体lncRNA EPB41L4A-AS1可以从CD56bright NK转移到CD56dim NK,并且能够抑制靶NK的糖酵解。本研究数据表明,患者NK细胞中糖酵解的停滞与CD56bright NK亚群中lncRNA的升高有关,而不同NK亚群之间的交叉对话是通过外泌体传递代谢抑制lncRNA来实现的。

Fig5. CD56bright NK衍生外泌体lncRNA EPB41L4A-AS1抑制CD56dim NK细胞糖酵解和细胞毒性
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37024023/










