推荐产品
公司新闻/正文
Mol Pharm丨编码NPC1的mRNA治疗可挽救罕见病Niemann-Pick病C1型
人阅读 发布时间:2022-10-14 11:22
Niemann-Pick病C型(NP-C)是一种罕见的遗传性神经内脏疾病,由两个蛋白质编码基因 NPC1(95%的病例)或NPC2中的其中一个失活突变引起。NP-C1疾病的发病率约为1/90000活产儿,但由于临床表型的极端异质性,据估计,晚发型NP-C1的发病率要高得多,在1/19000至1/36000之间。NPC1和NPC2都是内溶酶体蛋白,在正常情况下,它们协同作用将从内吞脂蛋白中获得的未酯化胆固醇穿过晚期内吞体膜进入细胞质。NPC2是一种小的可溶性蛋白质,可与管腔中的未酯化胆固醇结合,并将其呈现给NPC1的N端结构域。NPC1(相比之下,NPC1是一种大型的多通道跨膜蛋白)随后促进胆固醇通过内吞体膜排出。
然而,在NP-C疾病中,运输缺陷导致全身细胞溶酶体中未酯化胆固醇和鞘糖脂的隔离和积累。这会导致各种器官的损伤,包括中枢神经系统(CNS)、肝脏、脾脏,有时甚至是肺。这些病理的临床表现通常出现在不同的时间点,并遵循非常不同的轨迹。相比之下,一些严重的婴儿型疾病会导致致命的肝或呼吸衰竭,而其他成人型则会导致迟发性神经退行性疾病。然而,大多数患者的典型神经系统表现包括垂直性核上性注视麻痹、小脑性共济失调、肌张力障碍、构音障碍、吞咽困难、痴笑性猝倒和癫痫发作。这些症状的严重程度往往会随着时间的推移而恶化,因为NP-C疾病是慢性的、进行性的并且总是致命的。
尽管做出了许多不同的努力,但很少有治疗NP-C疾病的方法。尽管各种化合物已被引入后期临床试验,包括热休克蛋白诱导剂arimoclomol(ClinicalTrials.gov标识符NCT02612129),但目前还没有一种药物得到FDA的批准。miglustat(一种葡糖神经酰胺合酶抑制剂,Clinical-Trials.gov标识符NCT01760564)和羟丙基-β-环糊精(一种环状寡糖,ClinicalTrials.gov标识符NCT04860960)已被证明可将未酯化的胆固醇从晚期核内体中隔离并转运至胞质溶胶,从而增加胆固醇的酯化。Miglustat目前已在欧盟、加拿大和日本获批用于治疗NP-C疾病的进行性神经系统并发症,而在美国经常被处方用于NP-C1疾病的适应症外。同时,自2009年以来,羟丙基-β-环糊精已获批准在全球范围内根据同情使用协议治疗数名NP-C疾病患者。然而,即使使用上述药物,患者的预后仍然很差,疾病负担仍然很高。
由于NP-C疾病是因为缺乏正常功能的NPC1或NPC2蛋白而发生的,因此人们一直在探索引入受影响蛋白的功能性拷贝的治疗方法。蛋白质替代疗法不适用于NP-C1疾病,因为它涉及跨膜蛋白,但已在NP-C2疾病的小鼠模型中证明了部分疗效。依赖于腺相关病毒载体血清型 9(AAV9)的病毒基因治疗策略在全身和局部给药时已在NP-C1疾病的小鼠模型中显示出了治疗前景。然而,AAV基因治疗也存在一些重要的缺陷,包括插入突变的风险、潜在的致命肝毒性和导致无法重新给药的强免疫原性。
基于信使RNA(mRNA)的药物是一类新兴的治疗药物,有可能在遗传性疾病的背景下恢复野生型蛋白质水平和功能,而不会出现与病毒DNA递送相关的遗传毒性问题。由于mRNA疗法涉及为细胞提供单链mRNA模板,并依靠核糖体机制在原位产生功能齐全的生物活性蛋白,因此它可以替代大型、复杂的蛋白质,如跨膜蛋白。临床前研究已经证明了基于mRNA的疗法对多种不同遗传疾病的疗效,包括囊性纤维化、α1-抗胰蛋白酶缺乏症、甲基丙二酸血症和B型血友病等。目前,科学家们正在进行临床试验以研究mRNA治疗propionic acid血症(ClinicalTrials.gov标识符NCT04159103)和囊性纤维化(ClinicalTrials.gov标识符NCT03375047)的疗效。
在结构上,体外转录(IVT)mRNA分子包含多个部分:5' cap、两侧为5'和3'非翻译区(UTR)的蛋白质编码序列和 3' poly(A)尾。这些部分都可以通过修饰来增强mRNA的细胞内稳定性、生物相容性和翻译能力。系统地研究工作揭示了优化5' cap、5' UTR、3' UTR和poly(A)尾长的策略。对于编码序列,密码子优化已被证明可以提高mRNA分子的可翻译性和结构稳定性。此外,化学碱基修饰已被证明可增强mRNA翻译,同时降低免疫激活。然而,不同的mRNA密码子优化方法,加上相互矛盾的报告表明,对于需要重复给药的应用,甚至可能不需要化学碱基修饰,这些都导致了关于哪种mRNA工程策略是最有效的持续争论。
为了研究不同密码子优化和碱基修饰策略的功效,以及探索外源性mRNA是否可用于替代患者成纤维细胞中的NPC1蛋白。近日,墨尔本大学的研究人员在Molecular Pharmaceutics期刊发表了题为mRNA Treatment Rescues Niemann-Pick Disease Type C1 in Patient Fibroblasts的研究论文。首次证明了工程化mRNA用于体外纠正NPC1疾病。该研究结果证实了mRNA作为一种可行的蛋白质替代选择的潜力,不仅适用于NPC1,还有助于进一步验证该技术在纠正与编码大型、复杂的细胞内蛋白质的基因功能缺失性突变相关的疾病方面的潜力。

本研究中,研究人员使用编码NPC1的mRNA来挽救培养的成纤维细胞(来自NP-C1患者)中由双等位基因NPC1突变引起的蛋白质不足和致病表型。首先,研究人员评估了产生能够在多种细胞类型中引发高蛋白表达的有效mRNA的工程策略。
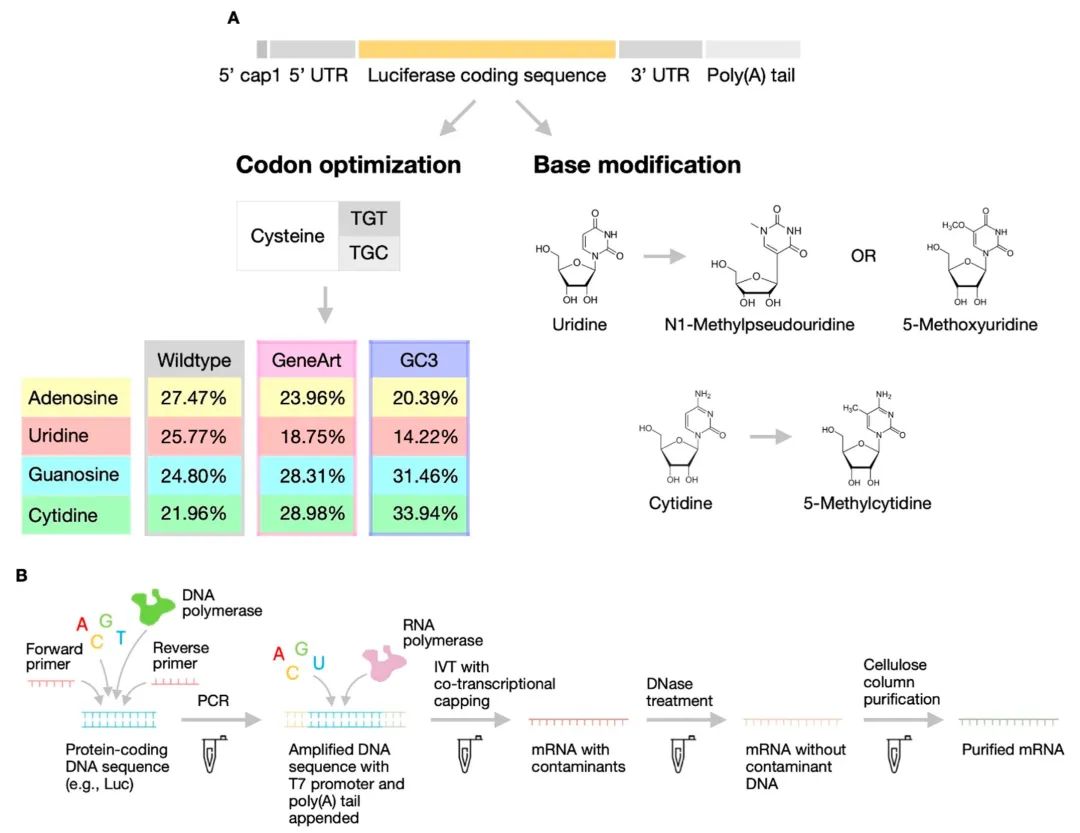
Fig1. mRNA工程化工作流程

新品上市!
* 锐博生物T7 mRNA转录试剂盒采用优化的帽结构类似物Ribo-Cap1,仅需一步共转录加帽即可完成mRNA的体外合成,加帽率可稳定在90%以上
* 与抗反帽ARCA相比,Ribo-cap1与GTP无竞争,不影响RNA的产率, 1μg模板投入量可产生70-150μg的mRNA
* 使用Ribo™ T7 mRNA转录试剂盒还可根据需求对单个或多个核苷酸单体进行替换,制备特殊化学修饰的mRNA
* 锐博生物可提供的修饰核苷包括N1-methylpseudo-UTP、5-Me-CTP、5-OMe-UTP、Pseudo-UTP等
结果发现,在荧光素酶报告试验中,“GC3”密码子优化与N1-methylpseudo-UTP碱基修饰相结合所产生的mRNA比野生型、未修饰的mRNA的效力高约1000倍,并且始终优于其他mRNA变体。研究数据表明,与这种设计策略相关表达的改善在很大程度上是由于设计的mRNA的二级结构增加。密码子优化和碱基修饰似乎都有助于增加二级结构。

Fig2. 不同碱基修饰的密码子优化的Luc mRNA的体外表达分析
随后,研究人员将这些原则应用于NPC1编码的mRNA工程中,结果观察到mRNA处理后NPC1蛋白水平的正常化,以及突变表型的拯救。具体来说,mRNA处理使患者细胞的胆固醇酯化能力恢复到野生型水平,并导致非酯化胆固醇水平(在胆固醇酯化试验中,与Lipofectamine处理的对照相比降低>57%)和溶酶体大小(与lipofectamine处理的对照组相比减少了157μm2)显著降低。

Fig3. mRNA治疗可挽救患者成纤维细胞中NPC1蛋白不足和疾病表型
总之,本研究结果阐明了设计能够在多种哺乳动物细胞类型中产生强烈蛋白质表达的mRNA的原则。并在NP-C1(一种罕见的单基因疾病)的背景下应用这些原则,结果发现用工程化的NPC1 mRNA治疗可以挽救患者成纤维细胞中的蛋白质不足和下游疾病表型。这些结果证实了mRNA作为一种可行的蛋白质替代选择的潜力,不仅适用于NPC1,而且可以更广泛地适用于涉及编码非常大、复杂的细胞内蛋白质的基因功能缺失性突变的疾病。

Fig4. 研究模型示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/36125338/










