广州市锐博生物科技有限公司品牌商
18 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
外泌体提取试剂
¥1800
推荐产品
公司新闻/正文
Mol Cancer丨circSTX6促进PDAC进展,可作为其潜在治疗靶点
607 人阅读发布时间:2022-06-07 10:13
胰腺癌是人类最恶性的肿瘤之一,5年生存率不到9%。由于局部进展和远处转移,大多数PDAC患者失去了接受根治性切除的机会。即使是能够接受根治性手术的部分患者,由于早期复发或远处转移,也只有37%的患者能存活5年。因此,有必要阐明PDAC的分子机制。
环状RNAs(circRNAs)是一类新型非编码RNA,由共价闭合的连续环产生,没有末端5'帽和3' polyA尾。由于环状结构对RNase R具有抗性,因此circRNA比其线性对应物表现出更高的稳定性。最近,circRNAs在多种癌症中的生物学功能已经得到了很好的研究,circRNAs的分子机制似乎与其亚细胞定位有关。细胞核中的circRNAs可参与基因转录的调控和RNA的可变剪接,而细胞质中的circRNAs则倾向于充当RNA海绵或与RNA结合蛋白(RBPs)相互作用,参与肿瘤相关基因的转录后调控。然而,circRNAs在PDAC中的潜在机制仍不明确,需要进一步研究。
2022年6月1日,Molecular Cancer期刊在线发表了一篇题为CircSTX6 promotes pancreatic ductal adenocarcinoma progression by sponging miR-449b-5p and interacting with CUL2的研究论文。报道了一种致癌circRNA circSTX6,其在PDAC组织中明显上调。揭示了circSTX6通过circSTX6/miR-449b-5p轴和circSTX6/CUL2/HIF1A信号通路调控MYH9的表达,从而促进PDAC细胞增殖和转移的作用机制。暗示circSTX6可以作为治疗PDAC的潜在治疗靶点。
首先,为了鉴定出对PDAC进展至关重要的circRNAs,研究人员通过RNA测序和qRT-PCR鉴定了一种致癌的circRNA circSTX6,并证实了其在PDAC组织中显著上调,且与预后相关。此外,circSTX6表达水平与肿瘤分化程度和N期相关。FISH和亚细胞分离实验显示circSTX6主要位于PDAC细胞的细胞质中。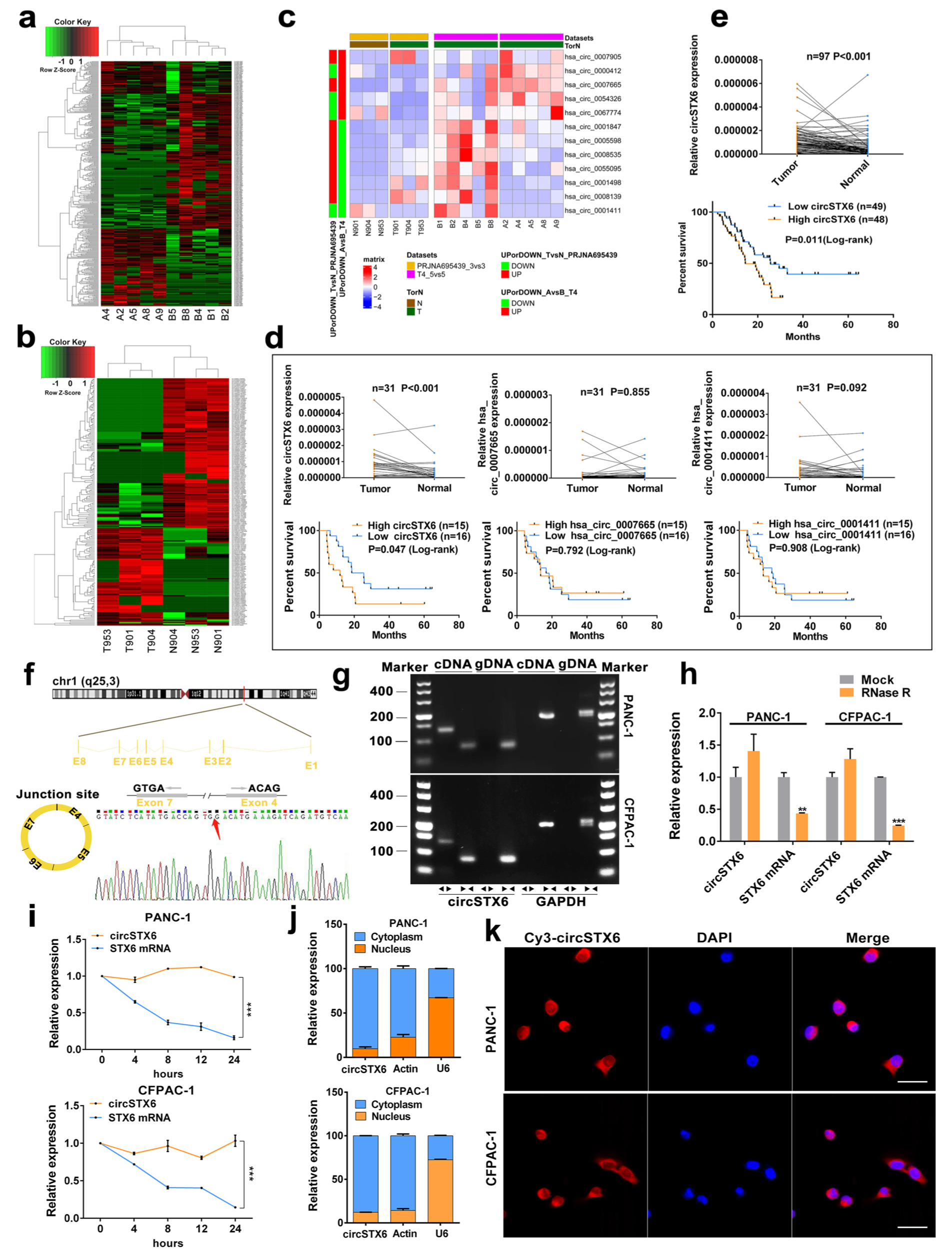
随后,研究人员为了评估circSTX6在PDAC中的生物学功能,在体内和体外进行功能获得性和功能缺失性实验,结果发现circSTX6过表达在体内和体外均能促进肿瘤的增殖和转移表型。这些发现说明了circSTX6在PDAC中的致癌作用。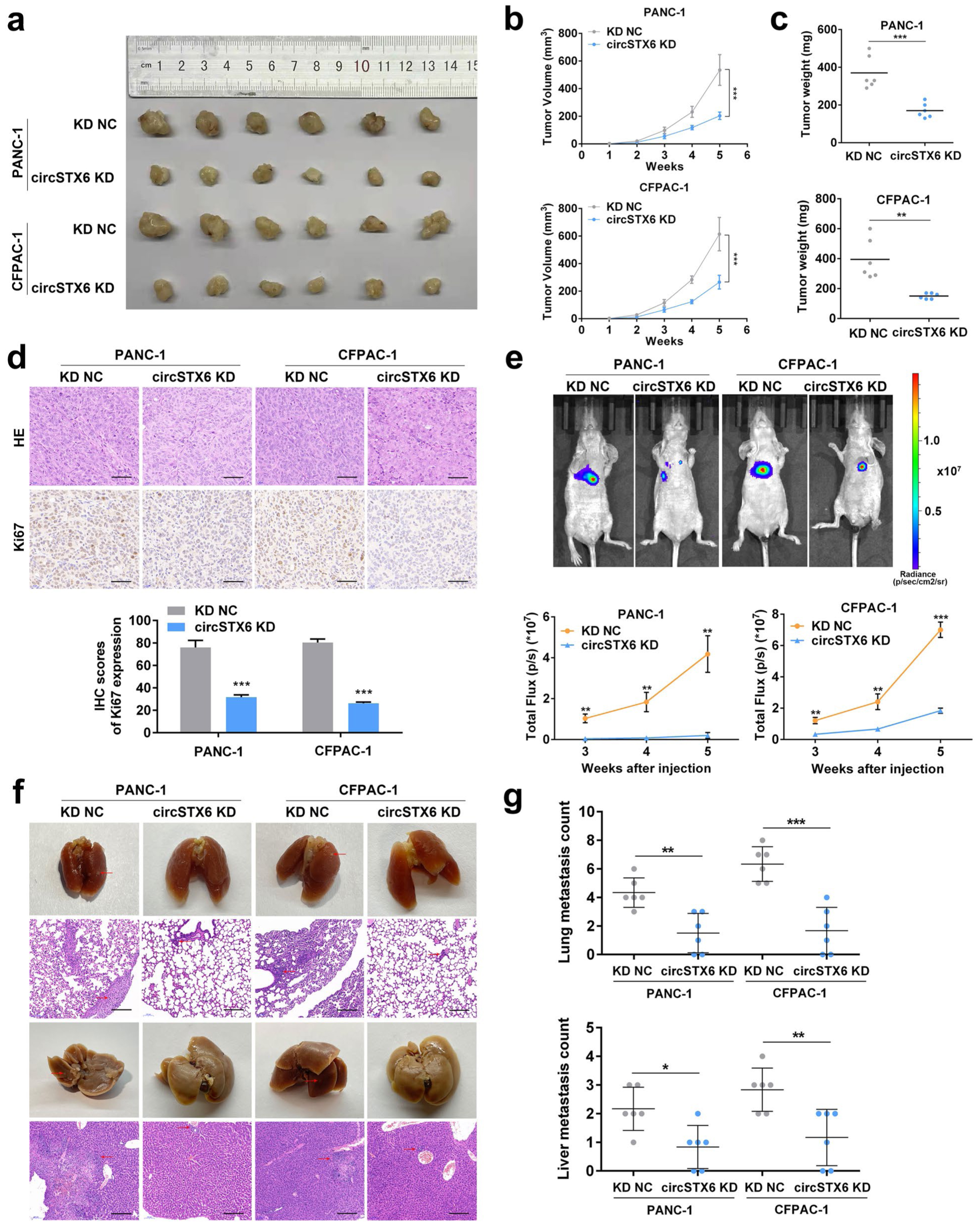
最后,为了探索circSTX6促进PDAC进展的分子机制,研究人员通过生物素偶联的circRNA捕获、FISH、荧光素酶报告基因实验发现circSTX6可以通过充当miR-449b-5p海绵以转录后调节MYH9的表达。此外,RNA pull-down、RIP和western blotting等实验进一步揭示了circSTX6通过与CUL2竞争性结合抑制HIF1A的VHL-EloBC-CUL2-Rbx1复合物依赖性泛素化降解,随后参与MYH9的转录调控。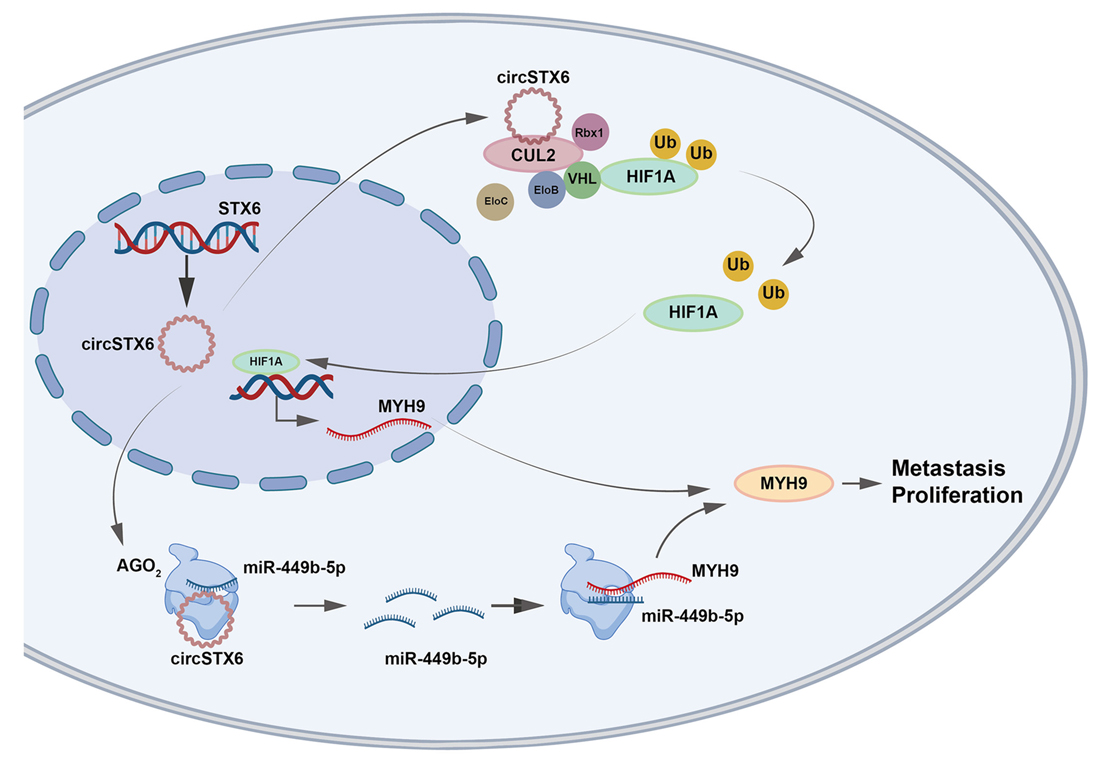
总的来说,本研究结果表明circSTX6/miR-449b-5p/MYH9和circSTX6/CUL2/HIF1A/MYH9轴在PDAC进展中起重要作用。circSTX6可以作为PDAC的潜在生物标志物和治疗靶点。
原文链接:
https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-022-01599-5
本研究RNA pull-down实验中涉及到的生物素标记的circRNA探针和EdU细胞增殖检测试剂盒由锐博生物提供!更多circRNA研究产品与服务信息,欢迎登陆锐博生物官网(www.ribobio.com)进行查询或来电咨询!
环状RNAs(circRNAs)是一类新型非编码RNA,由共价闭合的连续环产生,没有末端5'帽和3' polyA尾。由于环状结构对RNase R具有抗性,因此circRNA比其线性对应物表现出更高的稳定性。最近,circRNAs在多种癌症中的生物学功能已经得到了很好的研究,circRNAs的分子机制似乎与其亚细胞定位有关。细胞核中的circRNAs可参与基因转录的调控和RNA的可变剪接,而细胞质中的circRNAs则倾向于充当RNA海绵或与RNA结合蛋白(RBPs)相互作用,参与肿瘤相关基因的转录后调控。然而,circRNAs在PDAC中的潜在机制仍不明确,需要进一步研究。
2022年6月1日,Molecular Cancer期刊在线发表了一篇题为CircSTX6 promotes pancreatic ductal adenocarcinoma progression by sponging miR-449b-5p and interacting with CUL2的研究论文。报道了一种致癌circRNA circSTX6,其在PDAC组织中明显上调。揭示了circSTX6通过circSTX6/miR-449b-5p轴和circSTX6/CUL2/HIF1A信号通路调控MYH9的表达,从而促进PDAC细胞增殖和转移的作用机制。暗示circSTX6可以作为治疗PDAC的潜在治疗靶点。

首先,为了鉴定出对PDAC进展至关重要的circRNAs,研究人员通过RNA测序和qRT-PCR鉴定了一种致癌的circRNA circSTX6,并证实了其在PDAC组织中显著上调,且与预后相关。此外,circSTX6表达水平与肿瘤分化程度和N期相关。FISH和亚细胞分离实验显示circSTX6主要位于PDAC细胞的细胞质中。

Fig1. circSTX6在PDAC细胞和组织中的鉴定与表征
随后,研究人员为了评估circSTX6在PDAC中的生物学功能,在体内和体外进行功能获得性和功能缺失性实验,结果发现circSTX6过表达在体内和体外均能促进肿瘤的增殖和转移表型。这些发现说明了circSTX6在PDAC中的致癌作用。

Fig2. CircSTX6在体内促进PDAC细胞的肿瘤发生和转移
最后,为了探索circSTX6促进PDAC进展的分子机制,研究人员通过生物素偶联的circRNA捕获、FISH、荧光素酶报告基因实验发现circSTX6可以通过充当miR-449b-5p海绵以转录后调节MYH9的表达。此外,RNA pull-down、RIP和western blotting等实验进一步揭示了circSTX6通过与CUL2竞争性结合抑制HIF1A的VHL-EloBC-CUL2-Rbx1复合物依赖性泛素化降解,随后参与MYH9的转录调控。

Fig3. circSTX6促进PDAC增殖和转移的机制模型图
总的来说,本研究结果表明circSTX6/miR-449b-5p/MYH9和circSTX6/CUL2/HIF1A/MYH9轴在PDAC进展中起重要作用。circSTX6可以作为PDAC的潜在生物标志物和治疗靶点。
原文链接:
https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-022-01599-5
本研究RNA pull-down实验中涉及到的生物素标记的circRNA探针和EdU细胞增殖检测试剂盒由锐博生物提供!更多circRNA研究产品与服务信息,欢迎登陆锐博生物官网(www.ribobio.com)进行查询或来电咨询!