推荐产品
公司新闻/正文
miRNA新研究进展盘点(20220519)
人阅读 发布时间:2022-05-19 09:24
Hsa-miR-3178/RhoB/PI3K/Akt, a novel signaling pathway regulates ABC transporters to reverse gemcitabine resistance in pancreatic cancer
Hsa-miR-3178/RhoB/PI3K/Akt,一种新的信号通路调节ABC转运蛋白以逆转胰腺癌中吉西他滨耐药性
发表期刊:Mol Cancer
影响因子:27.401
发表时间:2022年5月10日
背景:尽管吉西他滨被认为是晚期胰腺癌(PC)的一线药物,但吉西他滨耐药性的发展严重限制了这种化疗的有效性,吉西他滨耐药的潜在机制仍不清楚。各种因素,如ATP结合盒 (ABC)转运蛋白、microRNAs及其下游信号通路,都包括在对吉西他滨的化学抗性中。本研究在体内和体外调查了microRNAs和ABC转运蛋白相关信号通路在PC对吉西他滨耐药中的潜在机制。
结果:本研究发现P-gp、BCRP和MRP1在吉西他滨耐药的PC组织和细胞中高表达。分子对接分析表显示,吉西他滨可以与ABC转运蛋白结合。与其亲本PANC-1细胞相比,Hsa-miR-3178在吉西他滨耐药PANC-1细胞中上调。此外,研究发现hsa-miR-3178促进了PC细胞对吉西他滨的耐药性。这些结果也得到了动物实验的验证。RhoB在吉西他滨耐药的PC细胞中被下调,是hsa-miR-3178的下游靶标。Kaplan-Meier生存曲线显示,较低的RhoB表达与PC患者较差的总生存期显著相关。挽救实验表明,RhoB可以逆转hsa-miR-3178介导的吉西他滨耐药性。有趣的是,hsa-miR-3178通过激活PI3K/Akt通路介导的ABC转运蛋白上调来促进PC中的吉西他滨耐药性。
结论:本研究结果表明,hsa-miR-3178通过RhoB/PI3K/Akt信号通路介导的ABC转运蛋白上调促进吉西他滨耐药。这些发现表明,hsa-miR-3178可能是克服PC中吉西他滨耐药性的新治疗靶点。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35538494/
Extracellular vesicles enclosed-miR-421 suppresses air pollution (PM2.5 )-induced cardiac dysfunction via ACE2 signalling
细胞外囊泡封装的miR-421通过ACE2信号抑制空气污染(PM 2.5)诱导的心功能障碍
发表期刊:J Extracell Vesicles
影响因子:25.841
发表时间:2022年5月9日
通过环境PM2.5造成的空气污染对公众健康构成了巨大威胁,因为它与心肺损伤的住院率、发病率和死亡率增加有关。然而,PM2.5引起的心血管疾病中肺损伤的潜在介质尚不完全清楚。为了探索在PM2.5暴露后肺和心脏之间的潜在交互作用,本研究分别进行了体内气管内滴注、离体器官培养和体外人支气管上皮细胞(Beas-2B)培养实验。收集暴露的Beas-2B上清液以治疗原代新生大鼠心肌细胞(NRCM)。经气管内滴注后,亚急性PM2.5暴露会导致心功能障碍,这是继发于小鼠肺损伤的时间依赖性心功能障碍,从而表明了肺和心脏之间的交互作用可能是通过小细胞外囊泡(sEV)来介导的。研究人员从PM2.5暴露的小鼠血清和Beas-2B上清液中分离出sEV,以分析sEV亚群响应PM2.5的变化。单粒子干涉反射成像传感分析(SP-IRIS)表明PM2.5增加了CD63/CD81/CD9阳性颗粒。结果表明,含有miR-421的呼吸系统来源的sEV会导致PM2.5暴露后的心脏功能障碍。AAV9-miR421-sponge抑制miR-421可显著逆转PM2.5诱导的小鼠心功能障碍。研究发现心脏血管紧张素转化酶2(ACE2)是sEV-miR421的下游靶标,可诱导心肌细胞凋亡和心功能障碍。此外,研究人员观察到GW4869(一种sEV释放抑制剂)或DIZE(一种ACE2的激活剂)治疗可以减轻体内PM2.5诱导的心功能障碍。总之,本研究结果表明,PM2.5暴露可促进肺损伤后与sEV相关的miR421释放,从而通过抑制ACE2导致PM2.5诱导的心功能障碍。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35536587/
Targeted Suppression of miRNA-33 Using pHLIP Improves Atherosclerosis Regression
使用pHLIP靶向抑制miRNA-33可改善动脉粥样硬化消退
发表期刊:Circ Res
影响因子:17.367
发表时间:2022年5月9日
背景:miRNA疗法在过去的十年中引起了人们的关注。这些寡核苷酸治疗可以调节体内miRNAs的表达,并可用于纠正肥胖、代谢综合征和动脉粥样硬化等人类疾病中发现的基因表达失衡。当前的anti-miRNA技术在体内的功效受到生理和细胞屏障的阻碍,无法递送到靶细胞中,而miRNA的性质允许靶向可能导致有害脱靶效应的整个途径。出于这些原因,抑制特定组织中miRNAs的新型靶向递送系统对于开发包括动脉粥样硬化在内的多种疾病的有效治疗策略至关重要。
结果:anti-miR-33共轭的pHLIP构建体优先递送至动脉粥样硬化斑块巨噬细胞。使用pHLIP指导的巨噬细胞靶向抑制miR-33通过增加胶原含量和减少血管病变内的脂质积累来改善动脉粥样硬化的消退。单细胞RNA测序分析揭示了pHLIP-anti-miR-33靶向的动脉粥样硬化病变巨噬细胞中纤维化基因(Col2a1、Col3a1、Col1a2、Fn1等)和金属蛋白酶组织抑制因子3(Timp3)的高表达以及Mmp12表达的下调。
结论:本研究通过药理学抑制巨噬细胞中的 miR-33 避免了对其他代谢组织的有害影响,为应用pHLIP治疗晚期动脉粥样硬化提供了原理证明。这可能通过选择性递送其他保护性miRNAs为动脉粥样硬化相关心血管疾病开辟新的治疗机会。
原文链接:https://pubmed.ncbi.nlm.nih.gov/35534923/
sRNAbench and sRNAtoolbox 2022 update: accurate miRNA and sncRNA profiling for model and non-model organisms
sRNAbench和sRNAtoolbox 2022更新:模式和非模式生物的精确miRNA和sncRNA分析
发表期刊:Nucleic Acids Res
影响因子:16.971
发表时间:2022年5月12日
NCBI Sequence Read Archive目前拥有超过800个不同物种的microRNA测序数据,证明了在小RNA研究领域存在广泛的分类分布。同时,每个miRNA-seq研究的样本数量不断增加,导致大量的数据需要准确、快速和方便使用的分析方法。自2019年sRNAtoolbox发布以来,已经提交了55000个sRNAbench研究,这推动了其可用性和基础注释数据库范围的许多改进。通过此次更新,用户可以上传无限数量的样本或从Google Drive、Dropbox或URLs导入它们。现在可以分别使用高可信度的后生动物和植物特异性数据库MirGeneDB和PmiREN,以及来自441个Ensembl物种的基因组组装和文库来进行MicroRNA和小RNA分析。新的结果页面包括简单的样本注释,以允许使用sRNAde进行下游差异表达分析。还可以通过一种新工具来探索未指定功能的reads,该工具可以映射到微生物参考,这可以揭示污染事件或我们在示例中描述的具有生物学意义的发现。sRNAtoolbox可在https://arn.ugr.es/srnatoolbox/使用。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35556129/
A translatable RNAi-driven gene therapy silences PMP22/Pmp22 genes and improves neuropathy in CMT1A mice
一种可翻译的RNAi驱动的基因疗法使PMP22/Pmp22基因沉默并改善CMT1A小鼠的神经病变
发表期刊:J Clin Invest
影响因子:14.808
发表时间:2022年5月17日
腓骨肌萎缩症1A型(CMT1A)是最常见的遗传性脱髓鞘周围神经病变,由PMP22基因复制引起。野生型PMP22在Schwann细胞中的过度表达使髓鞘不稳定,导致脱髓鞘并最终导致继发性轴突损失和残疾。目前还没有治疗方法可以改变这种疾病的进程。CMT1A治疗的最直接途径是将PMP22降低到正常水平。为了实现这一目标,本研究开发了一种基因治疗策略,使用靶向人和小鼠PMP22/Pmp22 mRNA的新型人工microRNAs来减少PMP22。主要的治疗性microRNA miR871被封装到AAV9载体中,并通过腰椎鞘内注射递送到C61-het小鼠(CMT1A模型)中。AAV9-miR871能有效地转导C61-het周围神经中的Schwann细胞,并降低人和小鼠PMP22/Pmp22 mRNA和蛋白质水平。疾病早期和晚期的治疗显著改善了多种功能预后和神经传导速度。此外,腰椎根和股运动神经的髓鞘病变得到改善。接受治疗的小鼠还表现出CMT1A循环生物标志物的减少。总之,本研究数据表明AAV9-miR871驱动的PMP22沉默挽救了CMT1A模型,并为使用可翻译基因治疗方法治疗CMT1A提供了原理证据。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35579942/
Hsa-miR-3178/RhoB/PI3K/Akt,一种新的信号通路调节ABC转运蛋白以逆转胰腺癌中吉西他滨耐药性
发表期刊:Mol Cancer
影响因子:27.401
发表时间:2022年5月10日
背景:尽管吉西他滨被认为是晚期胰腺癌(PC)的一线药物,但吉西他滨耐药性的发展严重限制了这种化疗的有效性,吉西他滨耐药的潜在机制仍不清楚。各种因素,如ATP结合盒 (ABC)转运蛋白、microRNAs及其下游信号通路,都包括在对吉西他滨的化学抗性中。本研究在体内和体外调查了microRNAs和ABC转运蛋白相关信号通路在PC对吉西他滨耐药中的潜在机制。
结果:本研究发现P-gp、BCRP和MRP1在吉西他滨耐药的PC组织和细胞中高表达。分子对接分析表显示,吉西他滨可以与ABC转运蛋白结合。与其亲本PANC-1细胞相比,Hsa-miR-3178在吉西他滨耐药PANC-1细胞中上调。此外,研究发现hsa-miR-3178促进了PC细胞对吉西他滨的耐药性。这些结果也得到了动物实验的验证。RhoB在吉西他滨耐药的PC细胞中被下调,是hsa-miR-3178的下游靶标。Kaplan-Meier生存曲线显示,较低的RhoB表达与PC患者较差的总生存期显著相关。挽救实验表明,RhoB可以逆转hsa-miR-3178介导的吉西他滨耐药性。有趣的是,hsa-miR-3178通过激活PI3K/Akt通路介导的ABC转运蛋白上调来促进PC中的吉西他滨耐药性。
结论:本研究结果表明,hsa-miR-3178通过RhoB/PI3K/Akt信号通路介导的ABC转运蛋白上调促进吉西他滨耐药。这些发现表明,hsa-miR-3178可能是克服PC中吉西他滨耐药性的新治疗靶点。

Fig1. hsa-miR-3178/RhoB轴通过PI3K/Akt通路介导的PC细胞中ABC转运蛋白过表达来介导肿瘤生长和吉西他滨耐药的潜在机制示意图
原文链接:https://pubmed.ncbi.nlm.nih.gov/35538494/
Extracellular vesicles enclosed-miR-421 suppresses air pollution (PM2.5 )-induced cardiac dysfunction via ACE2 signalling
细胞外囊泡封装的miR-421通过ACE2信号抑制空气污染(PM 2.5)诱导的心功能障碍
发表期刊:J Extracell Vesicles
影响因子:25.841
发表时间:2022年5月9日
通过环境PM2.5造成的空气污染对公众健康构成了巨大威胁,因为它与心肺损伤的住院率、发病率和死亡率增加有关。然而,PM2.5引起的心血管疾病中肺损伤的潜在介质尚不完全清楚。为了探索在PM2.5暴露后肺和心脏之间的潜在交互作用,本研究分别进行了体内气管内滴注、离体器官培养和体外人支气管上皮细胞(Beas-2B)培养实验。收集暴露的Beas-2B上清液以治疗原代新生大鼠心肌细胞(NRCM)。经气管内滴注后,亚急性PM2.5暴露会导致心功能障碍,这是继发于小鼠肺损伤的时间依赖性心功能障碍,从而表明了肺和心脏之间的交互作用可能是通过小细胞外囊泡(sEV)来介导的。研究人员从PM2.5暴露的小鼠血清和Beas-2B上清液中分离出sEV,以分析sEV亚群响应PM2.5的变化。单粒子干涉反射成像传感分析(SP-IRIS)表明PM2.5增加了CD63/CD81/CD9阳性颗粒。结果表明,含有miR-421的呼吸系统来源的sEV会导致PM2.5暴露后的心脏功能障碍。AAV9-miR421-sponge抑制miR-421可显著逆转PM2.5诱导的小鼠心功能障碍。研究发现心脏血管紧张素转化酶2(ACE2)是sEV-miR421的下游靶标,可诱导心肌细胞凋亡和心功能障碍。此外,研究人员观察到GW4869(一种sEV释放抑制剂)或DIZE(一种ACE2的激活剂)治疗可以减轻体内PM2.5诱导的心功能障碍。总之,本研究结果表明,PM2.5暴露可促进肺损伤后与sEV相关的miR421释放,从而通过抑制ACE2导致PM2.5诱导的心功能障碍。

Fig2. 呼吸系统来源的sEV包裹miR-421介导PM2.5暴露后的心肌细胞凋亡
原文链接:https://pubmed.ncbi.nlm.nih.gov/35536587/
Targeted Suppression of miRNA-33 Using pHLIP Improves Atherosclerosis Regression
使用pHLIP靶向抑制miRNA-33可改善动脉粥样硬化消退
发表期刊:Circ Res
影响因子:17.367
发表时间:2022年5月9日
背景:miRNA疗法在过去的十年中引起了人们的关注。这些寡核苷酸治疗可以调节体内miRNAs的表达,并可用于纠正肥胖、代谢综合征和动脉粥样硬化等人类疾病中发现的基因表达失衡。当前的anti-miRNA技术在体内的功效受到生理和细胞屏障的阻碍,无法递送到靶细胞中,而miRNA的性质允许靶向可能导致有害脱靶效应的整个途径。出于这些原因,抑制特定组织中miRNAs的新型靶向递送系统对于开发包括动脉粥样硬化在内的多种疾病的有效治疗策略至关重要。
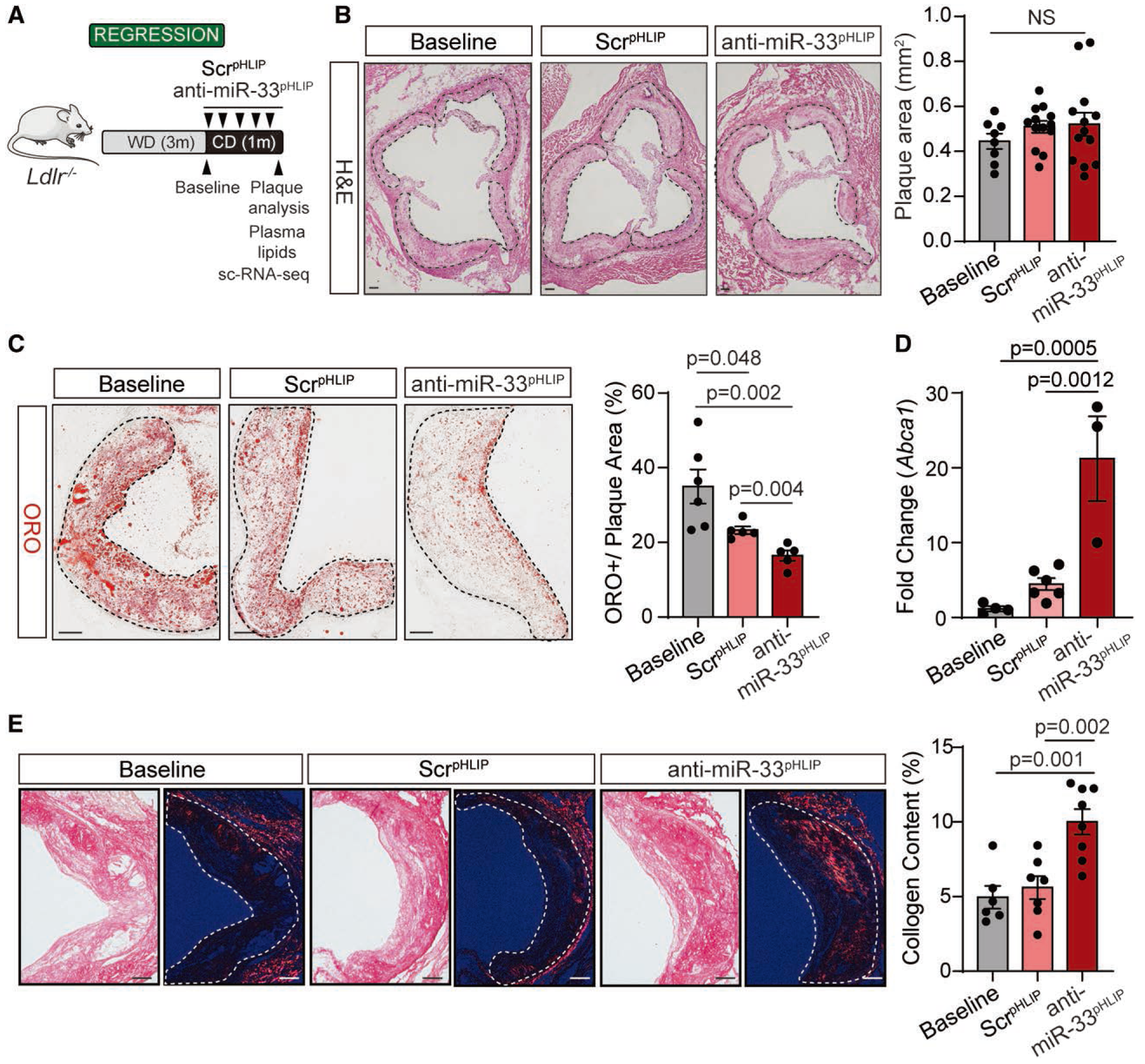
结果:anti-miR-33共轭的pHLIP构建体优先递送至动脉粥样硬化斑块巨噬细胞。使用pHLIP指导的巨噬细胞靶向抑制miR-33通过增加胶原含量和减少血管病变内的脂质积累来改善动脉粥样硬化的消退。单细胞RNA测序分析揭示了pHLIP-anti-miR-33靶向的动脉粥样硬化病变巨噬细胞中纤维化基因(Col2a1、Col3a1、Col1a2、Fn1等)和金属蛋白酶组织抑制因子3(Timp3)的高表达以及Mmp12表达的下调。
结论:本研究通过药理学抑制巨噬细胞中的 miR-33 避免了对其他代谢组织的有害影响,为应用pHLIP治疗晚期动脉粥样硬化提供了原理证明。这可能通过选择性递送其他保护性miRNAs为动脉粥样硬化相关心血管疾病开辟新的治疗机会。

Fig3. 使用pHLIP靶向沉默miR-33可改善动脉粥样硬化的消退
原文链接:https://pubmed.ncbi.nlm.nih.gov/35534923/
sRNAbench and sRNAtoolbox 2022 update: accurate miRNA and sncRNA profiling for model and non-model organisms
sRNAbench和sRNAtoolbox 2022更新:模式和非模式生物的精确miRNA和sncRNA分析
发表期刊:Nucleic Acids Res
影响因子:16.971
发表时间:2022年5月12日
NCBI Sequence Read Archive目前拥有超过800个不同物种的microRNA测序数据,证明了在小RNA研究领域存在广泛的分类分布。同时,每个miRNA-seq研究的样本数量不断增加,导致大量的数据需要准确、快速和方便使用的分析方法。自2019年sRNAtoolbox发布以来,已经提交了55000个sRNAbench研究,这推动了其可用性和基础注释数据库范围的许多改进。通过此次更新,用户可以上传无限数量的样本或从Google Drive、Dropbox或URLs导入它们。现在可以分别使用高可信度的后生动物和植物特异性数据库MirGeneDB和PmiREN,以及来自441个Ensembl物种的基因组组装和文库来进行MicroRNA和小RNA分析。新的结果页面包括简单的样本注释,以允许使用sRNAde进行下游差异表达分析。还可以通过一种新工具来探索未指定功能的reads,该工具可以映射到微生物参考,这可以揭示污染事件或我们在示例中描述的具有生物学意义的发现。sRNAtoolbox可在https://arn.ugr.es/srnatoolbox/使用。

Fig4. sRNAtoolbox改进和当前核心功能概述
原文链接:https://pubmed.ncbi.nlm.nih.gov/35556129/
A translatable RNAi-driven gene therapy silences PMP22/Pmp22 genes and improves neuropathy in CMT1A mice
一种可翻译的RNAi驱动的基因疗法使PMP22/Pmp22基因沉默并改善CMT1A小鼠的神经病变
发表期刊:J Clin Invest
影响因子:14.808
发表时间:2022年5月17日
腓骨肌萎缩症1A型(CMT1A)是最常见的遗传性脱髓鞘周围神经病变,由PMP22基因复制引起。野生型PMP22在Schwann细胞中的过度表达使髓鞘不稳定,导致脱髓鞘并最终导致继发性轴突损失和残疾。目前还没有治疗方法可以改变这种疾病的进程。CMT1A治疗的最直接途径是将PMP22降低到正常水平。为了实现这一目标,本研究开发了一种基因治疗策略,使用靶向人和小鼠PMP22/Pmp22 mRNA的新型人工microRNAs来减少PMP22。主要的治疗性microRNA miR871被封装到AAV9载体中,并通过腰椎鞘内注射递送到C61-het小鼠(CMT1A模型)中。AAV9-miR871能有效地转导C61-het周围神经中的Schwann细胞,并降低人和小鼠PMP22/Pmp22 mRNA和蛋白质水平。疾病早期和晚期的治疗显著改善了多种功能预后和神经传导速度。此外,腰椎根和股运动神经的髓鞘病变得到改善。接受治疗的小鼠还表现出CMT1A循环生物标志物的减少。总之,本研究数据表明AAV9-miR871驱动的PMP22沉默挽救了CMT1A模型,并为使用可翻译基因治疗方法治疗CMT1A提供了原理证据。

Fig5. 在CMT1A小鼠晚期治疗后,有效沉默PMP22/Pmp22并改善运动功能和坐骨神经MNCV,而不是CMAP或血液生物标志物表型
原文链接:https://pubmed.ncbi.nlm.nih.gov/35579942/










