推荐产品
公司新闻/正文
J Hematol Oncol(IF17.388)丨新致癌tRF AS-tDR-007333通过两种不同机制促进NSCLC的恶性
人阅读 发布时间:2022-05-17 10:46
肺癌是最常见的癌症类型,非小细胞肺癌(NSCLC)占所有肺癌病例的85%。尽管近年来在诊断和治疗方法上取得了长足的进步,但NSCLC患者的5年总体生存率仍不能令人满意。虽然大量研究表明,多种癌基因和抑癌基因参与了NSCLC的发病机制,但NSCLC致癌的分子基础仍未完全阐明。因此,仍有必要探索NSCLC中未知的分子机制,以鉴定新的诊断和治疗靶点。
tRNA衍生片段(tRFs)是一类新型小非编码RNAs(sncRNAs),由成熟或前体转移RNAs(tRNAs)的特异性切割产生。根据其长度、切割位置以及与tRNAs匹配的序列,tRFs大致分为五种亚型:tRF-5、tRF-3、tRF-2、tRF-1和tRNA半分子(tRNA halves, tiRNA)。tRF-5是由D环的5'端切割产生的;tRF-3来源于TψC环的3'端,包含CCA修饰;tRF-2仅由反密码子茎和环tRNA组成;tRF-1从前体tRNA的3'末端开始产生,其特征是在3'末端携带poly-U残基;tiRNA是由成熟tRNA的反密码子环特异性切割产生的。tRFs最初被视为下一代测序(RNA-seq)数据集中发现的tRNA的非功能性降解产物。然而,与成熟tRNAs的特定结构域匹配的reads重复出现表明这些sncRNAs可能是有功能的。事实上,新的证据表明tRFs参与了各种分子过程,例如基因沉默、RNA加工、蛋白质生物合成和致癌转化。一些tRFs也与某些类型癌细胞的增殖、迁移和侵袭有关。然而,tRFs是否以及如何参与NSCLC的肿瘤发生在很大程度上仍然未知。
近日,Journal of Hematology & Oncology(IF17.388)期刊在线发表了一篇题为A novel tRNA-derived fragment AS-tDR-007333 promotes the malignancy of NSCLC via the HSPB1/MED29 and ELK4/MED29 axes的研究论文。报道了一种在NSCLC中上调的新型tRF AS-tDR-007333,且其上调与NSCLC的发展和进展有关。揭示了AS-tDR-007333通过双重HSPB1-和ELK4-MED29调节机制促进NSCLC肿瘤发生的分子机制,暗示AS-tDR-007333可能作为NSCLC的潜在治疗靶点。

首先,为了鉴定和表征NSCLC中差异表达的循环tRFs,研究人员比较了9对来自NSCLC患者术前和术后血浆样本之间的tRF表达谱。tRF和tiRNA测序显示tRF表达谱在术前和术后血浆样本之间存在显著差异。循环tRFs的长度范围为15~50个核苷酸(nt),其中53.97%和30.11%的tRFs分别在20~23nt和31~33nt之间。值得注意的是,术后血浆中大多数tRFs的表达水平显著低于术前血浆样品中的表达水平,表明血浆tRFs上调与NSCLC中肿瘤的存在有关。堆积图表明,通过切割成具有相同序列的片段,可以从不同的tRNAs产生一种类型的tRF或tiRNA。饼图分析显示,大多数血浆tRFs来源于tRNAs的5'端。同样,tiRNA系列更多地属于tiRNA-5。

基于测序数据和qRT-PCR分析,研究人员发现AS-tDR-007333是一种未被表征的新型tRF,其在NSCLC组织、血浆和细胞中显著上调,并可能在NSCLC的发病机制中发挥关键作用。临床上,AS-tDR-007333过表达可以将NSCLC患者与健康对照区分开来,并且与NSCLC患者的不良预后相关。

为了评估AS-tDR-007333在NSCLC中的生物学功能,研究人员在NSCLC细胞中进行了功能获得性和功能缺失性实验。结果发现,过表达AS-tDR-007333促进了NSCLC细胞的增殖和迁移,而敲低AS-tDR-007333则会产生相反的效果。
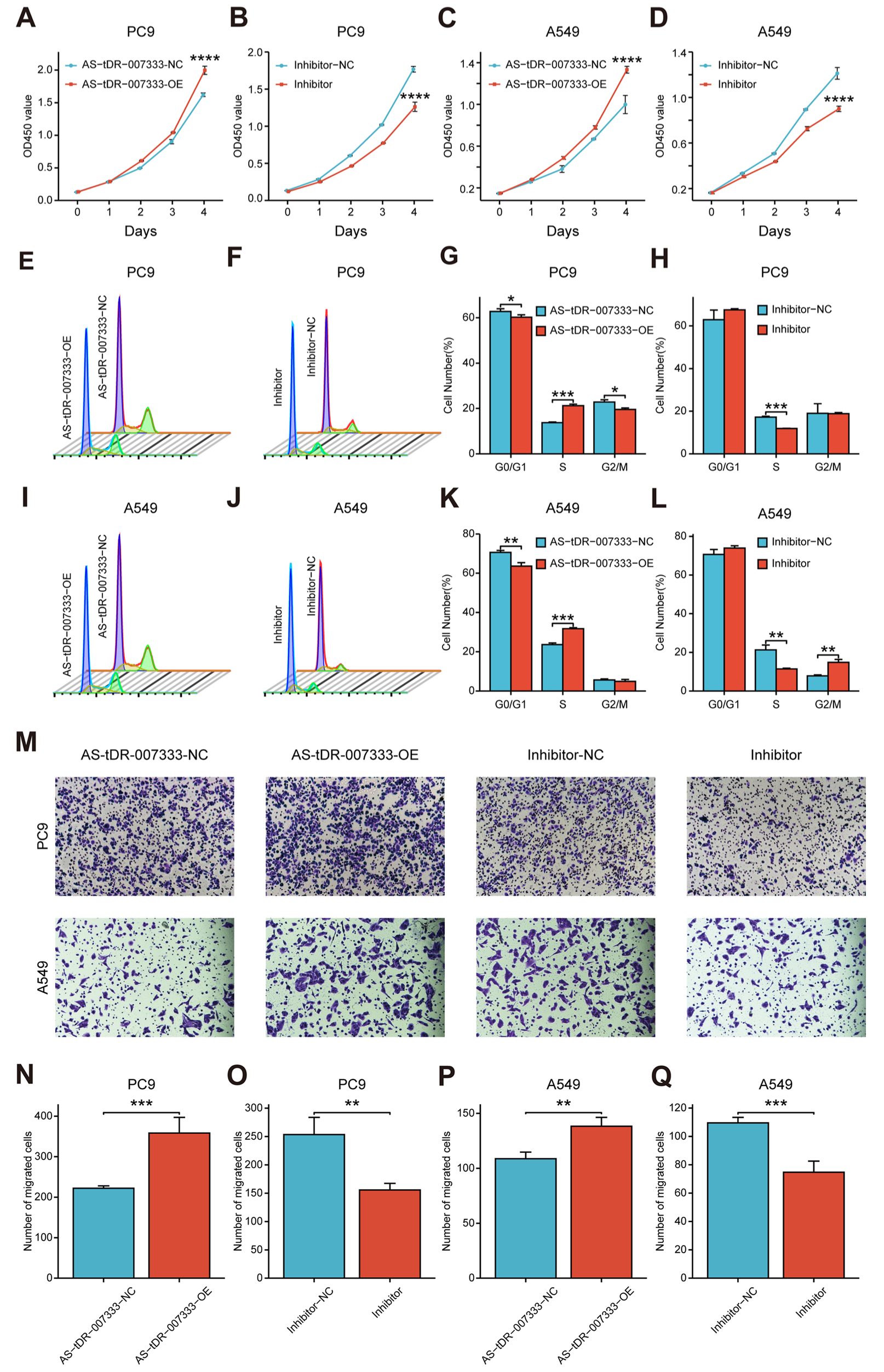

Fig4. AS-tDR-007333通过HSPB1-MED29和ELK4-MED29轴促进NSCLC肿瘤发生的作用机制

Fig5. 靶向AS-tDR-007333的抑制剂可减少体内NSCLC肿瘤的生长
tRNA衍生片段(tRFs)是一类新型小非编码RNAs(sncRNAs),由成熟或前体转移RNAs(tRNAs)的特异性切割产生。根据其长度、切割位置以及与tRNAs匹配的序列,tRFs大致分为五种亚型:tRF-5、tRF-3、tRF-2、tRF-1和tRNA半分子(tRNA halves, tiRNA)。tRF-5是由D环的5'端切割产生的;tRF-3来源于TψC环的3'端,包含CCA修饰;tRF-2仅由反密码子茎和环tRNA组成;tRF-1从前体tRNA的3'末端开始产生,其特征是在3'末端携带poly-U残基;tiRNA是由成熟tRNA的反密码子环特异性切割产生的。tRFs最初被视为下一代测序(RNA-seq)数据集中发现的tRNA的非功能性降解产物。然而,与成熟tRNAs的特定结构域匹配的reads重复出现表明这些sncRNAs可能是有功能的。事实上,新的证据表明tRFs参与了各种分子过程,例如基因沉默、RNA加工、蛋白质生物合成和致癌转化。一些tRFs也与某些类型癌细胞的增殖、迁移和侵袭有关。然而,tRFs是否以及如何参与NSCLC的肿瘤发生在很大程度上仍然未知。
近日,Journal of Hematology & Oncology(IF17.388)期刊在线发表了一篇题为A novel tRNA-derived fragment AS-tDR-007333 promotes the malignancy of NSCLC via the HSPB1/MED29 and ELK4/MED29 axes的研究论文。报道了一种在NSCLC中上调的新型tRF AS-tDR-007333,且其上调与NSCLC的发展和进展有关。揭示了AS-tDR-007333通过双重HSPB1-和ELK4-MED29调节机制促进NSCLC肿瘤发生的分子机制,暗示AS-tDR-007333可能作为NSCLC的潜在治疗靶点。

首先,为了鉴定和表征NSCLC中差异表达的循环tRFs,研究人员比较了9对来自NSCLC患者术前和术后血浆样本之间的tRF表达谱。tRF和tiRNA测序显示tRF表达谱在术前和术后血浆样本之间存在显著差异。循环tRFs的长度范围为15~50个核苷酸(nt),其中53.97%和30.11%的tRFs分别在20~23nt和31~33nt之间。值得注意的是,术后血浆中大多数tRFs的表达水平显著低于术前血浆样品中的表达水平,表明血浆tRFs上调与NSCLC中肿瘤的存在有关。堆积图表明,通过切割成具有相同序列的片段,可以从不同的tRNAs产生一种类型的tRF或tiRNA。饼图分析显示,大多数血浆tRFs来源于tRNAs的5'端。同样,tiRNA系列更多地属于tiRNA-5。

Fig1. NSCLC患者血浆tRFs表达谱特征
基于测序数据和qRT-PCR分析,研究人员发现AS-tDR-007333是一种未被表征的新型tRF,其在NSCLC组织、血浆和细胞中显著上调,并可能在NSCLC的发病机制中发挥关键作用。临床上,AS-tDR-007333过表达可以将NSCLC患者与健康对照区分开来,并且与NSCLC患者的不良预后相关。

Fig2. tRF AS-tDR-007333在NSCLC中上调,并与NSCLC患者的不良预后相关
为了评估AS-tDR-007333在NSCLC中的生物学功能,研究人员在NSCLC细胞中进行了功能获得性和功能缺失性实验。结果发现,过表达AS-tDR-007333促进了NSCLC细胞的增殖和迁移,而敲低AS-tDR-007333则会产生相反的效果。

Fig3. AS-tDR-007333促进NSCLC细胞的增殖和迁移能力
接下来,研究人员通过染色质免疫沉淀(ChIP)、荧光素酶报告基因、RNA pulldown、质谱分析、RNA免疫沉淀(RIP)、Western blot、免疫共沉淀(Co-IP)实验和挽救实验探索了tRF在NSCLC中的调节机制。结果表明,AS-tDR-007333通过两种不同的机制激活MED29,从而促进NSCLC细胞的恶性。首先,AS-tDR-007333与HSPB1结合并相互作用,通过增强MED29启动子中的H3K4me1和H3K27ac来激活MED29表达。其次,AS-tDR-007333刺激转录因子ELK4的表达,它与MED29启动子结合并增加其转录。

Fig4. AS-tDR-007333通过HSPB1-MED29和ELK4-MED29轴促进NSCLC肿瘤发生的作用机制
最后,鉴于AS-tDR-007333在NSCLC中充当致癌tRF,研究人员假设抑制AS-tDR-007333可能对NSCLC具有治疗作用。因此,为了评估AS-tDR-007333抑制剂在体内的治疗效果,研究人员合成了用于体内研究的AS-tDR-007333靶向抑制剂。结果显示,AS-tDR-007333抑制剂组的肿瘤体积显著更小,平均肿瘤重量显著更低。此外,AS-tDR-007333抑制剂组异种移植肿瘤组织中AS-tDR-007333、HSPB1、ELK4、MED29的表达水平被显著抑制,MED29和Ki-67蛋白的表达水平也被抑制。表明AS-tDR-007333抑制剂在体内可以通过抑制MED29的表达来抑制NSCLC肿瘤生长。

Fig5. 靶向AS-tDR-007333的抑制剂可减少体内NSCLC肿瘤的生长
总之,本研究将AS-tDR-007333鉴定为NSCLC中的新型致癌tRF。揭示了AS-tDR-007333通过激活HSPB1和ELK4介导的表观遗传和转录调控轴来靶向致癌MED29,从而促进NSCLC细胞恶性的作用机制。并在体外和体内证明了抑制AS-tDR-007333可抑制NSCLC细胞的增殖。本研究结果强调了tRF在NSCLC中的重要性,并表明AS-tDR-007333可以作为NSCLC的一种有前途的诊断/预后生物标志物和新的治疗靶点。
原文链接:
https://jhoonline.biomedcentral.com/articles/10.1186/s13045-022-01270-y
本研究中使用到的动物用tRF inhibitor由锐博生物提供!此外,我们还可提供tsRNA-seq测序服务、tRF细胞功能研究、作用机制研究产品,更多产品及服务信息请登录锐博生物官网(www.ribobio.com)查询或联系当地锐博销售人员!
https://jhoonline.biomedcentral.com/articles/10.1186/s13045-022-01270-y
本研究中使用到的动物用tRF inhibitor由锐博生物提供!此外,我们还可提供tsRNA-seq测序服务、tRF细胞功能研究、作用机制研究产品,更多产品及服务信息请登录锐博生物官网(www.ribobio.com)查询或联系当地锐博销售人员!










