推荐产品
公司新闻/正文
lncRNA新研究进展盘点(20220429)
人阅读 发布时间:2022-04-29 11:17
ATF3 -activated accelerating effect of LINC00941/lncIAPF on fibroblast-to-myofibroblast differentiation by blocking autophagy depending on ELAVL1/HuR in pulmonary fibrosis
ATF3激活通过阻断肺纤维化中依赖于ELAVL1/HuR的自噬促进了LINC00941/lncIAPF对成纤维细胞向肌成纤维细胞分化的作用
发表期刊:Autophagy
影响因子:16.016
发表时间:2022年4月15日
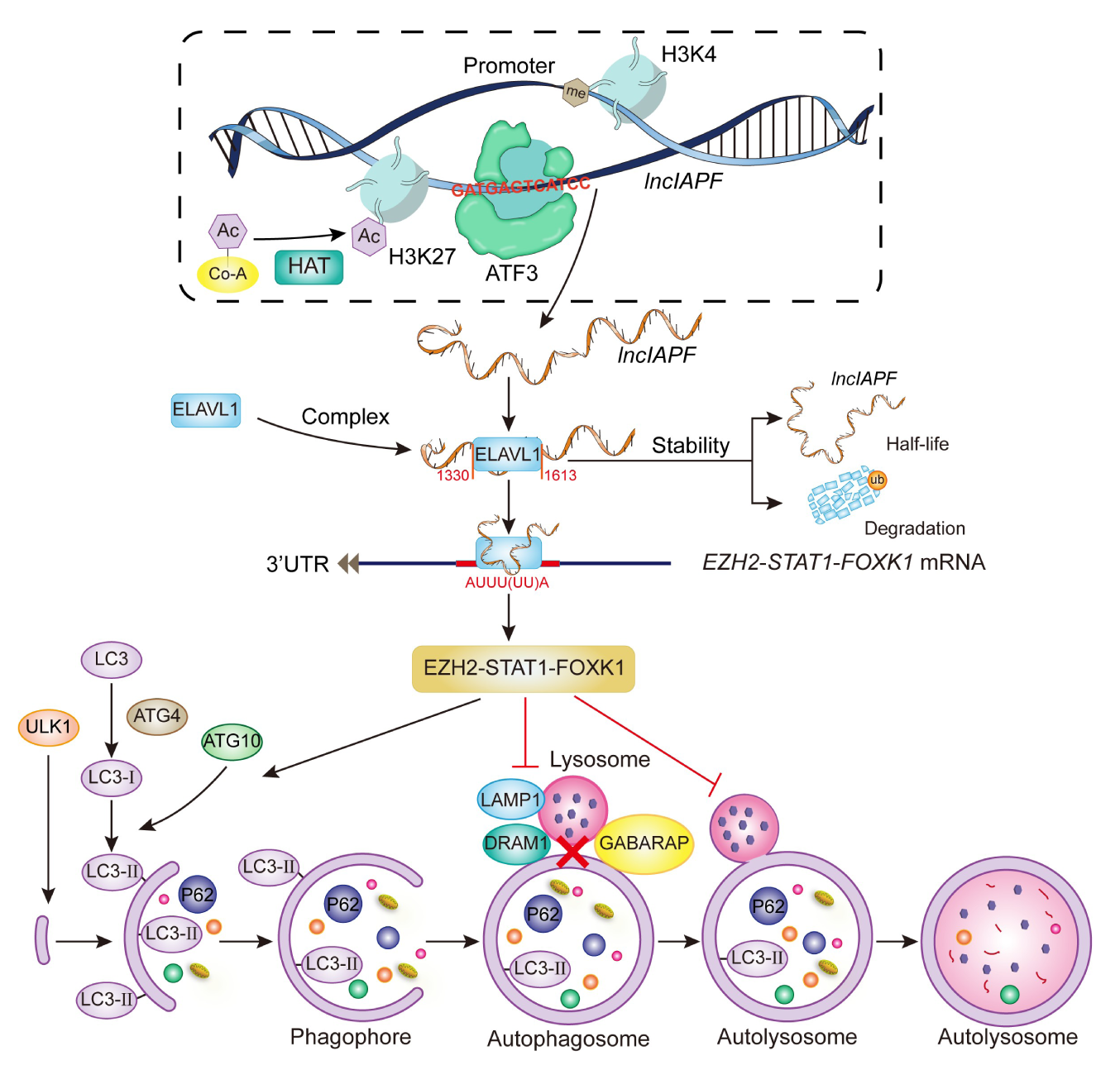
特发性肺纤维化(IPF)以肺部瘢痕为特征,目前尚无有效的治疗方法。成纤维细胞向肌成纤维细胞分化、肌成纤维细胞的增殖和迁移是这种疾病的主要临床表现;因此,阻止这些过程是一种实用的治疗策略。本研究发现高度上调的LINC00941/lncIAPF通过促进成纤维细胞向肌成纤维细胞的分化,以及肌成纤维细胞的增殖和迁移来加速肺纤维化。染色质转座酶可及性测序(ATAC-seq)和染色质免疫沉淀实验阐明了组蛋白3赖氨酸27乙酰化(H3K27ac)激活了LINC00941启动子上染色体区域的开放。结果,转录因子ATF3(激活转录因子3)结合到该区域,使LINC00941转录增强。RNA亲和分离、RNA免疫沉淀(RIP)、RNase-RIP、半衰期分析和泛素化实验揭示LINC00941与ELAVL1/HuR(ELAV样RNA结合蛋白1)形成RNA-蛋白复合物以发挥其促纤维化功能。双荧光mRFP-GFP-MAP1LC3/LC3(微管相关蛋白1轻链3)腺病毒监测技术、人自噬RT2分析仪PCR芯片和自噬通量显示LINC00941-ELAVL1轴抑制自噬体与溶酶体的融合。ELAVL1 RIP-seq、RIP-PCR、mRNA稳定性和挽救实验表明,LINC00941-ELAVL1复合物通过控制靶基因EZH2(zeste 2多梳抑制复合物2亚基增强子)、STAT1(信号转导和转录激活因子1)和FOXK1(叉头框K1)的稳定性来抑制自噬。最后,在小鼠模型和IPF患者中证实了LINC00941的治疗效果。本研究为IPF提供了一个与自噬相关的治疗靶点和新的有效治疗策略。
原文链接:https://pubmed.ncbi.nlm.nih.gov/35427207/
Long Noncoding RNAs That Function in Nutrition: Lnc-ing Nutritional Cues to Metabolic Pathways
在营养中起作用的长链非编码RNA:Lnc-ing对代谢途径的营养信号
发表期刊:Annu Rev Nutr
影响因子:11.848
发表时间:2022年4月18日
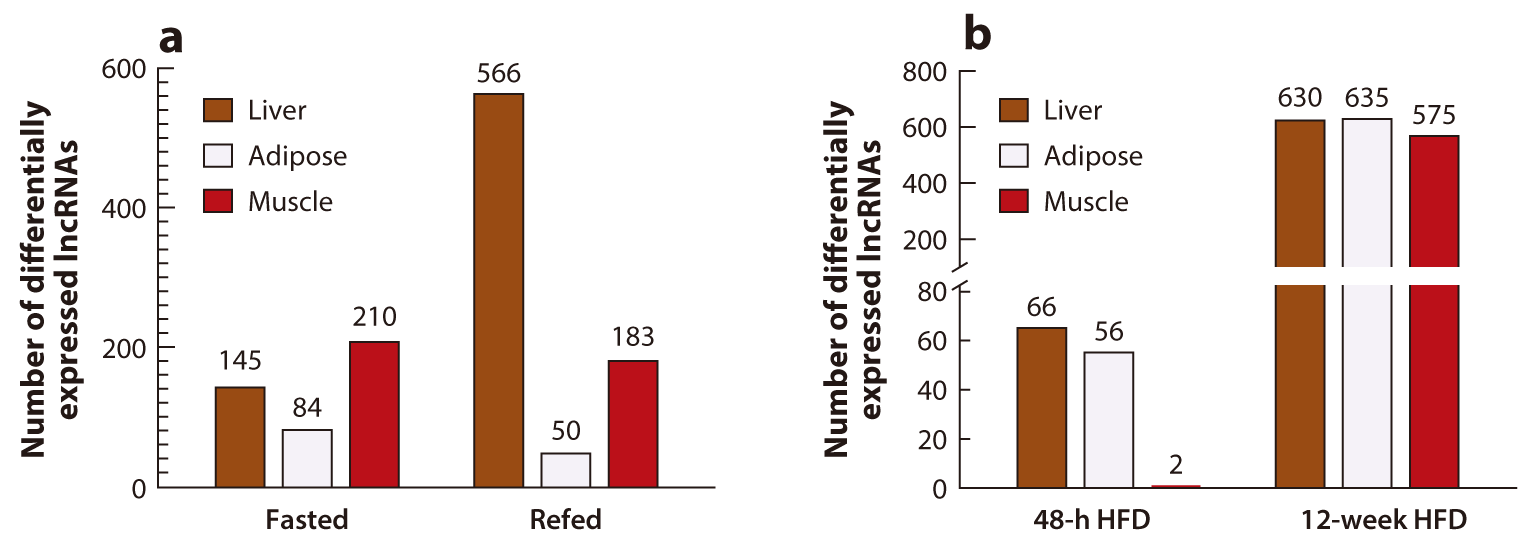
长链非编码RNAs(lncRNAs)对环境变化敏感,并在健康和疾病中发挥关键作用。新的证据表明,lncRNAs通过调节基因表达来形成代谢过程,以响应不断变化的营养信号。本文回顾了在关键代谢组织(肝脏、脂肪和肌肉)中对禁食、喂养和高脂饮食敏感的各种lncRNAs,重点介绍了触发lncRNAs自身表达变化的调节机制,以及这些lncRNAs如何在特定细胞类型或跨组织中调节关键代谢基因的表达。确定lncRNAs如何对营养变化做出反应,对于理解饮食变化后复杂的下游级联反应至关重要,并且可以决定我们治疗代谢疾病的方式。此外,研究可能影响lncRNA调节反应的性别偏见可能会揭示代谢疾病中所观察到的性别差异的贡献。
原文链接:https://pubmed.ncbi.nlm.nih.gov/35436418/
Role of lncSLCO1C1 in gastric cancer progression and resistance to oxaliplatin therapy
lncSLCO1C1在胃癌进展和对奥沙利铂治疗耐药中的作用
发表期刊:Clin Transl Med
影响因子:11.493
发表时间:2022年4月26日
背景:胃癌(GC)由于肿瘤转移和对治疗的耐药,是最致命的疾病之一。了解肿瘤进展和耐药的分子机制将有助于提高治疗效果,并开发新的干预策略。
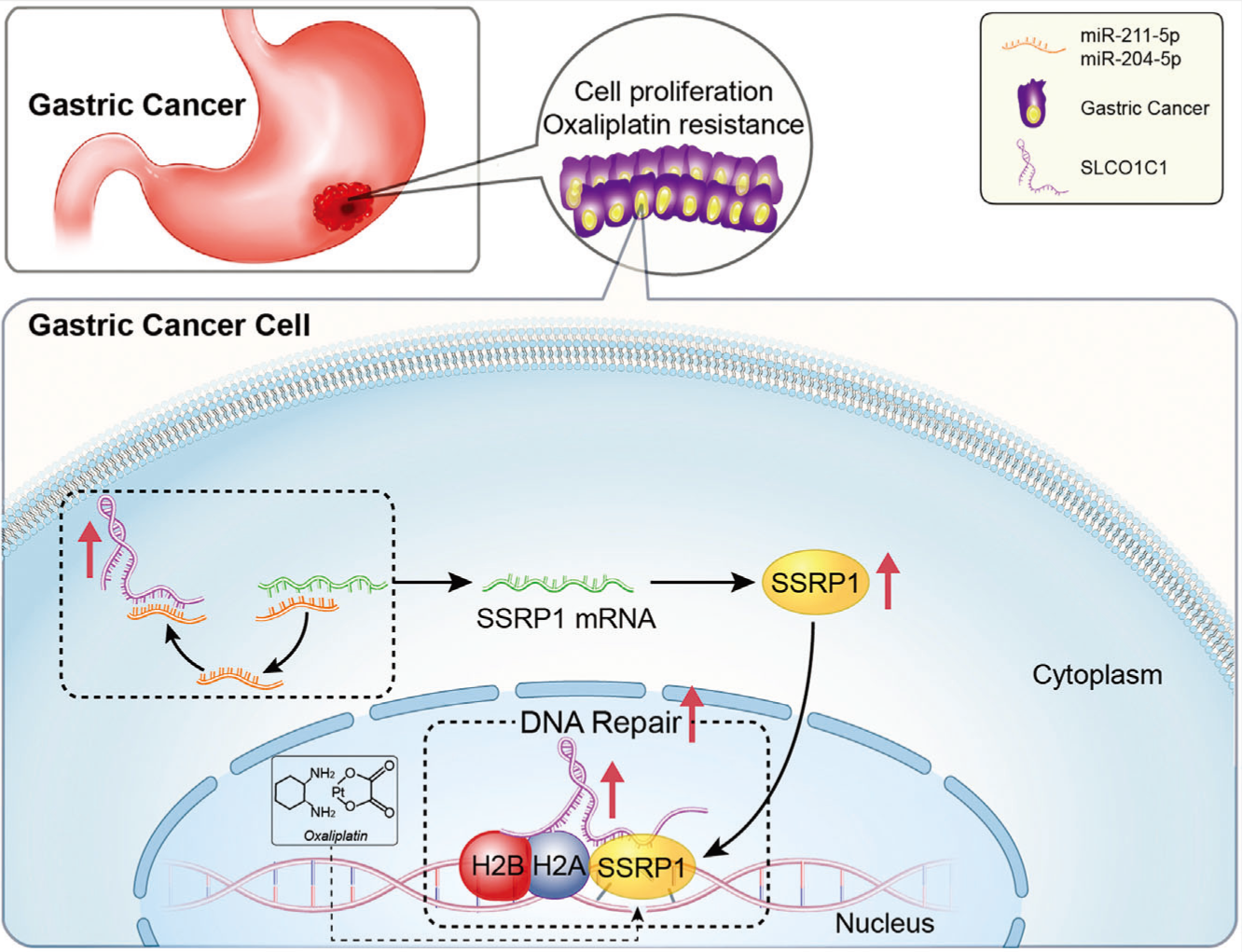
结果:LncSLCO1C1在GC组织样本中高度上调,并与GC患者较差的总生存期相关。lncSLCO1C1过表达促进了细胞增殖和迁移,而降低lncSLCO1C1表达则产生了相反的效果。lncSLCO1C1还通过减少DNA损伤和增加细胞增殖来介导肿瘤对奥沙利铂化疗的耐药性。尽管lncSLCO1C1和PDE3A之间存在序列重叠,但PDE3A表达的变化对GC细胞的进展无影响,这表明lncSLCO1C1而不是PDE3A与GC细胞的进展有关。机制上,lncSLCO1C1作为SSRP1(结构特异性识别蛋白1)/H2A/H2B复合物的支架,调节SSRP1在减少DNA损伤方面的功能。同时,lncSLCO1C1可作为分子海绵吸附靶向SSRP1 mRNA的miR-204-5p和miR-211-5p,从而增加SSRP1的表达。lncSLCO1C1和SSRP1均高表达的患者总生存期较差,突显了lncSLCO1C1在GC进展中的作用。
结论:LncSLCO1C1通过与SSRP1/H2A/H2b复合物相互作用并充当其支架,以及吸附miR-211-5p和miR-204-5p来增加SSRP1表达,从而促进细胞生长和防止DNA损伤,最终促进GC进展。
原文链接:https://pubmed.ncbi.nlm.nih.gov/35474446/
LncRNA-H19 in Fibroblasts Promotes Diabetic Wound Healing
LncRNA-H19在成纤维细胞中促进糖尿病伤口愈合
发表期刊:Diabetes
影响因子:9.461
发表时间:2022年4月26日
糖尿病患者皮肤伤口愈合受损,并会发展为不愈合性溃疡。然而,伤口愈合过程的分子机制在很大程度上仍不清楚。本研究发现皮肤PDGFRα+成纤维细胞表达的lncRNA-H19(lncH19)通过促进受损皮肤中的真皮成纤维细胞增殖和巨噬细胞浸润来加速伤口愈合过程。PDGFRα+细胞来源的lncH19在2型糖尿病患者和小鼠的伤口愈合皮肤组织中含量较低,其通过促进真皮成纤维细胞的增殖能力和巨噬细胞募集来促进伤口愈合。机制上,lncH19通过抑制p53活性和GDF15释放来缓解成纤维细胞的细胞周期停滞,并增加受损组织中的巨噬细胞浸润。此外,源自脂肪细胞祖细胞的外泌体通过将lncH19递送至受损组织,有效地恢复受损的糖尿病伤口愈合。因此,本研究揭示了lncRNA在调节皮肤组织修复中的新作用,并为开发糖尿病的临床治疗提供了新的有希望的见解。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35472819/
Functional elements of the cis-regulatory lincRNA-p21
顺式调控lincRNA-p21的功能元件
发表期刊:Cell Reports
影响因子:9.423
发表时间:2022年4月19日
p53诱导的长链非编码RNA(lncRNA)lincRNA-p21被认为以顺式作用促进邻近细胞周期基因Cdkn1a/p21的p53依赖性表达。转录的lincRNA-p21调控位点激活p21表达的分子机制仍然知之甚少。为了阐明顺式调节的功能元件,本研究生成了一系列破坏DNA调节元件、lincRNA-p21转录或成熟lincRNA-p21积累的遗传模型。出乎意料的是,研究人员确定了lincRNA-p21的全长转录、剪接和积累对于基因座的染色质组织和顺式调节是可有可无的。相反,本研究发现通过lincRNA-p21外显子1中的保守区域产生lincRNA-p21促进了顺式激活。这些发现表明,该lncRNA位点新生转录的激活(而不是成熟lncRNA转录本的产生或积累)是进行局部基因表达控制所必需的。

原文链接:https://www.sciencedirect.com/science/article/pii/S2211124722004454
ATF3激活通过阻断肺纤维化中依赖于ELAVL1/HuR的自噬促进了LINC00941/lncIAPF对成纤维细胞向肌成纤维细胞分化的作用
发表期刊:Autophagy
影响因子:16.016
发表时间:2022年4月15日
特发性肺纤维化(IPF)以肺部瘢痕为特征,目前尚无有效的治疗方法。成纤维细胞向肌成纤维细胞分化、肌成纤维细胞的增殖和迁移是这种疾病的主要临床表现;因此,阻止这些过程是一种实用的治疗策略。本研究发现高度上调的LINC00941/lncIAPF通过促进成纤维细胞向肌成纤维细胞的分化,以及肌成纤维细胞的增殖和迁移来加速肺纤维化。染色质转座酶可及性测序(ATAC-seq)和染色质免疫沉淀实验阐明了组蛋白3赖氨酸27乙酰化(H3K27ac)激活了LINC00941启动子上染色体区域的开放。结果,转录因子ATF3(激活转录因子3)结合到该区域,使LINC00941转录增强。RNA亲和分离、RNA免疫沉淀(RIP)、RNase-RIP、半衰期分析和泛素化实验揭示LINC00941与ELAVL1/HuR(ELAV样RNA结合蛋白1)形成RNA-蛋白复合物以发挥其促纤维化功能。双荧光mRFP-GFP-MAP1LC3/LC3(微管相关蛋白1轻链3)腺病毒监测技术、人自噬RT2分析仪PCR芯片和自噬通量显示LINC00941-ELAVL1轴抑制自噬体与溶酶体的融合。ELAVL1 RIP-seq、RIP-PCR、mRNA稳定性和挽救实验表明,LINC00941-ELAVL1复合物通过控制靶基因EZH2(zeste 2多梳抑制复合物2亚基增强子)、STAT1(信号转导和转录激活因子1)和FOXK1(叉头框K1)的稳定性来抑制自噬。最后,在小鼠模型和IPF患者中证实了LINC00941的治疗效果。本研究为IPF提供了一个与自噬相关的治疗靶点和新的有效治疗策略。

Fig1. lncIAPF作为促纤维化因子促进肺纤维化的机制
原文链接:https://pubmed.ncbi.nlm.nih.gov/35427207/
Long Noncoding RNAs That Function in Nutrition: Lnc-ing Nutritional Cues to Metabolic Pathways
在营养中起作用的长链非编码RNA:Lnc-ing对代谢途径的营养信号
发表期刊:Annu Rev Nutr
影响因子:11.848
发表时间:2022年4月18日
长链非编码RNAs(lncRNAs)对环境变化敏感,并在健康和疾病中发挥关键作用。新的证据表明,lncRNAs通过调节基因表达来形成代谢过程,以响应不断变化的营养信号。本文回顾了在关键代谢组织(肝脏、脂肪和肌肉)中对禁食、喂养和高脂饮食敏感的各种lncRNAs,重点介绍了触发lncRNAs自身表达变化的调节机制,以及这些lncRNAs如何在特定细胞类型或跨组织中调节关键代谢基因的表达。确定lncRNAs如何对营养变化做出反应,对于理解饮食变化后复杂的下游级联反应至关重要,并且可以决定我们治疗代谢疾病的方式。此外,研究可能影响lncRNA调节反应的性别偏见可能会揭示代谢疾病中所观察到的性别差异的贡献。

Fig2. 在禁食、再喂食和48h或12周的高脂饮食后,小鼠肝脏、脂肪和肌肉组织中lncRNA表达数量的变化
原文链接:https://pubmed.ncbi.nlm.nih.gov/35436418/
Role of lncSLCO1C1 in gastric cancer progression and resistance to oxaliplatin therapy
lncSLCO1C1在胃癌进展和对奥沙利铂治疗耐药中的作用
发表期刊:Clin Transl Med
影响因子:11.493
发表时间:2022年4月26日
背景:胃癌(GC)由于肿瘤转移和对治疗的耐药,是最致命的疾病之一。了解肿瘤进展和耐药的分子机制将有助于提高治疗效果,并开发新的干预策略。
结果:LncSLCO1C1在GC组织样本中高度上调,并与GC患者较差的总生存期相关。lncSLCO1C1过表达促进了细胞增殖和迁移,而降低lncSLCO1C1表达则产生了相反的效果。lncSLCO1C1还通过减少DNA损伤和增加细胞增殖来介导肿瘤对奥沙利铂化疗的耐药性。尽管lncSLCO1C1和PDE3A之间存在序列重叠,但PDE3A表达的变化对GC细胞的进展无影响,这表明lncSLCO1C1而不是PDE3A与GC细胞的进展有关。机制上,lncSLCO1C1作为SSRP1(结构特异性识别蛋白1)/H2A/H2B复合物的支架,调节SSRP1在减少DNA损伤方面的功能。同时,lncSLCO1C1可作为分子海绵吸附靶向SSRP1 mRNA的miR-204-5p和miR-211-5p,从而增加SSRP1的表达。lncSLCO1C1和SSRP1均高表达的患者总生存期较差,突显了lncSLCO1C1在GC进展中的作用。
结论:LncSLCO1C1通过与SSRP1/H2A/H2b复合物相互作用并充当其支架,以及吸附miR-211-5p和miR-204-5p来增加SSRP1表达,从而促进细胞生长和防止DNA损伤,最终促进GC进展。

Fig3. LncSLCO1C1促进肿瘤进展和对奥沙利铂治疗耐药的作用机制
原文链接:https://pubmed.ncbi.nlm.nih.gov/35474446/
LncRNA-H19 in Fibroblasts Promotes Diabetic Wound Healing
LncRNA-H19在成纤维细胞中促进糖尿病伤口愈合
发表期刊:Diabetes
影响因子:9.461
发表时间:2022年4月26日
糖尿病患者皮肤伤口愈合受损,并会发展为不愈合性溃疡。然而,伤口愈合过程的分子机制在很大程度上仍不清楚。本研究发现皮肤PDGFRα+成纤维细胞表达的lncRNA-H19(lncH19)通过促进受损皮肤中的真皮成纤维细胞增殖和巨噬细胞浸润来加速伤口愈合过程。PDGFRα+细胞来源的lncH19在2型糖尿病患者和小鼠的伤口愈合皮肤组织中含量较低,其通过促进真皮成纤维细胞的增殖能力和巨噬细胞募集来促进伤口愈合。机制上,lncH19通过抑制p53活性和GDF15释放来缓解成纤维细胞的细胞周期停滞,并增加受损组织中的巨噬细胞浸润。此外,源自脂肪细胞祖细胞的外泌体通过将lncH19递送至受损组织,有效地恢复受损的糖尿病伤口愈合。因此,本研究揭示了lncRNA在调节皮肤组织修复中的新作用,并为开发糖尿病的临床治疗提供了新的有希望的见解。

Fig4. LncRNA-H19在成纤维细胞中促进糖尿病伤口愈合的机制模型
原文链接:https://pubmed.ncbi.nlm.nih.gov/35472819/
Functional elements of the cis-regulatory lincRNA-p21
顺式调控lincRNA-p21的功能元件
发表期刊:Cell Reports
影响因子:9.423
发表时间:2022年4月19日
p53诱导的长链非编码RNA(lncRNA)lincRNA-p21被认为以顺式作用促进邻近细胞周期基因Cdkn1a/p21的p53依赖性表达。转录的lincRNA-p21调控位点激活p21表达的分子机制仍然知之甚少。为了阐明顺式调节的功能元件,本研究生成了一系列破坏DNA调节元件、lincRNA-p21转录或成熟lincRNA-p21积累的遗传模型。出乎意料的是,研究人员确定了lincRNA-p21的全长转录、剪接和积累对于基因座的染色质组织和顺式调节是可有可无的。相反,本研究发现通过lincRNA-p21外显子1中的保守区域产生lincRNA-p21促进了顺式激活。这些发现表明,该lncRNA位点新生转录的激活(而不是成熟lncRNA转录本的产生或积累)是进行局部基因表达控制所必需的。

Fig5. 顺式调控lincRNA-p21的功能元件
原文链接:https://www.sciencedirect.com/science/article/pii/S2211124722004454










