推荐产品
公司新闻/正文
Adv Sci丨LINC01431阻止HBV cccDNA转录的分子机制
人阅读 发布时间:2022-04-28 16:19
乙型肝炎病毒(HBV)感染仍然是全球公共卫生的沉重负担。尽管通过接种保护性疫苗已成功降低了HBV感染的新发病率,但慢性HBV感染约占所有肝细胞癌(HCC)病例的一半,约占HCC死亡总数的33%。目前对慢性HBV感染的治疗仅限于I型干扰素和核苷酸类似物,但这两种方法都不能治愈,因为它们对病毒复制模板共价闭合环状DNA(cccDNA)的作用有限。
HBV是一种部分双链松弛环状DNA病毒,其基因组为3.2 kb,编码四个重叠的开放阅读框(ORFs)。感染后,HBV松弛环状DNA(rcDNA)转变为cccDNA。cccDNA在细胞核中积累,与组蛋白和非组蛋白相互作用形成微型染色体,作为实现病毒RNA转录的模板。很明显,一系列组蛋白翻译后修饰(PTMs),包括活性PTMs H3K4me3、H3K27ac、H3K36me3、H3K122ac,以及抑制性PTMs H3K9me3和H3K27me3,直接在cccDNA上富集,提供了cccDNA转录活性的动态表观遗传调控。最近的研究表明,这些表观遗传机制已被最关键的病毒蛋白HBx采用,以促进HBV转录。例如,HBx将p300/CBP和PACF募集到cccDNA并乙酰化组蛋白,以促进HBV复制。此外,HBx反式激活HAT1并促进cccDNA上的组蛋白乙酰化,以增强cccDNA转录。然而,既参与cccDNA转录调控又受HBV/HBx操纵的宿主因子尚未完全确定。需要进一步鉴定这些宿主因子以确定用于HBV治疗的药物靶点。
长链非编码RNAs(lncRNAs)是一类长度超过200个核苷酸的异质性转录本,具有很少或没有蛋白质编码潜能,已被证明在各种细胞过程中发挥关键的调节作用,包括调节基因表达和表观遗传修饰。新出现的证据表明lncRNAs参与介导宿主细胞与包括HCV和HBV在内的多种病毒之间的相互作用。据报道,lncRNAs以HBx依赖性方式通过重塑cccDNA微型染色体来调节HBV复制。LncRNA HULC通过调节HBx/STAT3/miR-539/APOBEC3B信号通路激活HBV复制并加速HCC进展。LncRNA HOTAIR与DDX5/PRC2相互作用以抑制cccDNA转录,而HBx结合的lncRNA DLEU2可维持cccDNA和癌症相关基因的转录。因此,鉴定HBx靶向的、且在表观遗传上抑制HBV转录的新型lncRNAs,对于开发新的HBV治疗策略具有重要意义。
近日,Advanced Science(IF16.806)期刊发表了题为LINC01431 Promotes Histone H4R3 Methylation to Impede HBV Covalently Closed Circular DNA Transcription by Stabilizing PRMT1的研究论文。报道了一个可被HBx下调并抑制cccDNA转录的新型HBV限制性lncRNA LINC01431,并揭示了HBx-LINC01431-PRMT1在调节HBV cccDNA转录中的关键调控作用,暗示其可能是HBV治疗的潜在靶点。

首先,为了鉴定负责调节肝细胞中HBV复制的lncRNAs,研究人员对有或无HBV感染的HLCZ01细胞(HLCZ01细胞是一种可支持HBV整个生命周期的肝癌细胞系)进行了lncRNA测序,结果在HBV感染的HLCZ01细胞中总共鉴定出306个差异表达的lncRNAs(60个上调和246个下调),进一步分析发现LINC01431是一种新的被HBx下调的lncRNA,并且高水平的HBV复制与低水平的LINC01431相关。

接着,为了评价LINC01431在HBV复制中的作用,研究人员通过核质分离和RNA FISH实验证实了LINC01431定位于细胞核。功能获得性和缺失性实验显示,LINC01431过表达显著抑制了HBV复制,而LINC01431敲低则促进了HBV复制,表现为所有检测到的细胞中HBV抗原(HBsAg/HBeAg)、HBV病毒粒子和pgRNA的产生增加。体内实验显示LINC01431过表达显著降低了HBsAg和HBV DNA的血清水平,以及肝脏HBcAg表达。证明了LINC01431是HBV复制的宿主限制因子。

随后,为了详细表征LINC01431引发的HBV抑制,研究人员采用了几种支持HBV复制的细胞模型。结果发现LINC01431过表达显著降低HepaRGNTCP细胞中的HBV抗原、病毒DNA和RNA,但对cccDNA水平和pgRNA稳定性影响不大,提示LINC01431特异性抑制cccDNA转录。鉴于组蛋白修饰在cccDNA微型染色体上起着调控cccDNA转录的重要作用。因此,研究人员探讨了LINC01431是否影响了cccDNA的表观遗传修饰。结果显示LINC01431过表达大大降低了包括H3K4me3和H3K27ac在内的活性修饰的富集,而LINC01431敲低则显著增加了对cccDNA结合的组蛋白的这些修饰。表明LINC01431是一种新型HBV转录宿主限制因子。

机制研究表明,LINC01431与I型蛋白精氨酸甲基转移酶(PRMT1)竞争性结合,以阻断HBx介导的PRMT1泛素化和降解。因此,LINC01431增加了PRMT1在cccDNA上的占有率,导致H4R3me2a修饰增强和cccDNA结合的组蛋白乙酰化减少,从而抑制cccDNA转录。反过来,为了促进病毒复制,HBV通过HBx介导的转录因子ZHX2(锌指和同源框2)的抑制来转录抑制LINC01431的表达。
总的来说,本研究证明了LINC01431是cccDNA微型染色体的一种新型表观遗传调节因子,并强调了HBx-LINC01431-PRMT1在HBV复制中的反馈回路,为HBV治疗提供了潜在的治疗靶点。
原文链接:
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202103135
本研究中使用到的18S、U6、LINC01431 FISH探针&试剂盒、生物素标记T7体外转录试剂盒均由锐博生物提供!更多产品与服务信息,欢迎登陆锐博生物官方网站查询或来电咨询!
HBV是一种部分双链松弛环状DNA病毒,其基因组为3.2 kb,编码四个重叠的开放阅读框(ORFs)。感染后,HBV松弛环状DNA(rcDNA)转变为cccDNA。cccDNA在细胞核中积累,与组蛋白和非组蛋白相互作用形成微型染色体,作为实现病毒RNA转录的模板。很明显,一系列组蛋白翻译后修饰(PTMs),包括活性PTMs H3K4me3、H3K27ac、H3K36me3、H3K122ac,以及抑制性PTMs H3K9me3和H3K27me3,直接在cccDNA上富集,提供了cccDNA转录活性的动态表观遗传调控。最近的研究表明,这些表观遗传机制已被最关键的病毒蛋白HBx采用,以促进HBV转录。例如,HBx将p300/CBP和PACF募集到cccDNA并乙酰化组蛋白,以促进HBV复制。此外,HBx反式激活HAT1并促进cccDNA上的组蛋白乙酰化,以增强cccDNA转录。然而,既参与cccDNA转录调控又受HBV/HBx操纵的宿主因子尚未完全确定。需要进一步鉴定这些宿主因子以确定用于HBV治疗的药物靶点。
长链非编码RNAs(lncRNAs)是一类长度超过200个核苷酸的异质性转录本,具有很少或没有蛋白质编码潜能,已被证明在各种细胞过程中发挥关键的调节作用,包括调节基因表达和表观遗传修饰。新出现的证据表明lncRNAs参与介导宿主细胞与包括HCV和HBV在内的多种病毒之间的相互作用。据报道,lncRNAs以HBx依赖性方式通过重塑cccDNA微型染色体来调节HBV复制。LncRNA HULC通过调节HBx/STAT3/miR-539/APOBEC3B信号通路激活HBV复制并加速HCC进展。LncRNA HOTAIR与DDX5/PRC2相互作用以抑制cccDNA转录,而HBx结合的lncRNA DLEU2可维持cccDNA和癌症相关基因的转录。因此,鉴定HBx靶向的、且在表观遗传上抑制HBV转录的新型lncRNAs,对于开发新的HBV治疗策略具有重要意义。
近日,Advanced Science(IF16.806)期刊发表了题为LINC01431 Promotes Histone H4R3 Methylation to Impede HBV Covalently Closed Circular DNA Transcription by Stabilizing PRMT1的研究论文。报道了一个可被HBx下调并抑制cccDNA转录的新型HBV限制性lncRNA LINC01431,并揭示了HBx-LINC01431-PRMT1在调节HBV cccDNA转录中的关键调控作用,暗示其可能是HBV治疗的潜在靶点。

首先,为了鉴定负责调节肝细胞中HBV复制的lncRNAs,研究人员对有或无HBV感染的HLCZ01细胞(HLCZ01细胞是一种可支持HBV整个生命周期的肝癌细胞系)进行了lncRNA测序,结果在HBV感染的HLCZ01细胞中总共鉴定出306个差异表达的lncRNAs(60个上调和246个下调),进一步分析发现LINC01431是一种新的被HBx下调的lncRNA,并且高水平的HBV复制与低水平的LINC01431相关。

Fig1. HBV感染期间HBx下调LINC01431的表达
接着,为了评价LINC01431在HBV复制中的作用,研究人员通过核质分离和RNA FISH实验证实了LINC01431定位于细胞核。功能获得性和缺失性实验显示,LINC01431过表达显著抑制了HBV复制,而LINC01431敲低则促进了HBV复制,表现为所有检测到的细胞中HBV抗原(HBsAg/HBeAg)、HBV病毒粒子和pgRNA的产生增加。体内实验显示LINC01431过表达显著降低了HBsAg和HBV DNA的血清水平,以及肝脏HBcAg表达。证明了LINC01431是HBV复制的宿主限制因子。

Fig2. LINC01431定位于细胞核,是HBV复制的宿主限制因子
随后,为了详细表征LINC01431引发的HBV抑制,研究人员采用了几种支持HBV复制的细胞模型。结果发现LINC01431过表达显著降低HepaRGNTCP细胞中的HBV抗原、病毒DNA和RNA,但对cccDNA水平和pgRNA稳定性影响不大,提示LINC01431特异性抑制cccDNA转录。鉴于组蛋白修饰在cccDNA微型染色体上起着调控cccDNA转录的重要作用。因此,研究人员探讨了LINC01431是否影响了cccDNA的表观遗传修饰。结果显示LINC01431过表达大大降低了包括H3K4me3和H3K27ac在内的活性修饰的富集,而LINC01431敲低则显著增加了对cccDNA结合的组蛋白的这些修饰。表明LINC01431是一种新型HBV转录宿主限制因子。

Fig3. LINC01431抑制cccDNA的转录
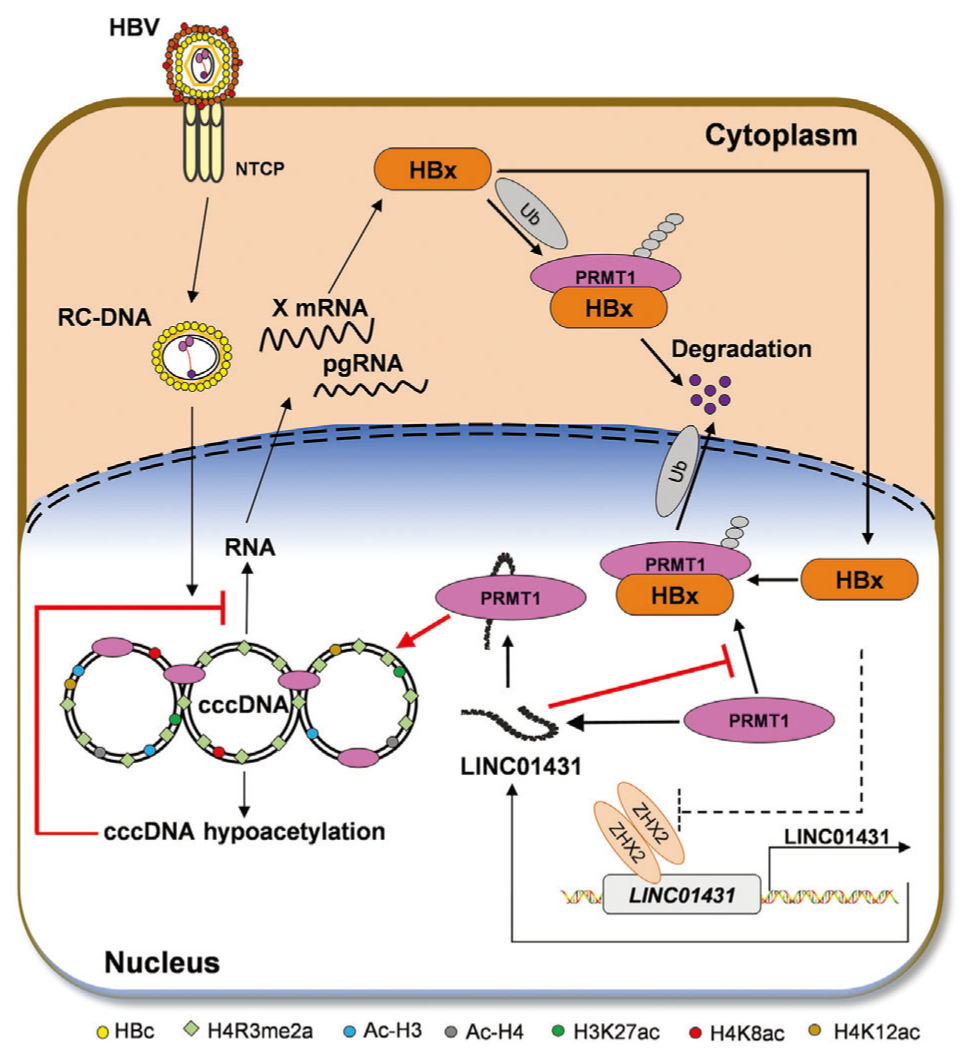
机制研究表明,LINC01431与I型蛋白精氨酸甲基转移酶(PRMT1)竞争性结合,以阻断HBx介导的PRMT1泛素化和降解。因此,LINC01431增加了PRMT1在cccDNA上的占有率,导致H4R3me2a修饰增强和cccDNA结合的组蛋白乙酰化减少,从而抑制cccDNA转录。反过来,为了促进病毒复制,HBV通过HBx介导的转录因子ZHX2(锌指和同源框2)的抑制来转录抑制LINC01431的表达。

Fig4. LINC01431与PRMT1相互作用抑制HBV cccDNA转录的模型示意图
总的来说,本研究证明了LINC01431是cccDNA微型染色体的一种新型表观遗传调节因子,并强调了HBx-LINC01431-PRMT1在HBV复制中的反馈回路,为HBV治疗提供了潜在的治疗靶点。
原文链接:
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202103135
本研究中使用到的18S、U6、LINC01431 FISH探针&试剂盒、生物素标记T7体外转录试剂盒均由锐博生物提供!更多产品与服务信息,欢迎登陆锐博生物官方网站查询或来电咨询!










