推荐产品
公司新闻/正文
lncRNA新研究进展盘点(20220415)
人阅读 发布时间:2022-04-15 09:11
Promoter and enhancer RNAs regulate chromatin reorganization and activation of miR-10b/HOXD locus, and neoplastic transformation in glioma
启动子和增强子RNAs调节染色质重组和miR-10b/HOXD位点的激活,以及胶质瘤的肿瘤转化
发表期刊:Mol Cell
影响因子:17.970
发表时间:2022年3月29日
miR-10b在大脑的正常神经胶质细胞中一般保持沉默,但在胶质瘤中通常被激活,它在其中发挥重要的肿瘤促进作用。本研究证明了整个承载miR-10b的HOXD位点通过涉及3D染色质重组和CTCF-cohesin介导的成环的顺式作用机制在神经胶质瘤中被激活。这种机制需要两个相互作用的lncRNAs,HOXD-AS2和LINC01116,一个与HOXD3/HOXD4/miR-10b启动子相关,另一个与远程增强子相关。在神经胶质瘤细胞中敲低任何一个lncRNA都会改变CTCF和cohesin的结合,破坏染色质成环,抑制HOXD位点内所有基因的表达,并导致神经胶质瘤细胞死亡。相反,在皮质星形胶质细胞中,增强子激活足以进行HOXD/miR-10b位点重组、基因去抑制和肿瘤细胞转化。LINC01116 RNA对于这一过程至关重要。本研究结果证明了两个lncRNAs在染色质折叠中的相互作用,以及协同调控miR-10b和多个HOXD基因在星形胶质细胞中的正常沉默,并触发肿瘤性胶质细胞转化。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35390275/
LINC01431 Promotes Histone H4R3 Methylation to Impede HBV Covalently Closed Circular DNA Transcription by Stabilizing PRMT1
LINC01431通过稳定PRMT1促进组蛋白H4R3甲基化以阻止HBV共价闭合环状DNA转录
发表期刊:Adv Sci (Weinh)
影响因子:16.806
发表时间:2022年4月10日
共价闭合环状DNA(cccDNA)是乙型肝炎病毒(HBV)的转录模板,它与宿主和病毒蛋白相互作用,在细胞核中形成微染色体,并对抗病毒药物具有抗性。鉴定参与cccDNA转录调控的宿主因子有望为HBV治疗提供一个新的途径。最近的证据表明,长链非编码RNAs(lncRNAs)参与介导宿主因子与各种病毒的相互作用。然而,HBV靶向并抑制cccDNA转录的lncRNAs尚未完全阐明。本研究将LINC01431鉴定为一种新型HBV转录宿主限制因子。机制上,LINC01431与PRMT1(I型蛋白精氨酸甲基转移酶)竞争性结合,以阻断HBx介导的PRMT1泛素化和降解。因此,LINC01431增加了PRMT1在cccDNA上的占有率,导致H4R3me2a修饰增强和cccDNA结合组蛋白的乙酰化减少,从而抑制cccDNA转录。反过来,为了促进病毒复制,HBV通过HBx介导的转录因子ZHX2(锌指和同源框2)的抑制来转录抑制LINC01431的表达。总的来说,该研究证明LINC01431是cccDNA微型染色体的一种新型表观遗传调节因子,并突出了HBx-LINC01431-PRMT1在HBV复制中的反馈回路,这为HBV治疗提供了潜在的治疗靶点。

原文链接:https://pubmed.ncbi.nlm.nih.gov/35398991/
Hypoxia-induced HIF-1α/lncRNA-PMAN inhibits ferroptosis by promoting the cytoplasmic translocation of ELAVL1 in peritoneal dissemination from gastric cancer
缺氧诱导的HIF-1α/lncRNA-PMAN通过促进ELAVL1在胃癌腹膜播散中的胞质易位来抑制铁死亡
发表期刊:Redox Biology
影响因子:11.799
发表时间:2022年4月9日
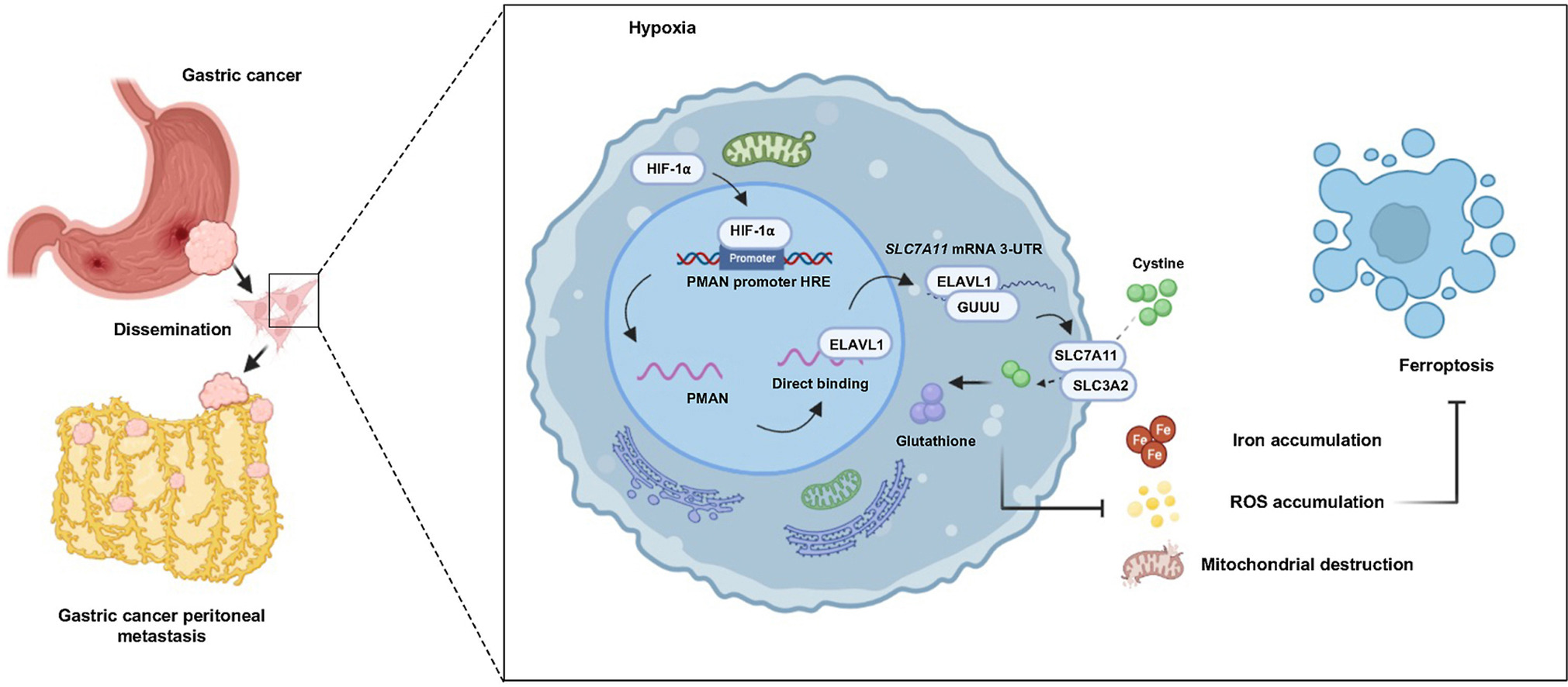
腹膜转移(PM)是胃癌(GC)远处转移的主要部位,预后和生存率极差。缺氧是腹膜转移的共同特征,HIF-1α(缺氧诱导因子1α)的上调可能是PM发生的潜在驱动因素。铁死亡是最近发现的一种受调控的细胞死亡形式,与肿瘤的发生和发展密切相关。然而,将HIF-1α与GC PM中的铁死亡联系起来的潜在机制仍然未知。本研究通过lncRNA微阵列和RNA文库构建/lncRNA-seq分析发现,lncRNA-PMAN在PM中高表达,并受到HIF-1α的显著调节。 PMAN的上调与GC患者的不良预后和PM相关。PMAN被HIF-1α上调并通过促进ELAVL1的细胞质分布来提高SLC7A11 mRNA的稳定性,这在RNA-pulldown/质谱结果中得到了鉴定。SLC7A11的积累会增加l-谷胱甘肽(GSH)的水平并抑制GC细胞中活性氧(ROS)和铁的积累。最后保护GC细胞免受Erastin和RSL3诱导的铁死亡。本研究结果阐明了HIF-1α/PMAN/ELAVL1在GC细胞铁死亡中的作用,并为GC中PM的潜在诊断生物标志物和治疗靶点提供了理论支持。
原文链接:https://www.sciencedirect.com/science/article/pii/S2213231722000842
LncRNA PCAT1 activates SOX2 and suppresses radioimmune responses via regulating cGAS/STING signalling in non-small cell lung cancer
LncRNA PCAT1通过调节非小细胞肺癌中的cGAS/STING信号激活SOX2并抑制放射免疫反应
发表期刊:Clin Transl Med
影响因子:11.492
发表时间:2022年4月12日
背景:长链非编码RNA(lncRNA)PCAT1(前列腺癌相关ncRNA转录本1)在非小细胞肺癌(NSCLC)中的表达增加。它刺激肿瘤生长和转移,但其在放射免疫反应中的作用仍然未知。 本研究旨在探讨PCAT1对NSCLC肿瘤发生和放射免疫反应的影响以及潜在的分子机制。
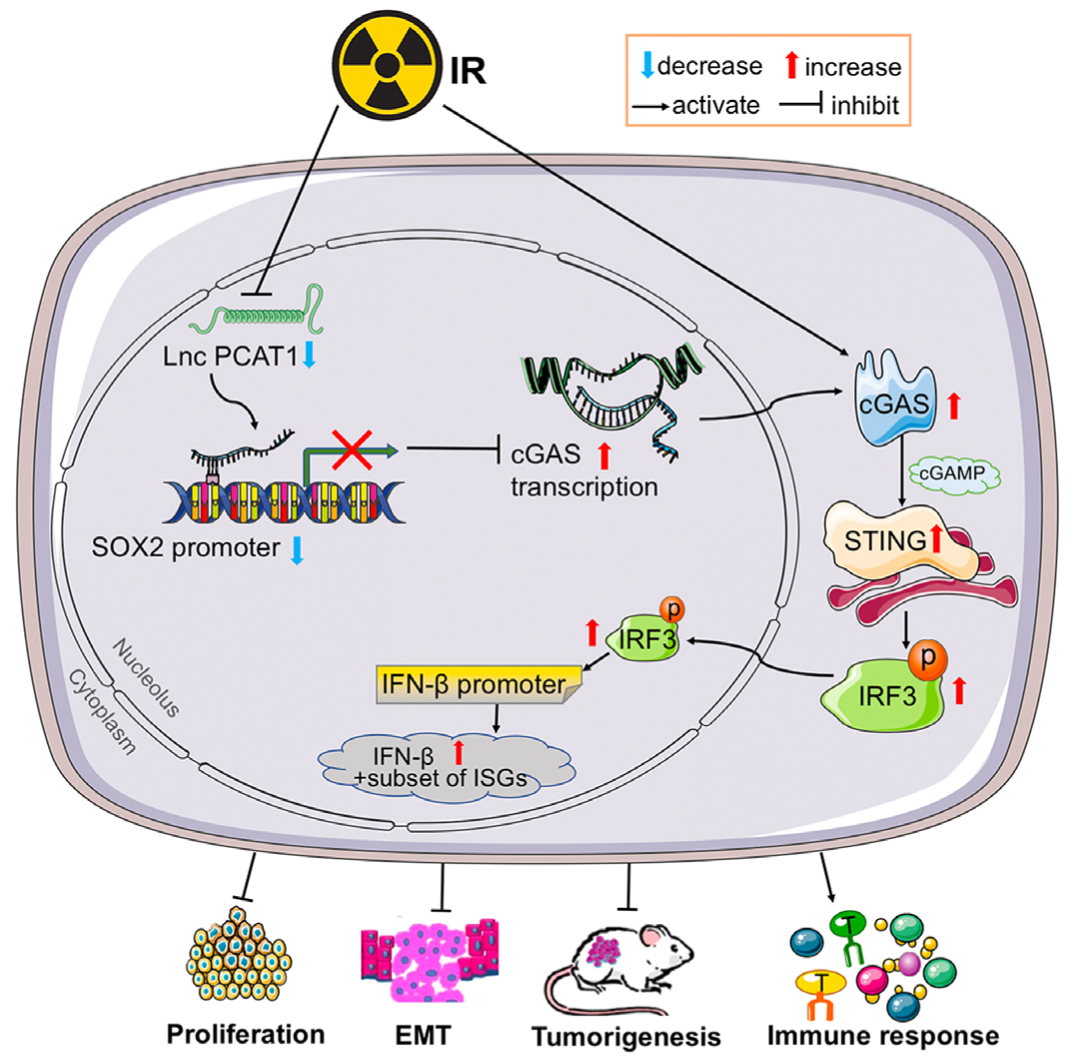
结果:PCAT1具有免疫抑制作用,与NSCLC的侵袭有关。PCAT1增加与NSCLC中的免疫细胞浸润呈负相关。PCAT1敲低在体内和体外抑制增殖、增加细胞凋亡和抑制细胞转移。PCAT1激活SOX2,加速肿瘤发生和免疫抑制。SOX2通过抑制细胞毒性T细胞免疫促进肿瘤生长。此外,SOX2抑制cGAS转录并阻碍下游I型干扰素(IFN)诱导的免疫应答。抑制PCAT1/SOX2协同放疗可进一步抑制肿瘤生长,并启动cGAS/STING信号通路,从而增强NSCLC放疗的免疫应答。
结论:PCAT1/SOX2轴通过抑制cGAS/STING信号介导的T细胞活化促进肿瘤发生和免疫抑制。抑制PCAT1和SOX2与放疗协同激活免疫反应,可作为潜在的治疗靶点。
原文链接:https://pubmed.ncbi.nlm.nih.gov/35415876/
LncRNA PMAT-PtoMYB46 module represses PtoMATE and PtoARF2 promoting Pb2+ uptake and plant growth in poplar
LncRNA PMAT-PtoMYB46组件抑制PtoMATE和PtoARF2以促进杨树中Pb2+的吸收和植物生长
发表期刊:J Hazard Mater
影响因子:10.588
发表时间:2022年3月23日
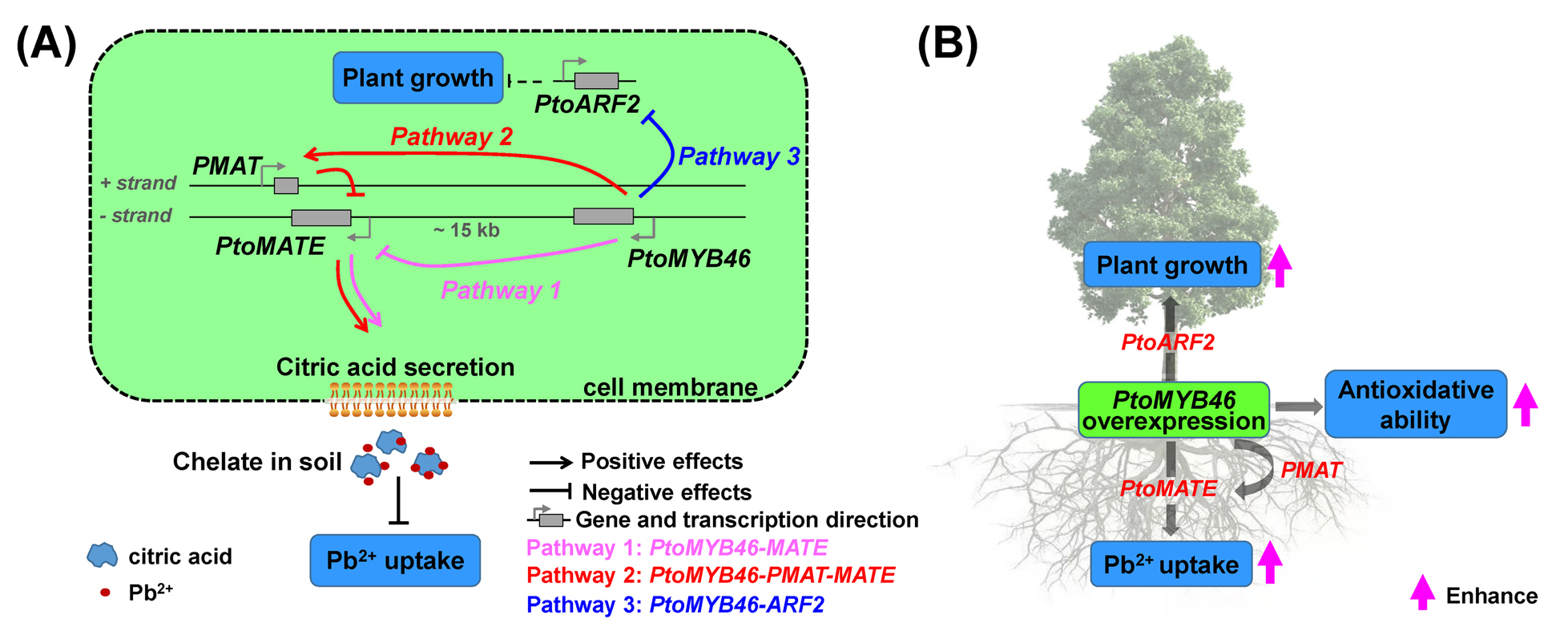
铅(Pb2+)是最具毒性的重金属污染物之一。具有大量生物量的速生型木本植物是生物修复的理想选择。然而,木本植物中Pb2+摄取的转录调控仍然不清楚。本研究在毛白杨(Populus tomentosa)中鉴定了226个Pb2+诱导的、差异表达的长链非编码RNAs(DELs)。功能注释显示,这些DELs主要通过其潜在的靶基因调节碳代谢、次生代谢物的生物合成、能量代谢和信号转导。关联和上位性分析表明,lncRNA PMAT(Pb2+诱导的MATE(多药和有毒化合物挤压)反义lncRNA)与PtoMYB46上位相互作用以调节叶片干重、光合作用速率和转酮酶活性。遗传转化和分子检测表明,PtoMYB46通过PMAT直接或间接降低PtoMATE的表达,从而减少柠檬酸(CA)的分泌,最终促进Pb2+的摄取。同时,PtoMYB46靶向ARF2(生长素应答因子2)并降低其表达,从而正向调节植物生长。本研究结果表明PMAT-PtoMYB46-PtoMATE-PtoARF2调节模块控制Pb2+耐受性、吸收和植物生长。这项研究证明了lncRNAs参与响应杨树中的Pb2+,为开发用于植物修复铅污染土壤的遗传改良木本植物品种的潜力提供了新的见解。
原文链接:https://pubmed.ncbi.nlm.nih.gov/35364535/
启动子和增强子RNAs调节染色质重组和miR-10b/HOXD位点的激活,以及胶质瘤的肿瘤转化
发表期刊:Mol Cell
影响因子:17.970
发表时间:2022年3月29日
miR-10b在大脑的正常神经胶质细胞中一般保持沉默,但在胶质瘤中通常被激活,它在其中发挥重要的肿瘤促进作用。本研究证明了整个承载miR-10b的HOXD位点通过涉及3D染色质重组和CTCF-cohesin介导的成环的顺式作用机制在神经胶质瘤中被激活。这种机制需要两个相互作用的lncRNAs,HOXD-AS2和LINC01116,一个与HOXD3/HOXD4/miR-10b启动子相关,另一个与远程增强子相关。在神经胶质瘤细胞中敲低任何一个lncRNA都会改变CTCF和cohesin的结合,破坏染色质成环,抑制HOXD位点内所有基因的表达,并导致神经胶质瘤细胞死亡。相反,在皮质星形胶质细胞中,增强子激活足以进行HOXD/miR-10b位点重组、基因去抑制和肿瘤细胞转化。LINC01116 RNA对于这一过程至关重要。本研究结果证明了两个lncRNAs在染色质折叠中的相互作用,以及协同调控miR-10b和多个HOXD基因在星形胶质细胞中的正常沉默,并触发肿瘤性胶质细胞转化。

Fig1. 胶质母细胞瘤中HOXD/miR-10b基因去抑制的机制模型
原文链接:https://pubmed.ncbi.nlm.nih.gov/35390275/
LINC01431 Promotes Histone H4R3 Methylation to Impede HBV Covalently Closed Circular DNA Transcription by Stabilizing PRMT1
LINC01431通过稳定PRMT1促进组蛋白H4R3甲基化以阻止HBV共价闭合环状DNA转录
发表期刊:Adv Sci (Weinh)
影响因子:16.806
发表时间:2022年4月10日
共价闭合环状DNA(cccDNA)是乙型肝炎病毒(HBV)的转录模板,它与宿主和病毒蛋白相互作用,在细胞核中形成微染色体,并对抗病毒药物具有抗性。鉴定参与cccDNA转录调控的宿主因子有望为HBV治疗提供一个新的途径。最近的证据表明,长链非编码RNAs(lncRNAs)参与介导宿主因子与各种病毒的相互作用。然而,HBV靶向并抑制cccDNA转录的lncRNAs尚未完全阐明。本研究将LINC01431鉴定为一种新型HBV转录宿主限制因子。机制上,LINC01431与PRMT1(I型蛋白精氨酸甲基转移酶)竞争性结合,以阻断HBx介导的PRMT1泛素化和降解。因此,LINC01431增加了PRMT1在cccDNA上的占有率,导致H4R3me2a修饰增强和cccDNA结合组蛋白的乙酰化减少,从而抑制cccDNA转录。反过来,为了促进病毒复制,HBV通过HBx介导的转录因子ZHX2(锌指和同源框2)的抑制来转录抑制LINC01431的表达。总的来说,该研究证明LINC01431是cccDNA微型染色体的一种新型表观遗传调节因子,并突出了HBx-LINC01431-PRMT1在HBV复制中的反馈回路,这为HBV治疗提供了潜在的治疗靶点。

Fig2. LINC01431和PRMT1相互作用抑制HBV cccDNA转录的模型示意图
原文链接:https://pubmed.ncbi.nlm.nih.gov/35398991/
Hypoxia-induced HIF-1α/lncRNA-PMAN inhibits ferroptosis by promoting the cytoplasmic translocation of ELAVL1 in peritoneal dissemination from gastric cancer
缺氧诱导的HIF-1α/lncRNA-PMAN通过促进ELAVL1在胃癌腹膜播散中的胞质易位来抑制铁死亡
发表期刊:Redox Biology
影响因子:11.799
发表时间:2022年4月9日
腹膜转移(PM)是胃癌(GC)远处转移的主要部位,预后和生存率极差。缺氧是腹膜转移的共同特征,HIF-1α(缺氧诱导因子1α)的上调可能是PM发生的潜在驱动因素。铁死亡是最近发现的一种受调控的细胞死亡形式,与肿瘤的发生和发展密切相关。然而,将HIF-1α与GC PM中的铁死亡联系起来的潜在机制仍然未知。本研究通过lncRNA微阵列和RNA文库构建/lncRNA-seq分析发现,lncRNA-PMAN在PM中高表达,并受到HIF-1α的显著调节。 PMAN的上调与GC患者的不良预后和PM相关。PMAN被HIF-1α上调并通过促进ELAVL1的细胞质分布来提高SLC7A11 mRNA的稳定性,这在RNA-pulldown/质谱结果中得到了鉴定。SLC7A11的积累会增加l-谷胱甘肽(GSH)的水平并抑制GC细胞中活性氧(ROS)和铁的积累。最后保护GC细胞免受Erastin和RSL3诱导的铁死亡。本研究结果阐明了HIF-1α/PMAN/ELAVL1在GC细胞铁死亡中的作用,并为GC中PM的潜在诊断生物标志物和治疗靶点提供了理论支持。

Fig3. 缺氧时PMAN通过SLC7A11调节铁死亡的模型示意图
原文链接:https://www.sciencedirect.com/science/article/pii/S2213231722000842
LncRNA PCAT1 activates SOX2 and suppresses radioimmune responses via regulating cGAS/STING signalling in non-small cell lung cancer
LncRNA PCAT1通过调节非小细胞肺癌中的cGAS/STING信号激活SOX2并抑制放射免疫反应
发表期刊:Clin Transl Med
影响因子:11.492
发表时间:2022年4月12日
背景:长链非编码RNA(lncRNA)PCAT1(前列腺癌相关ncRNA转录本1)在非小细胞肺癌(NSCLC)中的表达增加。它刺激肿瘤生长和转移,但其在放射免疫反应中的作用仍然未知。 本研究旨在探讨PCAT1对NSCLC肿瘤发生和放射免疫反应的影响以及潜在的分子机制。
结果:PCAT1具有免疫抑制作用,与NSCLC的侵袭有关。PCAT1增加与NSCLC中的免疫细胞浸润呈负相关。PCAT1敲低在体内和体外抑制增殖、增加细胞凋亡和抑制细胞转移。PCAT1激活SOX2,加速肿瘤发生和免疫抑制。SOX2通过抑制细胞毒性T细胞免疫促进肿瘤生长。此外,SOX2抑制cGAS转录并阻碍下游I型干扰素(IFN)诱导的免疫应答。抑制PCAT1/SOX2协同放疗可进一步抑制肿瘤生长,并启动cGAS/STING信号通路,从而增强NSCLC放疗的免疫应答。
结论:PCAT1/SOX2轴通过抑制cGAS/STING信号介导的T细胞活化促进肿瘤发生和免疫抑制。抑制PCAT1和SOX2与放疗协同激活免疫反应,可作为潜在的治疗靶点。

Fig4. PCAT1通过调节NSCLC中的cGAS/STING信号以激活SOX2并抑制放射免疫反应的潜在机制示意图
原文链接:https://pubmed.ncbi.nlm.nih.gov/35415876/
LncRNA PMAT-PtoMYB46 module represses PtoMATE and PtoARF2 promoting Pb2+ uptake and plant growth in poplar
LncRNA PMAT-PtoMYB46组件抑制PtoMATE和PtoARF2以促进杨树中Pb2+的吸收和植物生长
发表期刊:J Hazard Mater
影响因子:10.588
发表时间:2022年3月23日
铅(Pb2+)是最具毒性的重金属污染物之一。具有大量生物量的速生型木本植物是生物修复的理想选择。然而,木本植物中Pb2+摄取的转录调控仍然不清楚。本研究在毛白杨(Populus tomentosa)中鉴定了226个Pb2+诱导的、差异表达的长链非编码RNAs(DELs)。功能注释显示,这些DELs主要通过其潜在的靶基因调节碳代谢、次生代谢物的生物合成、能量代谢和信号转导。关联和上位性分析表明,lncRNA PMAT(Pb2+诱导的MATE(多药和有毒化合物挤压)反义lncRNA)与PtoMYB46上位相互作用以调节叶片干重、光合作用速率和转酮酶活性。遗传转化和分子检测表明,PtoMYB46通过PMAT直接或间接降低PtoMATE的表达,从而减少柠檬酸(CA)的分泌,最终促进Pb2+的摄取。同时,PtoMYB46靶向ARF2(生长素应答因子2)并降低其表达,从而正向调节植物生长。本研究结果表明PMAT-PtoMYB46-PtoMATE-PtoARF2调节模块控制Pb2+耐受性、吸收和植物生长。这项研究证明了lncRNAs参与响应杨树中的Pb2+,为开发用于植物修复铅污染土壤的遗传改良木本植物品种的潜力提供了新的见解。

Fig5. Pb2+处理下毛白杨中涉及PMAT、PtoMYB46、PtoMATE和PtoARF2的Pb2+摄取和植物生长调控网络模型
原文链接:https://pubmed.ncbi.nlm.nih.gov/35364535/










