广州市锐博生物科技有限公司品牌商
18 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
推荐产品
公司新闻/正文
J Hematol Oncol(IF29.5)丨myCAFs来源的外泌体lncRNA PWAR6是CRC肝转移的关键标志物
452 人阅读发布时间:2024-12-30 11:41
使用到的RiboBio产品或服务
1. NRF2 shRNA and SLC38A2 shRNA was purchased from Ribobio(Guangzhou, China).
2. Incubate the biotinylated PWAR6 probe (Ribobio, China) with streptavidin magnetic beads (CST,USA) at room temperature for 30 min, then wash the beads to remove unbound probes.
3. Besides, tail vein injections of a scrambled ASO or the inhibitor ASO-PWAR6 (10 nmol per injection, RiboBio) were performed in the mice every 3 days.
结直肠癌(CRC)是全球第三大最常见的恶性肿瘤,也是癌症相关死亡的第二大原因。随着CRC综合治疗的进步,局部CRC患者的5年总生存率(OS)现已超过90%。与此形成鲜明对比的是,伴有远处转移的CRC患者的5年OS率仍然很低,低于15%。同时,大约22%的CRC患者在初步诊断时面临同步远处转移的挑战。因此,了解CRC转移进展中的关键分子和调节机制至关重要。这些努力可能在早期干预、有效治疗和改善CRC患者的临床结果方面带来巨大的希望。
肿瘤细胞的内在干性和代谢重编程是它们的两个关键特征。癌症干性是驱动CRC发生和发展的基本特征,具有自我更新能力和肿瘤发生潜力。在之前的工中,研究人员也发现转移性CRC类器官具有显著的干性特征。抑制维持干细胞特性的关键转录因子SOX2可能会极大地阻碍类器官生长和转移潜力。鉴于干性特征在CRC中的关键作用,针对癌症干性的研究可能会揭示对抗CRC转移的潜在治疗靶点。
同样,代谢重编程在驱动肿瘤进展和转移中也至关重要。在这些改变中,异常的葡萄糖和谷氨酰胺消耗是CRC中观察到的最普遍的代谢变化。与葡萄糖的快速利用相反,谷氨酰胺对于支持三羧酸(TCA)循环至关重要,并且是脂质、核苷酸和己糖胺合成的重要前体。我们的初步研究也证实了CRC组织中谷氨酸及其下游产物的显著增加,提示CRC细胞中谷氨酰胺分解代谢的异常激活。此外,各种研究也表明,环境中的谷氨酰胺剥夺显著增强了多种癌细胞的干性特性,从而促进疾病进展。这些发现表明,癌细胞的代谢改变不仅影响细胞间营养代谢,而且深刻影响内在的干性特性。
众所周知,CRC细胞还与肿瘤周围环境,即肿瘤微环境(TME),建立了错综复杂的联系。这种环境包括癌症相关成纤维细胞(CAF)、免疫细胞和其他营养成分。其中,CAFs已被确定为TME中最丰富的基质成分,可根据其功能和分子标志物分为不同的亚型,例如肌成纤维细胞CAFs(myCAFs)、炎性CAFs(iCAFs)和抗原呈递CAFs(apCAFs)。MyCAFs的特征是α-SMA、FAP和I型胶原蛋白的高表达,并参与细胞外基质重塑,促进肿瘤侵袭,并导致肿瘤纤维化。这些特征使CAFs,尤其是myCAFs,在癌症进展中扮演重要角色。CAFs和CRC细胞之间的通讯通常由细胞外信号(尤其是外泌体)促进。外泌体是直径为30-200 nm的小型细胞外囊泡(sEVs),由TME中的各种细胞通过细胞内囊泡与质膜融合而释放。这些外泌体可以运输必需分子,包括蛋白质、脂质和RNAs,显著影响肿瘤细胞的特性。例如,有研究发现,CRC细胞可以摄取由CAFs分泌的含有miR-92a-3p的外泌体,诱导上皮-间充质转化(EMT)并促进CRC的转移。此外,还有研究报道,CAFs可以通过外泌体递送长链非编码RNA(lncRNA)来增强CRC的化疗耐药性。在之前的研究中,研究人员发现活化的CAFs可以分泌大量的促炎细胞因子,促进CRC的转移。
此外,据报道,myCAFs不仅在肿瘤细胞中,而且在TME内重编程营养代谢,从而影响代谢图谱。为了满足肿瘤细胞对谷氨酰胺需求的增加,myCAFs主动上调合成代谢途径,并将谷氨酰胺分泌到TME中,从而维持其供应。此外,myCAFs可以通过外泌体介导的机制抑制肿瘤细胞中的氧化磷酸化过程,从而促进谷氨酰胺依赖性还原羧化。尽管取得了这些进展,但myCAFs调节TME中谷氨酰胺代谢的具体机制及其对CRC肿瘤干性的影响仍然知之甚少,这凸显了当前研究的重大空白。
在TME中,巨噬细胞、自然杀伤(NK)细胞和T细胞等免疫细胞在肿瘤发生中发挥着多方面的作用,受其激活状态和不同表型的调节。NK细胞作为抗肿瘤免疫的基本组成部分,可以直接识别缺乏MHC-I分子的细胞,并通过分泌颗粒酶和穿孔素杀死肿瘤细胞。同时,NK细胞通过释放穿孔素在靶细胞膜上形成孔来消除感染细胞或肿瘤细胞,使颗粒酶B进入并诱导细胞凋亡。与肿瘤细胞类似,NK细胞和其他免疫细胞也需要TME中的多种营养物质来维持其功能并支持抗肿瘤活性。然而,肿瘤细胞摄取过多的营养会耗尽免疫细胞必需的资源,从而深刻影响其功能。谷氨酰胺作为一种关键代谢产物,在TME中被剥夺会损害活化T细胞的增殖和生长,同时也会抑制M2巨噬细胞的极化。然而,TME内谷氨酰胺耗竭对NK细胞功能的影响仍有待阐明。
近日,Journal of Hematology & Oncology期刊在线发表了一篇题为myCAF-derived exosomal PWAR6 accelerates CRC liver metastasis via altering glutamine availability and NK cell function in the tumor microenvironment的研究论文。该研究报道了一种CAF特异性IncRNA PWAR6,其可以调节TME中谷氨酰胺的可用性,并揭示了PWAR6通过改变TME中的谷氨酰胺可用性和NK细胞功能加速CRC肝转移的作用机制,为临床管理提供了有希望的治疗潜力。

首先,为了探索CAFs在CRC中的作用,研究人员利用从GSE166555和GSE178318获得的单细胞测序数据进行聚类分析发现,CAFs的比例在肝转移CRC患者(CRLM)中高于无LM的患者。具体来说,myCAFs在CRLM中显著升高,而iCAFs、apCAFs和其他CAFs的变化则不那么明显。随后,在meta-GEO和TCGA队列中,建立了myCAF评分以评估大量RNA-seq数据中myCAFs的水平。myCAF评分较高的患者主要在III期和IV期被诊断为CRC,而myCAF评分较低的患者主要在I期和II期。Kaplan-Meier分析显示,myCAF评分升高与CRC患者预后明显较差相关。进一步的研究发现,myCAFs可以增强CRC细胞干性并促进迁移。
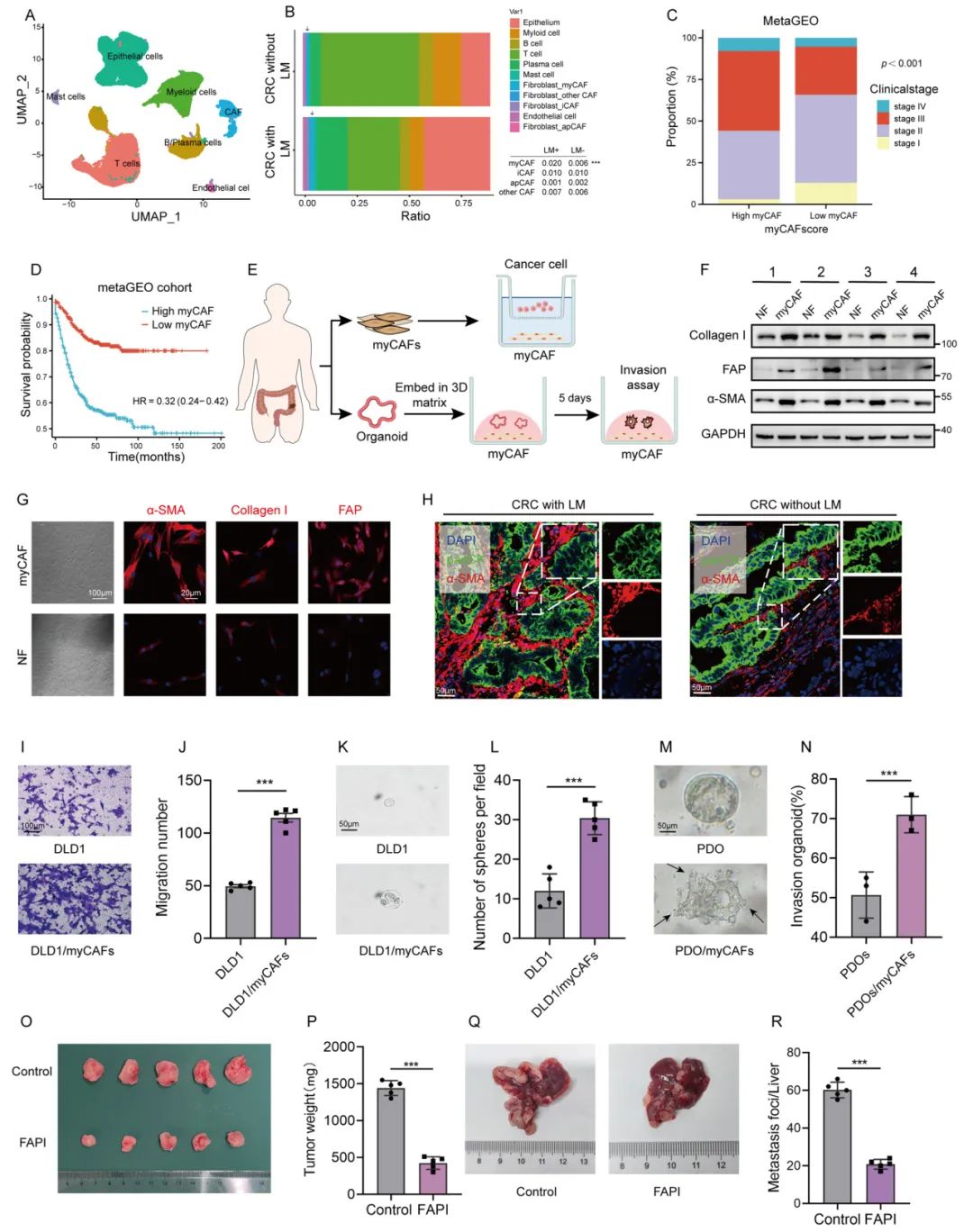
Fig1. myCAFs增强CRC细胞干性并促进迁移
外泌体是myCAFs与TME其他组分之间通信的主要载体。因此,研究人员进行细胞共培养实验以验证外泌体在促进CRC细胞干性和转移中的作用。结果显示,将外泌体抑制剂 GW4869添加到共培养系统中可逆转CRC细胞的迁移速率和干性特性。表明myCAFs通过外泌体促进CRC细胞的转移并增强干性。接着,为了阐明myCAF来源的外泌体(CAF-Exo)对CRC细胞的机制,研究人员进行了外泌体RNA测序。结果发现,lncRNA PWAR6在myCAF-Exo中表现出最显著的上调。随后的功能实验显示,PWAR6敲低显著导致CRC细胞迁移、干性和上皮-间质转化标志物的表达显著降低,并导致体内肝转移瘤和皮下肿瘤的数量和重量显著减少。表明myCAF来源的外泌体PWAR6在体外和体内均促进CRC干性和转移。
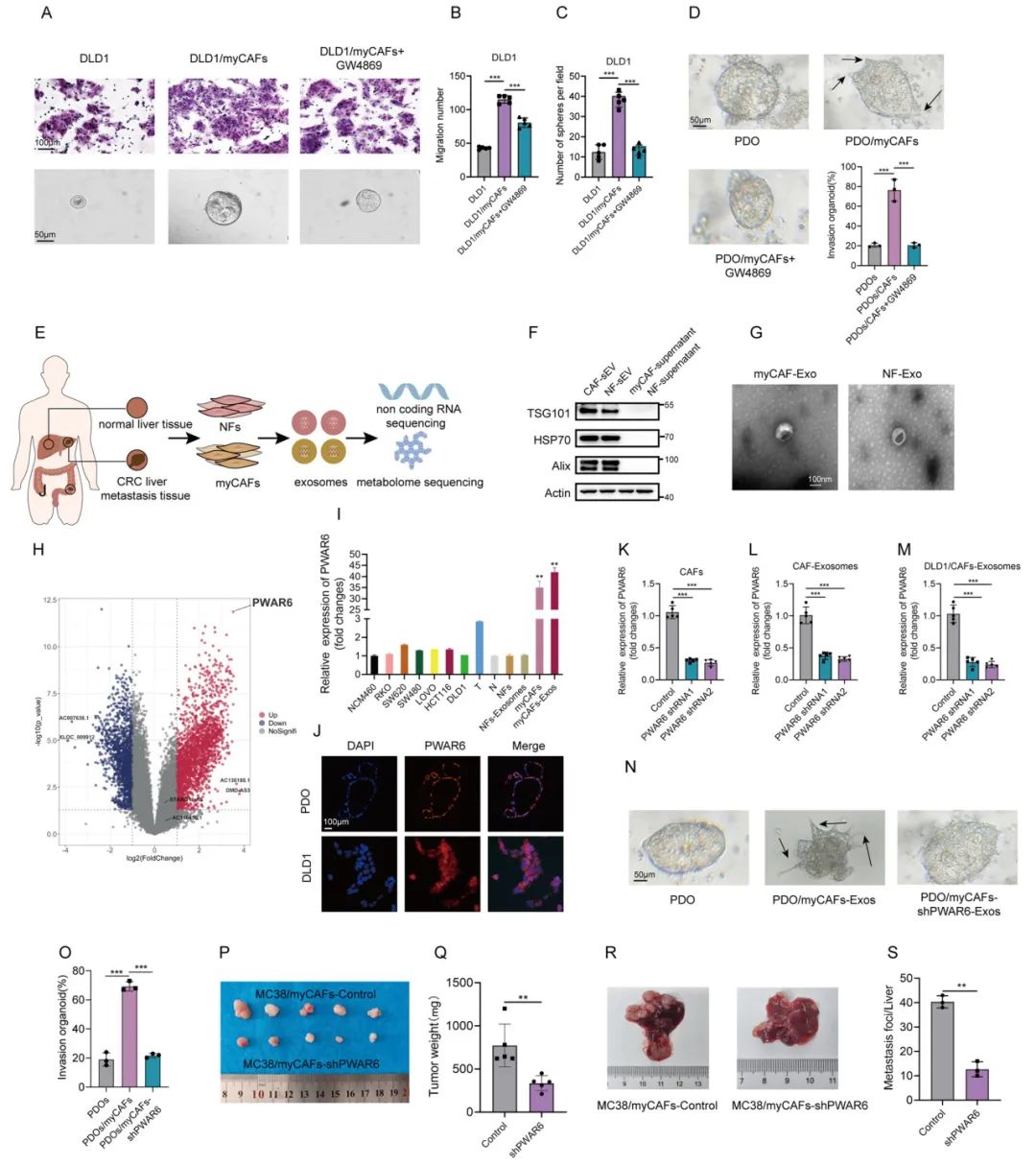
Fig2. myCAF来源的外泌体PWAR6的鉴定
临床分析显示,较高的PWAR6表达水平与68Ga FAPI-PET/CT SUVmax值的增加密切相关,尤其是在CRLM患者中,其表达显著超过非LM病例和正常结肠组织的表达。回归分析和生存数据进一步支持PWAR6作为阴性预后标志物,其水平升高与患者预后较差相关。
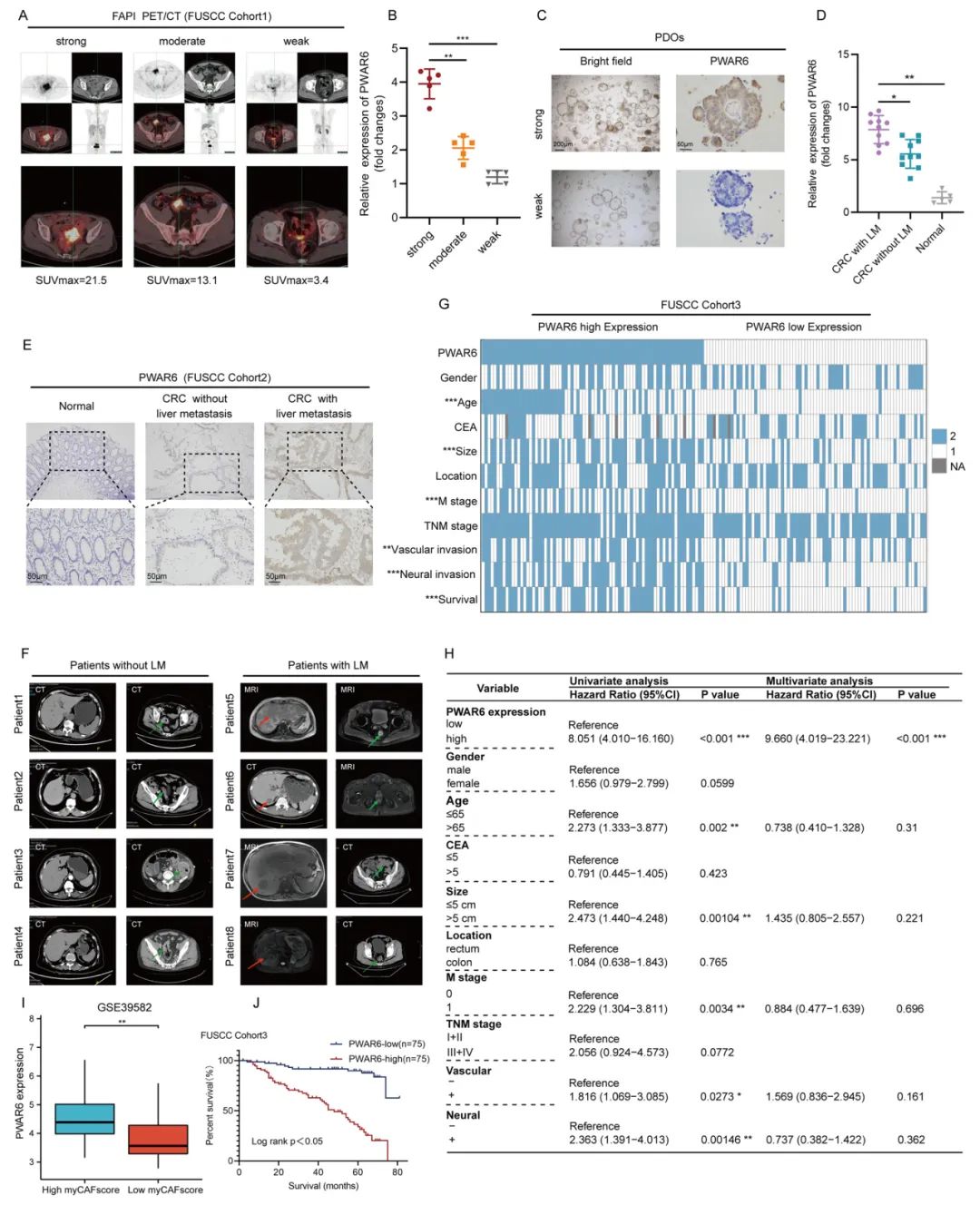
Fig3. exo-PWAR6在CRC患者中的表达及其临床意义
先前myCAF-Exo和myNF-Exo的代谢组测序数据阐明了肝转移中的myCAFs与正常肝组织中NF之间谷氨酰胺代谢途径的显著差异。本研究结果显示,在与myCAFs共培养的CRC细胞中,谷氨酰胺摄取显著增加,谷氨酸和α-酮戊二酸水平升高,但这种增强可以通过敲低CAFs中的PWAR6来逆转。进一步的研究发现,myCAF来源的外泌体PWAR6通过上调氨基酸转运蛋白SLC38A2促进CRC细胞中谷氨酰胺摄取的增加。此外,体内和体外实验还表明,myCAF来源的外泌体PWAR6诱导的SLC38A2上调可以促进CRC细胞的转移。
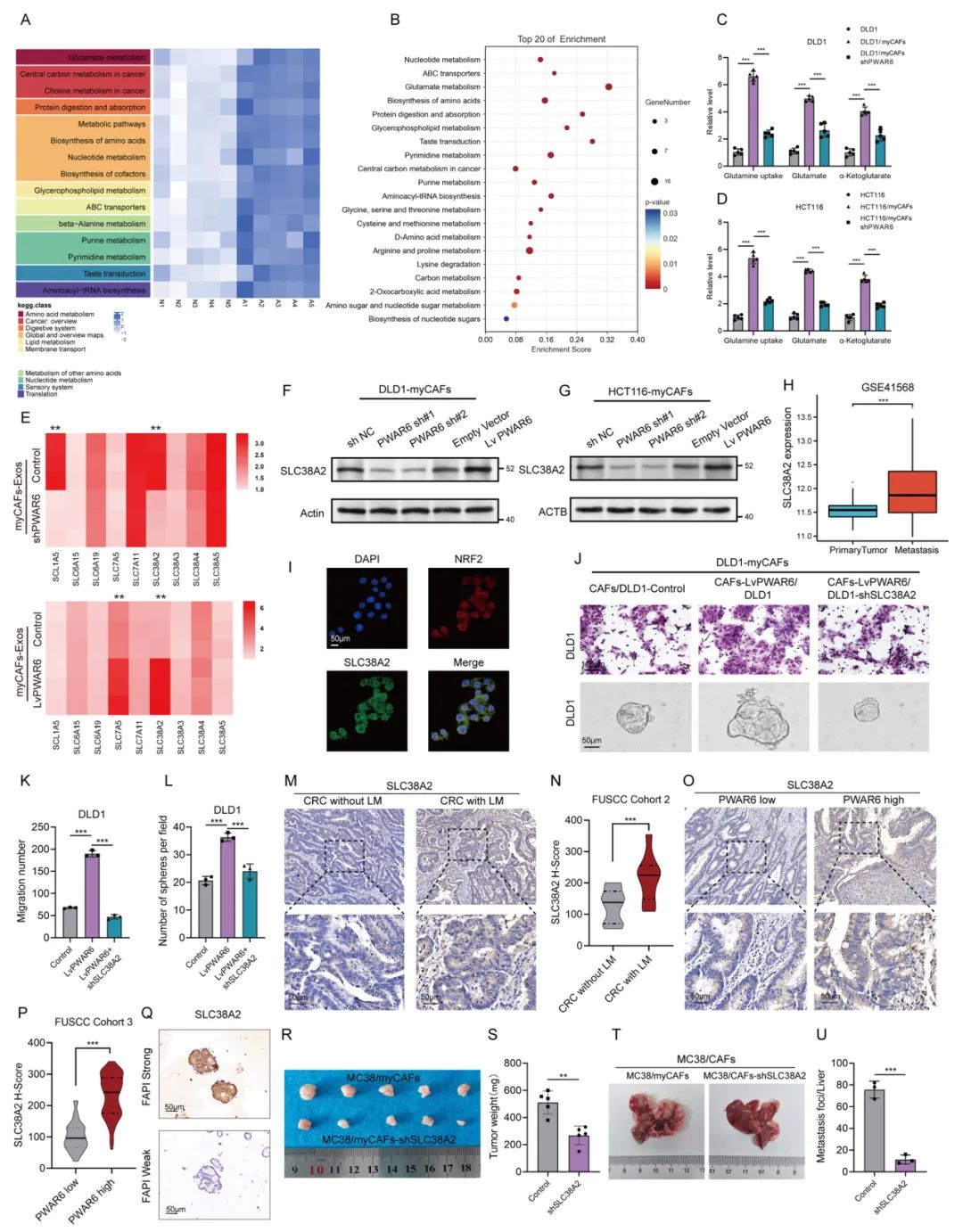
Fig4. myCAF来源的exo-PWAR6通过上调SLC38A2增强CRC细胞的谷氨酰胺摄取
为了阐明myCAF来源的PWAR6调节谷氨酰胺代谢和增强CRC转移的机制,研究人员进行了RNA pulldown、RIP、Co-IP、核质分离、免疫荧光染色、荧光素酶报告基因实验、Western blot等实验。结果发现,PWAR6通过与Keap1竞争性结合抑制NRF2降解,从而上调SLC38A2表达,从而增强CRC细胞中谷氨酰胺的摄取并耗尽NK细胞的谷氨酰胺可用性,最终导致CRC肿瘤进展和转移。
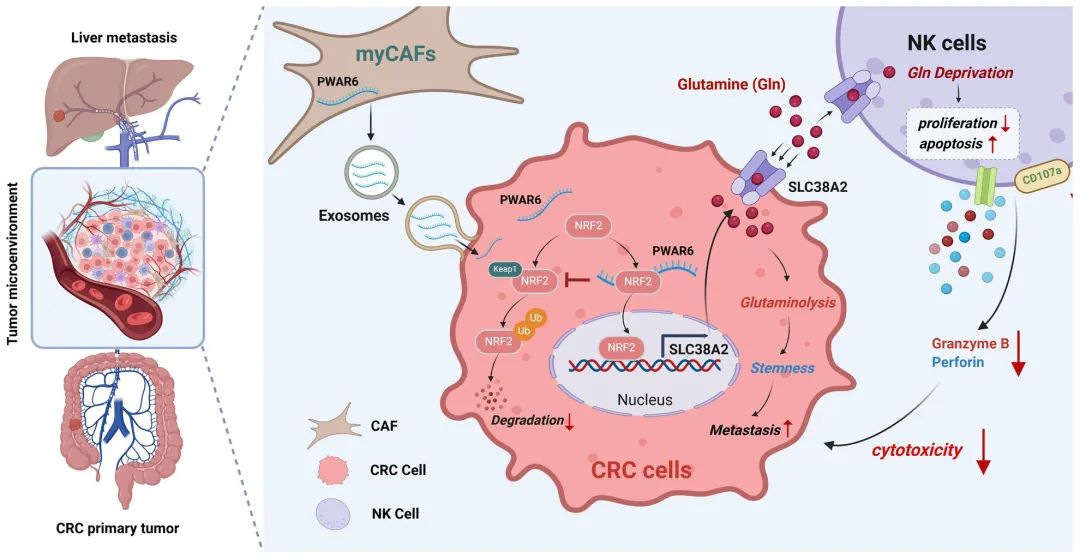
Fig5. 机制模型示意图
最后,基于PWAR6在CRC肿瘤发生中的关键作用,研究人员评估了PWAR6作为治疗靶点的潜力。结果显示,通过尾静脉注射ASO-PWAR6抑制剂显著减少了皮下肿瘤和肝转移肿瘤负荷。此外,ASO-PWAR6尾静脉注射和FAPI(成纤维细胞活化蛋白抑制剂)口服管饲法的组合表明,在减轻皮下肿瘤和肝转移负担方面的疗效增强。表明PWAR6是CRC的潜在治疗靶点。
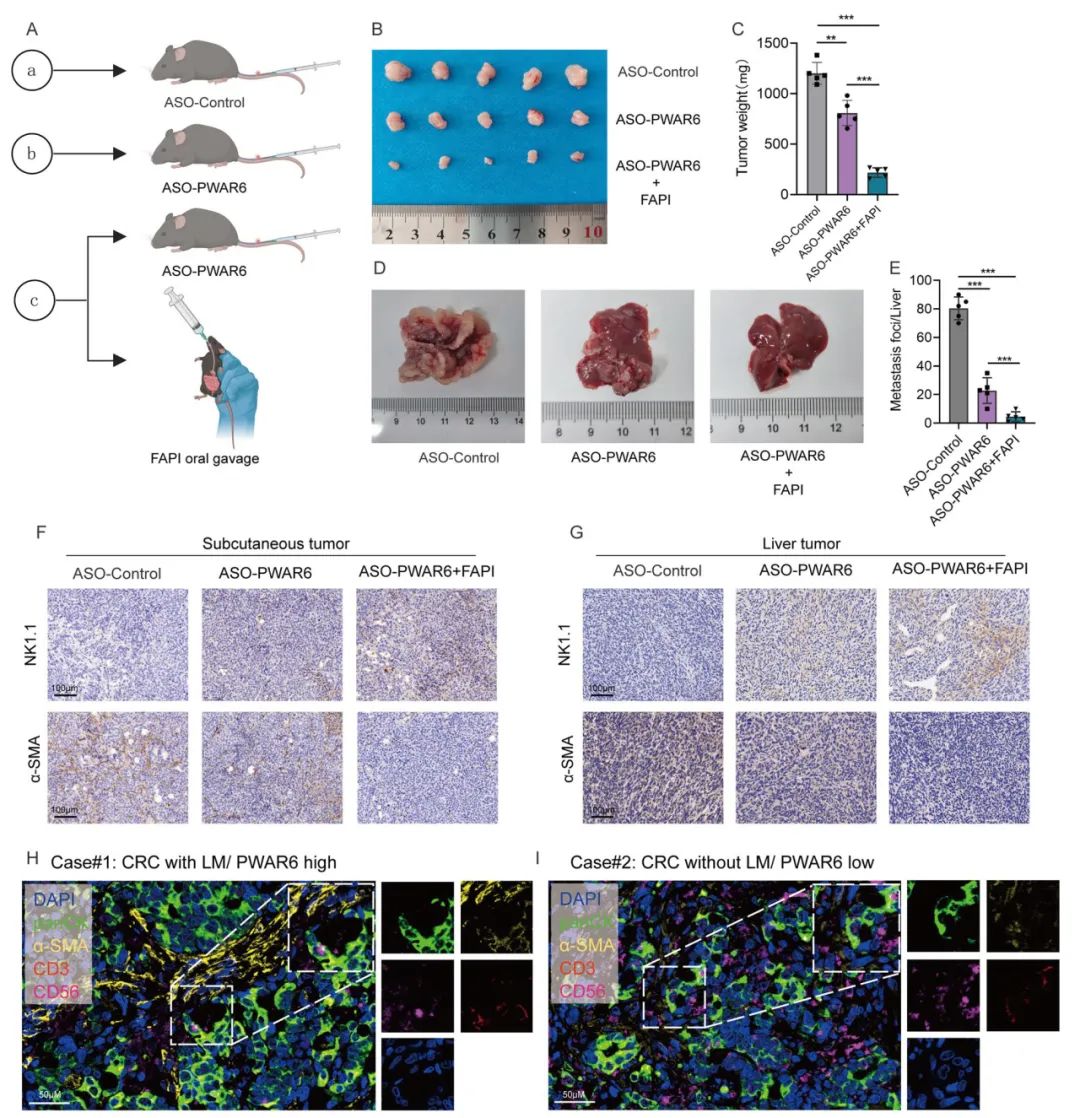
Fig6. PWAR6是CRC的潜在治疗靶点
总之,本研究鉴定了一种myCAF特异性lncRNA PWAR6,它增强了CRC细胞的干性、迁移和谷氨酰胺消耗。机制上,PWAR6与NRF2结合,阻止其与Keap1相互作用,从而抑制NRF2泛素化和降解。NRF2由PWAR6稳定,作为转录因子发挥作用,增强SLC38A2的表达,从而促进CRC细胞从TME摄取谷氨酰胺。这导致TME内的谷氨酰胺耗竭,随后NK细胞凋亡。