广州市锐博生物科技有限公司品牌商
18 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
推荐产品
公司新闻/正文
lncRNA研究进展盘点丨20241216期
437 人阅读发布时间:2024-12-30 11:33
A long noncoding eRNA forms R-loops to shape emotional experience-induced behavioral adaptation
长链非编码eRNA形成R环来塑造情绪体验诱导的行为适应
发表期刊:Science
影响因子:44.7
发表时间:2024年12月12日
情绪体验通常会唤起神经可塑性,从而支持行为的适应性变化,包括与情绪和物质使用障碍相关的适应不良可塑性。这些适应部分由即时早期反应基因的经验依赖性激活所支持的,例如Npas4(神经元PAS结构域蛋白4)。本研究报道了一个从活性敏感增强子转录而来的保守长链非编码增强子RNA(lnc-eRNA),产生DNA:RNA杂交R环结构,支持增强子和近端启动子之间的三维染色质环以及快速Npas4基因诱导。此外,在小鼠模型中,Npas4 lnc-eRNA及其R环是慢性社会心理压力或ke卡因暴露产生的行为适应发展所必需的,揭示了这种调节机制在情绪体验传递中的潜在作用。
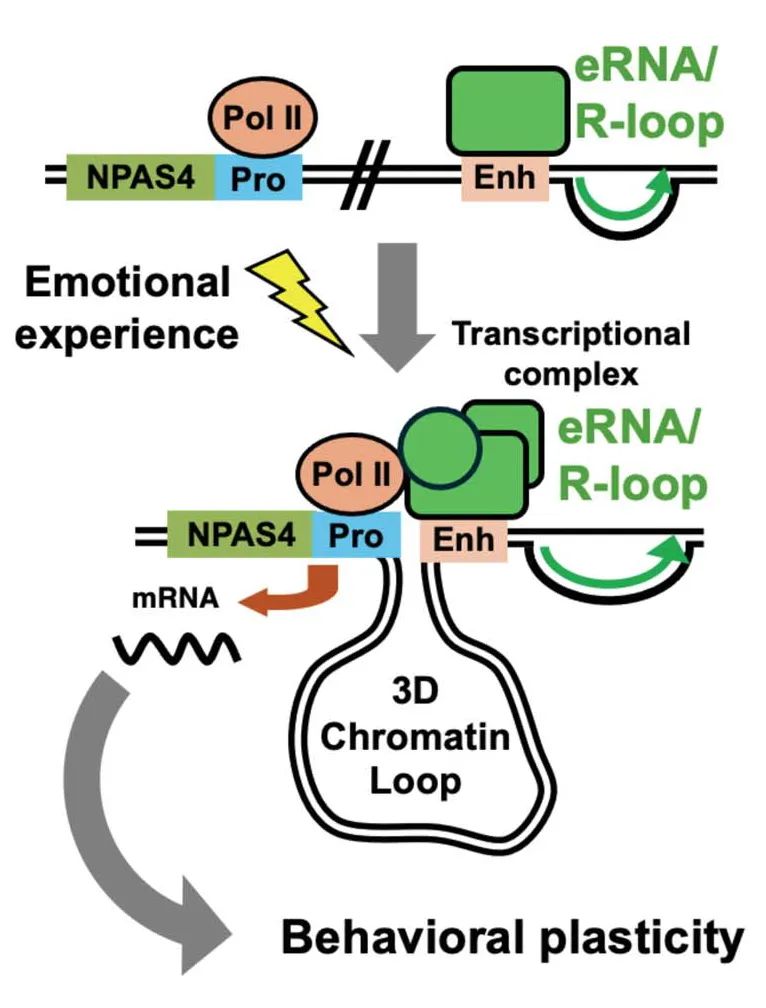
Fig1. 工作模型示意图
The long noncoding RNA ALEX1 confers a functional phase state of ARF3 to enhance rice resistance to bacterial pathogens
长链非编码RNA ALEX1赋予ARF3的功能相态以增强水稻对细菌病原体的抗性
发表期刊:Mol Plant
影响因子:17.1
发表时间:2024年12月9日
水稻白叶枯病在世界范围内是一种毁灭性的疾病,会导致严重的产量损失。了解植物如何抵御微生物感染对于可持续作物生产至关重要。研究人员之前鉴定了一种病原体诱导的长链非编码RNA(ALEX1)。本研究发现ALEX1定位于细胞核并直接与生长素反应因子3(ARF3)结合。研究表明ARF3通过其固有无序的中间区域(MR)在细胞核中形成冷凝物。值得注意的是,ARF3冷凝物具有类似固体的特性。进一步实验揭示ALEX1直接与ARF3的MR结合,调节ARF3凝聚物动力学并促进ARF3同源二聚化。ARF3的分散和二聚体形式,称为其功能相态,增强了其转录抑制下游靶基因(如JAZ13)的能力,从而调节茉莉酸(JA)信号通路并增强水稻对病原体的抗性。本研究强调了长链非编码RNA在调节蛋白质凝聚和组装中的作用,有助于植物的病原体防御。
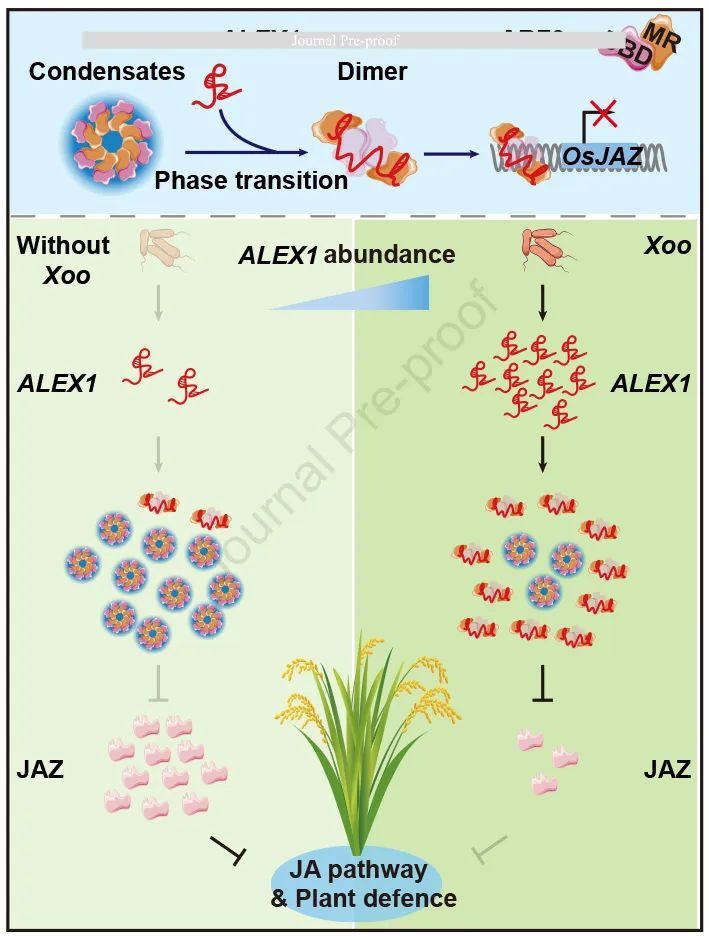
Fig2. ALEX1-ARF3模块在X. oryzae pv. Oryzae (Xoo)抗性下的工作模型
5-methylcytosine methylation of MALAT1 promotes resistance to sorafenib in hepatocellular carcinoma through ELAVL1/SLC7A11-mediated ferroptosis
MALAT1的5-甲基胞嘧啶甲基化通过ELAVL1/SLC7A11介导的铁死亡促进肝细胞癌对索拉非尼的耐药性
发表期刊:Drug Resist Updat
影响因子:15.8
发表时间:2024年12月4日
新出现的证据表明,长链非编码RNA(lncRNA)在肝细胞癌(HCC)索拉非尼耐药中起关键作用,而lncRNA转移相关肺腺癌转录本1(MALAT1)是索拉非尼耐药HCC细胞中失调的lncRNA。然而,MALAT1在索拉非尼耐药HCC细胞中的潜在调节机制仍不清楚。本研究证明了NSUN2和ALYREF催化的5-甲基胞嘧啶(m5C)甲基化有助于MALAT1的RNA稳定性和上调。NSUN2/ALYREF/MALAT1信号轴在索拉非尼耐药细胞中被激活,MALAT1的上调抑制索拉非尼诱导的铁死亡以驱动索拉非尼耐药。机制上,MALAT1通过直接结合ELAVL1并刺激其细胞质易位来维持SLC7A11的mRNA稳定性。此外,研究人员通过将MALAT1抑制剂MALAT1-IN1与索拉非尼联合使用,探索了一种治疗HCC的新协同策略。结果表明,MALAT1-IN1在体外和体内均显著增强了索拉非尼治疗HCC的疗效。总的来说,本研究结果为索拉非尼耐药的表观遗传机制带来了新的见解,并为索拉非尼耐药的HCC患者提供了一种针对铁死亡的替代治疗策略。
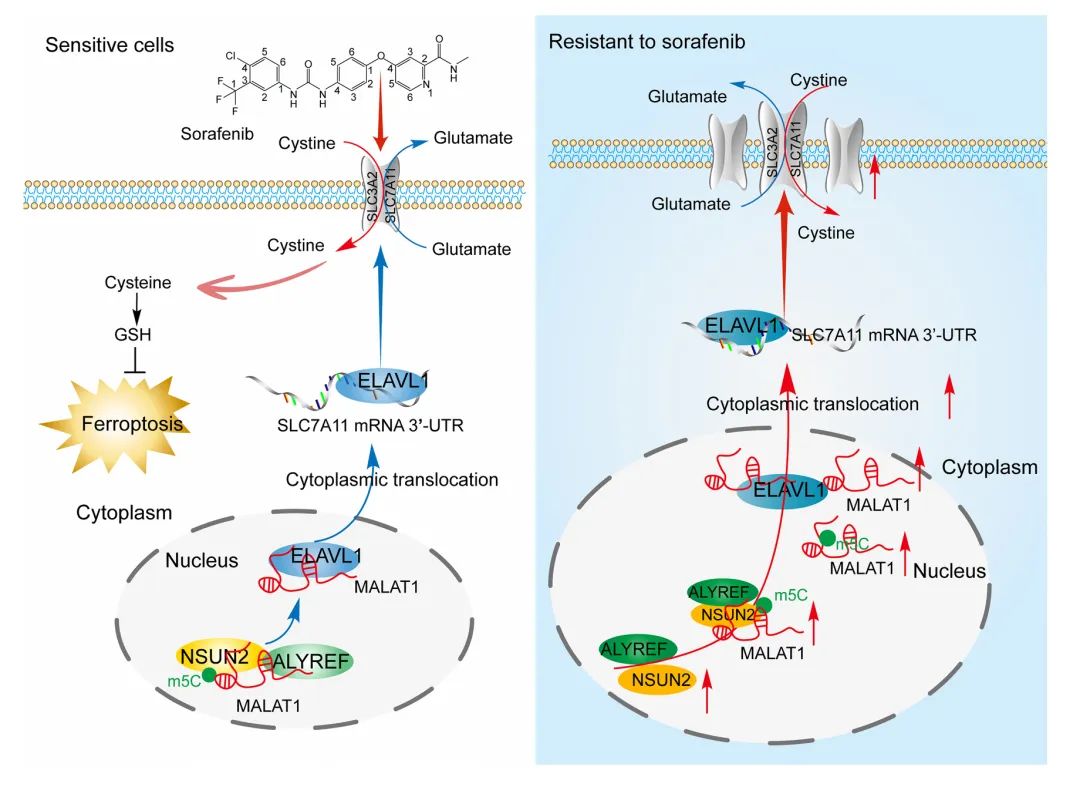
Fig3. MALAT1介导的HCC细胞索拉非尼耐药工作模型
X-linked deletion of Crossfirre, Firre, and Dxz4 in vivo uncovers diverse phenotypes and combinatorial effects on autosomes
Crossfire、Firre和Dxz4在体内的X连锁缺失揭示了常染色体上的多种表型和组合效应
发表期刊:Nat Commun
影响因子:14.7
发表时间:2024年12月5日
lncRNA Crossfirre被鉴定为印记X连锁基因,并且与反式作用lncRNA Firre进行反义转录。Firre位点与Dxz4形成无活性的X特异性相互作用,这两个位点都为最大的保守染色质结构提供了平台。本研究表征了这些基因座的表观遗传图谱,揭示了它们是全基因组范围内最具女性特异性的可及区域。为了探索它们的体内作用,本研究通过单独和组合删除 Crossfirre、Firre和Dxz4,进行了一项最大的X连锁敲除研究。尽管在X染色体上观察到它们独特的表观遗传特征,但等位基因特异性分析发现这些基因座对于印记和随机X染色体失活是非必要的。然而,本研究提供的证据表明Crossfirre影响常染色体基因调控,但仅与Firre联合使用。为了阐明这些性别特异性位点的功能作用,研究人员进行了广泛的标准化表型分析管道,并发现了不同的敲除和性别特异性表型。总的来说,本研究为探索体内保守的X连锁基因座的复杂相互作用提供了基础。
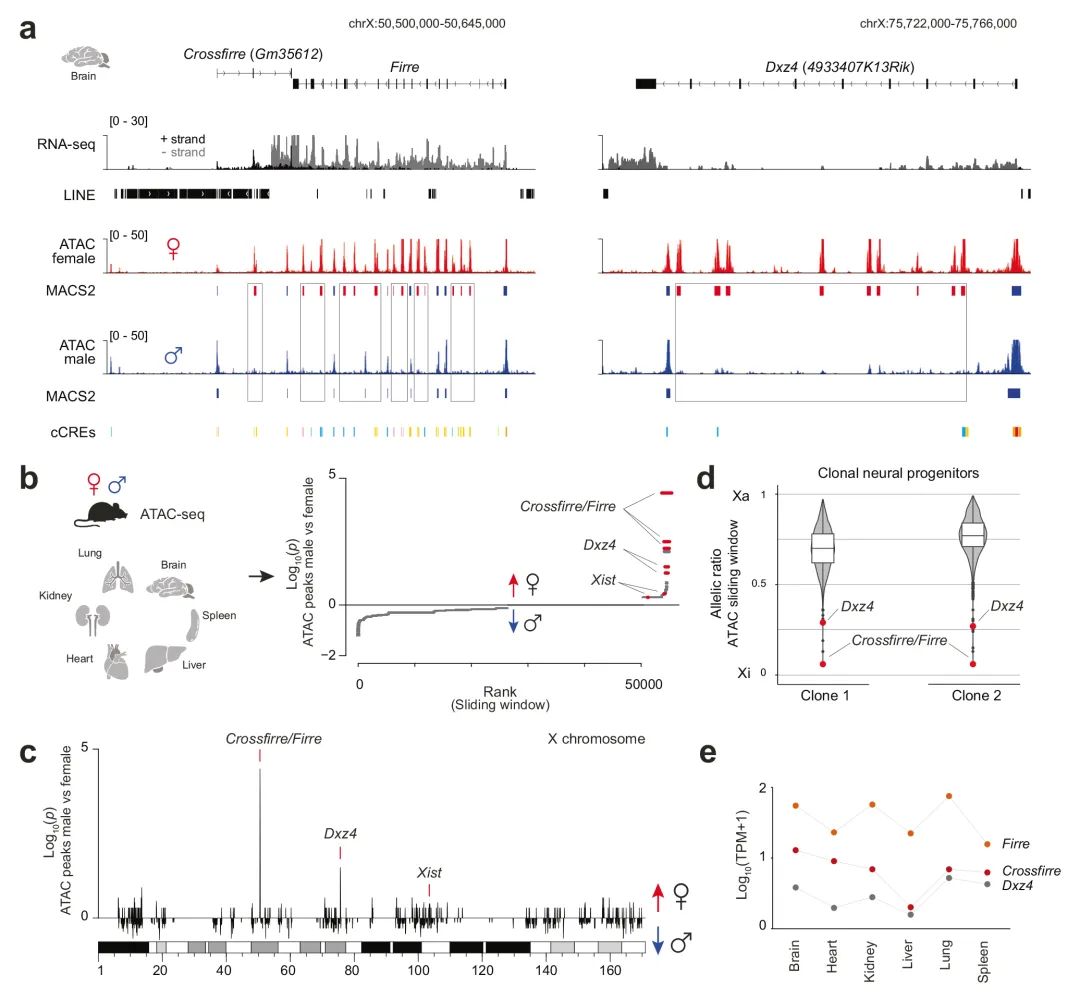
Fig4. Crossfirre、Firre和Dxz4位点是染色质可及性最靠前的女性特异性位点,具有独特的等位基因特异性特征
Hypoxia Induced Lnc191 Upregulation Dictates the Progression of Esophageal Squamous Cell Carcinoma by Activating GRP78/ERK Pathway
缺氧诱导的Lnc191上调通过激活 GRP78/ERK 通路决定食管鳞状细胞癌的进展
发表期刊:Adv Sci (Weinh)
影响因子:14.3
发表时间:2024年12月4日
缺氧是实体瘤的典型标志,在食管鳞状细胞癌(ESCC)的进展中起着至关重要的作用。然而,缺氧参与肿瘤发展的确切机制仍不清楚。本研究首先鉴定了一种新型缺氧诱导的长链非编码RNA(lncRNA)lnc191,它在临床ESCC组织中高表达,并与ESCC患者的不良预后呈正相关。这些发现证明缺氧诱导因子-1α(HIF-1α)介导的lnc191转录激活在体外和体内均增强了ESCC细胞的生长和转移。机制上,lnc191与内质网伴侣蛋白之一GRP78(78-kDa葡萄糖调节蛋白)相互作用,导致其易位到膜上,GRP78与EGFR结合并增强其磷酸化(Y845),进一步激活ERK/MAPK信号通路,从而有利于ESCC的进展。总体而言,这些数据表明lnc191是ESCC发展过程中的关键驱动因素,并揭示了激活的GRP78/ERK/MAPK轴参与lnc191介导的ESCC进展。这些发现表明lnc191作为ESCC中有前途的诊断生物标志物和治疗靶点的潜力。
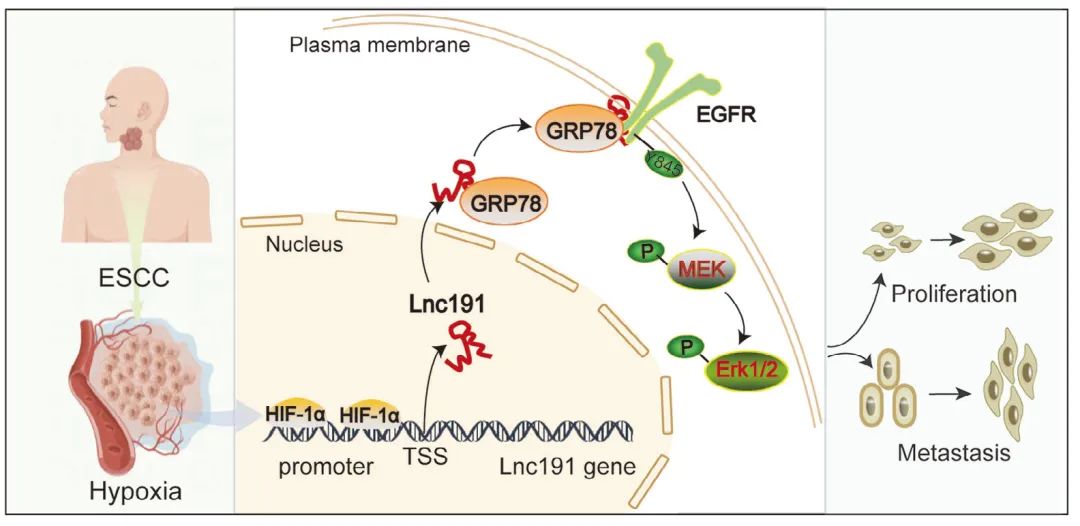
Fig5. HIF-1α/Lnc191/GRP78/p-ERK轴调控ESCC进展的模型