推荐产品
公司新闻/正文
miRNA研究进展盘点丨20240425期
人阅读 发布时间:2024-04-25 10:31
01
tRNA-derived small RNAs in human cancers: roles, mechanisms, and clinical application
tRNA来源的小RNAs在人类癌症中的作用、机制和临床应用
发表期刊:Molecular Cancer
影响因子:37.3
发表时间:2024年4月15日
转运RNA(tRNA)来源的小RNAs(tsRNAs)是一种由前体或成熟tRNAs特异性切割产生的新型非编码RNAs(ncRNAs)。tsRNAs参与表观遗传、转录、转录后、翻译调控等各种基本生物学过程,从而影响包括癌症在内的各种人类疾病的发生发展。最近的研究表明,tsRNAs通过调节恶性增殖、侵袭和转移、血管生成、免疫应答、肿瘤耐药和肿瘤代谢重编程等生物学行为,在肿瘤发生中发挥重要作用。这些可能是肿瘤治疗的新潜在靶点。此外,tsRNA可以以游离或被包裹的细胞外囊泡的形式大量稳定地存在于各种体液(如血液、血清和尿液)中,从而影响肿瘤微环境(TME)中的细胞间通讯。同时,其异常表达与肿瘤患者的临床病理特征密切相关,如肿瘤分期、淋巴结转移、肿瘤患者预后不良等;因此,tsRNAs可以作为一种新型的液体活检生物标志物。本文综述了tsRNAs的发现、产生和表达,分析了tsRNAs在肿瘤发展中的分子机制及其在肿瘤治疗中的潜在应用,为肿瘤的早期诊断和靶向治疗提供新的策略。
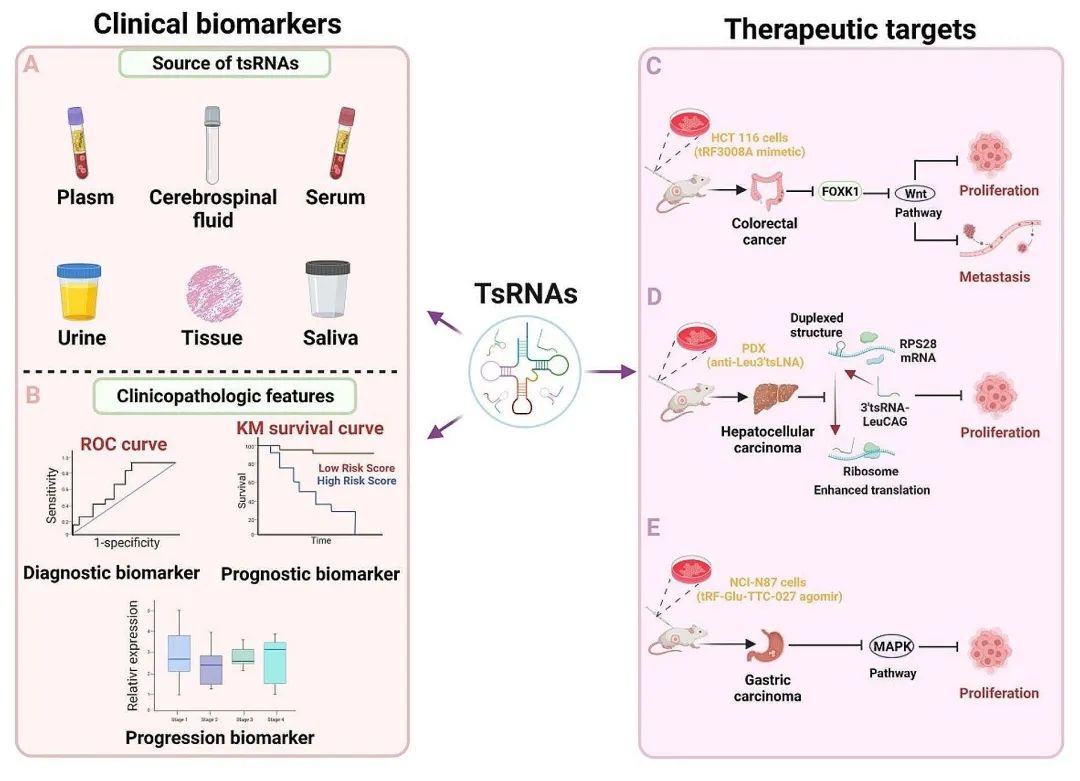
Fig1. tsRNAs作为肿瘤诊断生物标志物和治疗靶点的临床应用
原文链接:
https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-024-01992-2
02
Mimicking bacterial infection in male mice changes sperm small RNA profiles and multigenerationally alters offspring behavior and physiology
在雄性小鼠中模拟细菌感染会改变精子小RNA表达谱,并在多代之间改变后代的行为和生理机能
发表期刊:Brain Behav Immun
影响因子:15.1
发表时间:2024年4月16日
据报道,父本的孕前暴露,包括压力、饮食、药物滥用、寄生虫感染和通过Poly I:C激活的病毒免疫,会通过精子表观遗传变化影响后代的大脑和行为。然而,父本(F0)孕前暴露于细菌诱导的免疫激活对F1和F2代的行为和生理的影响仍未被探索。本研究使用C57BL / 6J小鼠对此进行了检查。8周龄雄性(F0)在注射后4周与naïve雌性交配之前,接受单次腹膜内注射细菌模拟脂多糖(LPS:5 mg/kg)或0.9%生理盐水(载体对照)。对8至14周龄范围内F1和F2代的焦虑、社交行为、抑郁样行为和认知进行了全面的行为评估。结果表明,只有暴露于LPS的父本的雌性后代在光/暗箱、大空地和新奇抑制喂养测试中表现出焦虑水平降低。这些F1雌性后代在三室社交互动测试中也表现出更高的社交能力,在糖精偏好测试中对糖精的偏好降低。此外,LPS胁迫雄性的F1雄性后代在光/暗箱中行走的总距离增加,在光区行走的距离更长。在三室社会互动测试中,它们对社会新奇事物的偏好也减弱,在Y迷宫中,它们对新颖性的偏好指数也升高。在F2代中,LPS处理父本的雄性后代在新奇抑制喂养测试中表现出减少的喂养潜伏期。此外,在急性LPS免疫刺激(5 mg/kg)后,LPS刺激父本的F2代,而不是F1代,在两性中都表现出增强的免疫应答。对来自LPS处理的F0小鼠的精子小非编码RNA表达谱的分析显示,在给药LPS后4周发生显著变化。这些变化包括3个microRNAs、8个PIWI相互作用RNAs和2个转运RNAs,表现出显著的上调(mmu-miR-146a-5p、mmu-piR-27082和mmu-piR-29102)或下调(mmu-miR-5110、mmu-miR-467e-3p、mmu-piR-22583、mmu-piR-23548、mmu-piR-36341、mmu-piR-50293、mmu-piR-16583、mmu-piR-36507、Mus_musculus_tRNA-Ile-AAT-2-1和Mus_musculus_tRNA-Tyr-GTA-1-1)。此外,在LPS处理的雄性F1后代的精子中检测到52个上调的小非编码RNAs(包括9个miRNAs、41个piRNAs和2个tRNAs)和7个下调的小非编码RNAs(3个miRNAs、3个piRNAs和1个tRNA)。这些发现提供了令人信服的证据,表明表观遗传机制参与调节大脑功能和免疫力以及相关的行为和免疫学特征,以应对细菌感染。
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38636562/
03
Toxicodynamic of combined mycotoxins: MicroRNAs and acute-phase proteins as diagnostic biomarkers
联合霉菌毒素的毒理动力学:MicroRNAs和急性期蛋白作为诊断生物标志物
发表期刊:Compr Rev Food Sci Food Saf
影响因子:14.8
发表时间:2024年4月17日
霉菌毒素是食品中普遍存在的污染物,对人类健康和福祉构成全球性威胁。缓解措施,如实施健全的农业实践、彻底的食品加工和霉菌毒素控制技术的进步,有助于减少霉菌毒素暴露和相关毒性。为了全面评估霉菌毒素及其毒理动力学影响,必须部署有效的预测性的策略。此外,了解霉菌毒素的作用方式、转化和累积毒性作用,还可以通过细胞和分子水平的基因表达和转录组分析来收集它们与食物基质的相互作用。MicroRNAs(miRNAs)控制在生理、病理和毒理学反应中起关键作用的靶基因和酶的表达,而急性期蛋白(APPs)通过内源性和转录后调控治疗剂的代谢。因此,本综述旨在巩固目前关于miRNAs在霉菌毒素引发的毒理学途径中的调节作用的知识,并探讨APPs作为霉菌毒素暴露后生物标志物的潜力。这项研究的结果强调了miRNAs和APPs作为通过生物过程检测和管理食品中霉菌毒素的指标的潜在效用。这些标志物为提高食品的安全性和质量提供了有希望的途径。
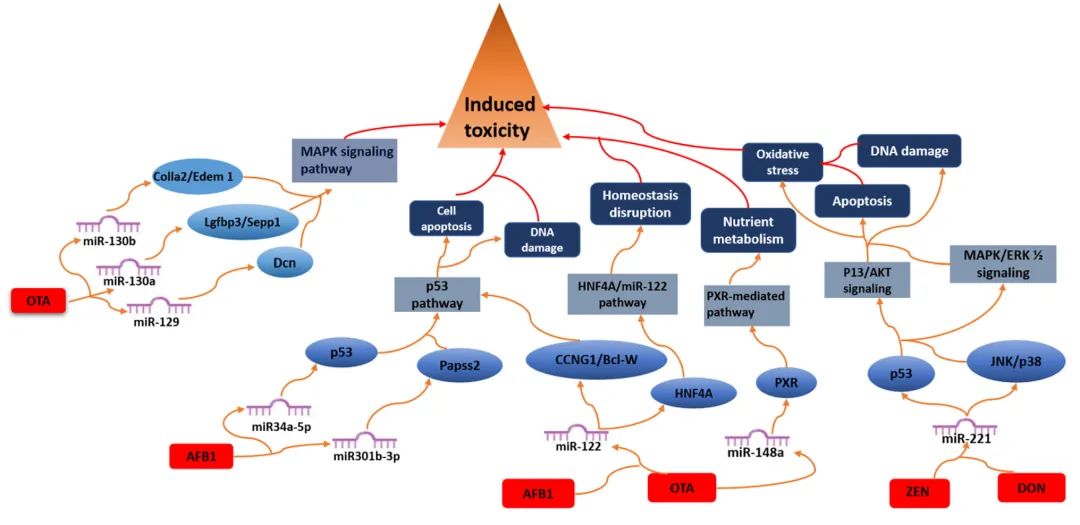
Fig2. MicroRNAs(MiRNAs)介导的调控机制和霉菌毒素诱导的毒性
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38629461/
04
Exosomal miR-9-5p derived from iPSC-MSCs ameliorates doxorubicin-induced cardiomyopathy by inhibiting cardiomyocyte senescence
来源于iPSC-MSCs的外泌体miR-9-5p通过抑制心肌细胞衰老来改善多柔比星诱导的心肌病
发表期刊:Journal of Nanobiotechnology
影响因子:10.2
发表时间:2024年4月20日
阿霉素(DOX)是一种广泛用于肿瘤治疗的化疗药物。然而,其临床应用仍受到其心脏毒性的严重限制。越来越多的证据表明,间充质干细胞来源的外泌体(MSC-EXOs)移植可以预防Dox诱导的心肌病(DIC)。本研究旨在探讨从人诱导多能干细胞来源的间充质干细胞(iPSC-MSCs)中分离的EXOs对DIC的心脏保护作用,并探讨其潜在机制。通过超速离心从人BM-MSCs(BM-MSC-EXOs)和iPSC-MSCs(iPSC-MSC-EXOs)的培养上清液中分离EXOs。通过腹腔注射Dox,然后尾静脉注射PBS、BM-MSC-EXOs或iPSC-MSC-EXOs来诱导DIC小鼠模型。评估每组小鼠的心脏功能、心肌细胞衰老和线粒体动力学。在体外,对新生小鼠心肌细胞(NMCMs)进行Dox,并用BM-MSC-EXOs或iPSC-MSC-EXOs处理。分别采用Mitotracker染色和衰老相关β-半乳糖苷酶测定法检测NMCMs的线粒体形态和细胞衰老情况。结果发现,与BM-MSC-EXOs相比,用iPSC-MSC-EXOs治疗的小鼠表现出心脏功能的改善,心肌细胞线粒体碎片化和衰老减少。在体外,iPSC-MSC-EXOs对DOX引起的心肌细胞线粒体碎裂和衰老的抑制作用优于BM-MSC-EXOs。MicroRNA测序显示iPSC-MSC-EXO中的miR-9-5p水平高于BM-MSC-EXO。机制上,iPSC-MSC-EXOs将miR-9-5p转运到DOX处理的心肌细胞中,从而通过调节VPO1/ERK信号通路抑制心肌细胞线粒体碎片化和衰老。这些针对DIC的保护作用和心脏保护在很大程度上被iPSC-MSC-EXO中miR-9-5p的敲低所逆转。本研究结果表明,iPSC-MSC-EXOs转移的miR-9-5p通过抑制VPO1/ERK通路缓解心肌细胞衰老来保护DIC免受DIC的影响。本研究为iPSC-MSC-EXOs作为DIC治疗新疗法的应用提供了新的见解。
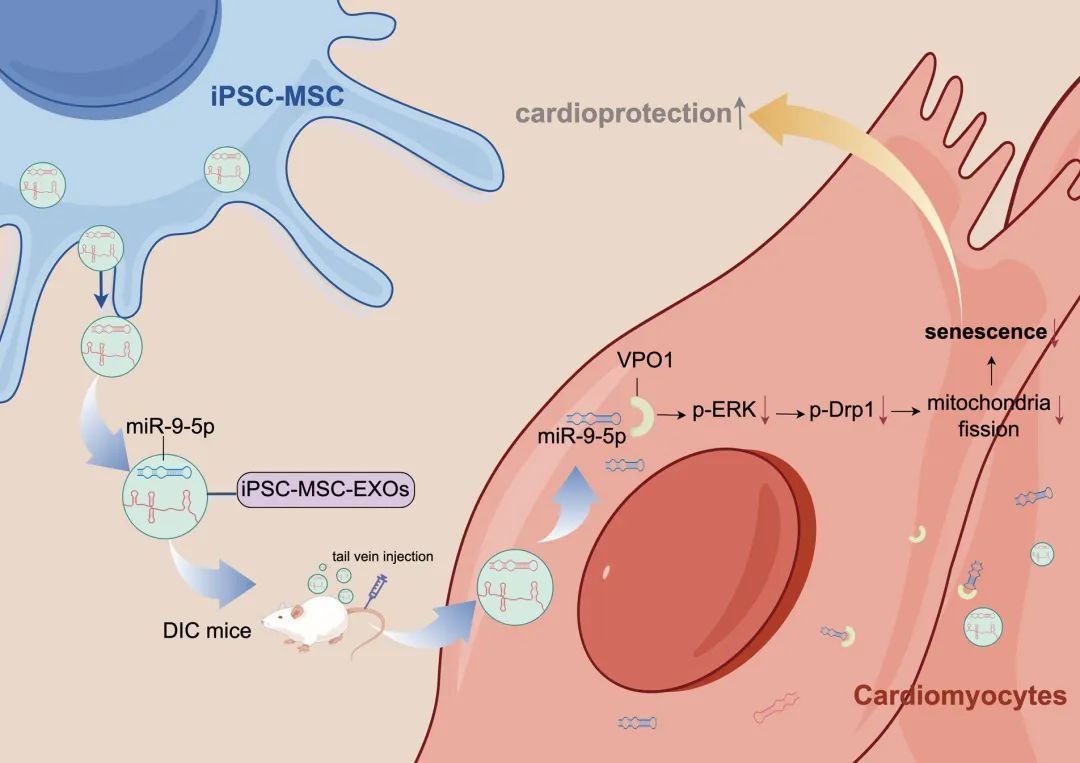
Fig3. 研究模型示意图
原文链接:
https://jnanobiotechnology.biomedcentral.com/articles/10.1186/s12951-024-02421-8
05
Increased levels of villus-derived exosomal miR-29a-3p in normal pregnancy than uRPL patients suppresses decidual NK cell production of interferon-γ and exerts a therapeutic effect in abortion-prone mice
与uRPL患者相比,正常妊娠的绒毛源性外泌体miR-29a-3p水平升高,可抑制蜕膜NK细胞产生干扰素-γ,并在易流产小鼠中发挥治疗作用
发表期刊:Cell Commun Signal
影响因子:8.4
发表时间:2024年4月16日
目的:复发性流产(RPL)患者蜕膜自然杀伤(dNK)细胞绝对数量较高,细胞内IFN-γ水平升高,导致促炎细胞因子环境,从而促进RPL的发病。本研究的主要目的有两个:首先探讨诱发性流产患者或RPL患者绒毛源性外泌体(vEXOs)在dNK细胞细胞内IFN-γ水平上的调控作用和机制;其次,通过体外实验和小鼠模型确定vEXOs在治疗不明原因RPL(uRPL)中的有效性。
结果:uRPL患者dNK细胞的IFN-γ水平显著高于IA患者。uRPL-vEXOs和IA-vEXOs都可以被dNK细胞有效地内化,而uRPL-vEXOs不能像IA-vEXOs那样降低dNK细胞对IFN-γ的表达。机制上,miR-29a-3p通过vEXOs递送,通过与dNK细胞中IFN-γ mRNA的3' UTR结合来抑制IFN-γ的产生。对于体内治疗,HA-Gel的应用通过持续释放有效地延长了vEXOs在子宫腔中的停留时间。负载miR-29a-3p的工程化vEXOs降低了RPL小鼠的胚胎吸收率,没有全身毒性迹象。
结论:本研究证明绒毛可以通过外泌体介导的miR-29a-3p转移来调节dNK细胞产生IFN-γ,这加深了我们对母胎免疫耐受性维持妊娠的理解。基于此,本研究开发了一种将工程vEXOs与HA-Gel混合的新策略,该策略在uRPL小鼠中表现出良好的治疗效果,可用于uRPL治疗的潜在临床应用。
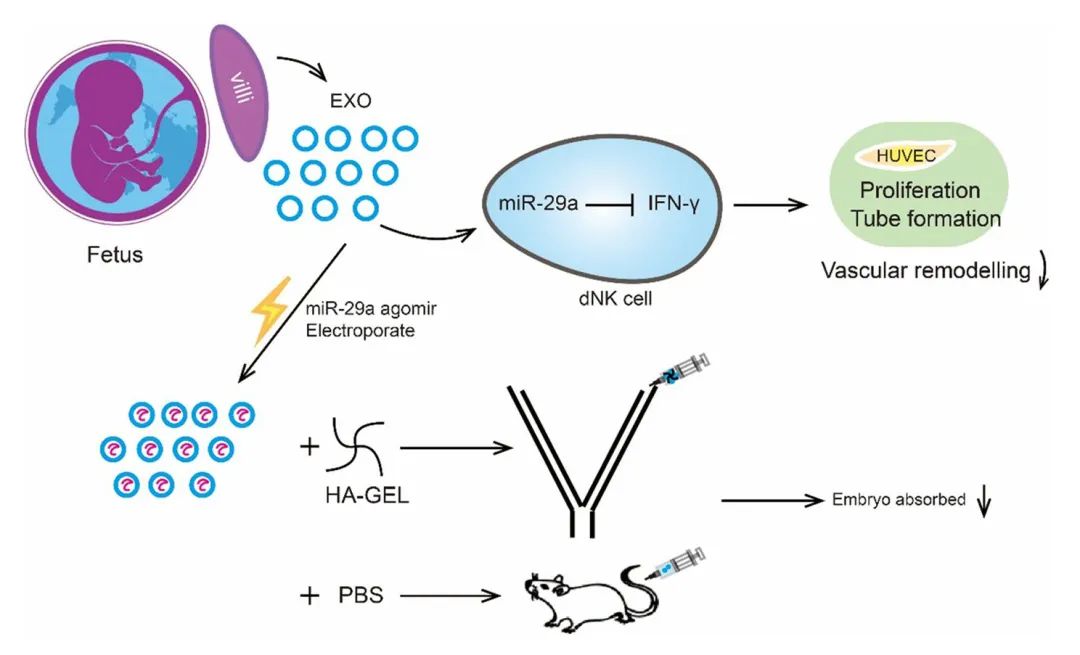
Fig4. 研究模型示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38627796/










