广州市锐博生物科技有限公司品牌商
18 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
推荐产品
公司新闻/正文
lncRNA研究进展盘点丨20240415期
489 人阅读发布时间:2024-04-25 10:00
01
Loss of lncRNA LINC01056 leads to sorafenib resistance in HCC
lncRNA LINC01056的缺失导致HCC患者索拉非尼耐药
发表期刊:Mol Cancer
影响因子:37.3
发表时间:2024年4月6日
背景和目的:索拉非尼是晚期肝细胞癌(HCC)患者的主要非手术选择;然而,其临床疗效在很大程度上受到耐药性的影响。本研究的目的是确定参与调节HCC中索拉非尼反应的关键lncRNA。
结果:CRISPR/Cas9 lncRNA文库筛选显示,Linc01056是索拉非尼耐药HCC细胞中下调最严重的lncRNA之一。敲低Linc01056降低了HCC细胞对索拉非尼的敏感性,抑制了体外细胞凋亡,并促进了小鼠体内的肿瘤生长。蛋白质组学分析显示,在索拉非尼处理的HCC细胞中,Linc01056敲低诱导了与脂肪酸氧化(FAO)相关基因的表达,同时抑制了糖酵解相关基因表达,导致有利于更高细胞内能量产生的代谢开关。敲低Linc01056对HCC细胞的FAO抑制显著恢复了对索拉非尼的敏感性。机制上,本研究确定了PPARα是控制HCC细胞中Linc01056敲低时代谢开关的关键分子,并且PPARα抑制确实恢复了体外HCC细胞和体内HCC肿瘤中的索拉非尼反应。临床上,Linc01056表达预测了HCC患者的最佳总生存期和无进展生存期预后,并预测了更好的索拉非尼反应。Linc01056表达表明HCC中的FAO水平较低。
结论:本研究将Linc01056确定为调控HCC索拉非尼反应的关键表观遗传调控因子和潜在治疗靶点。
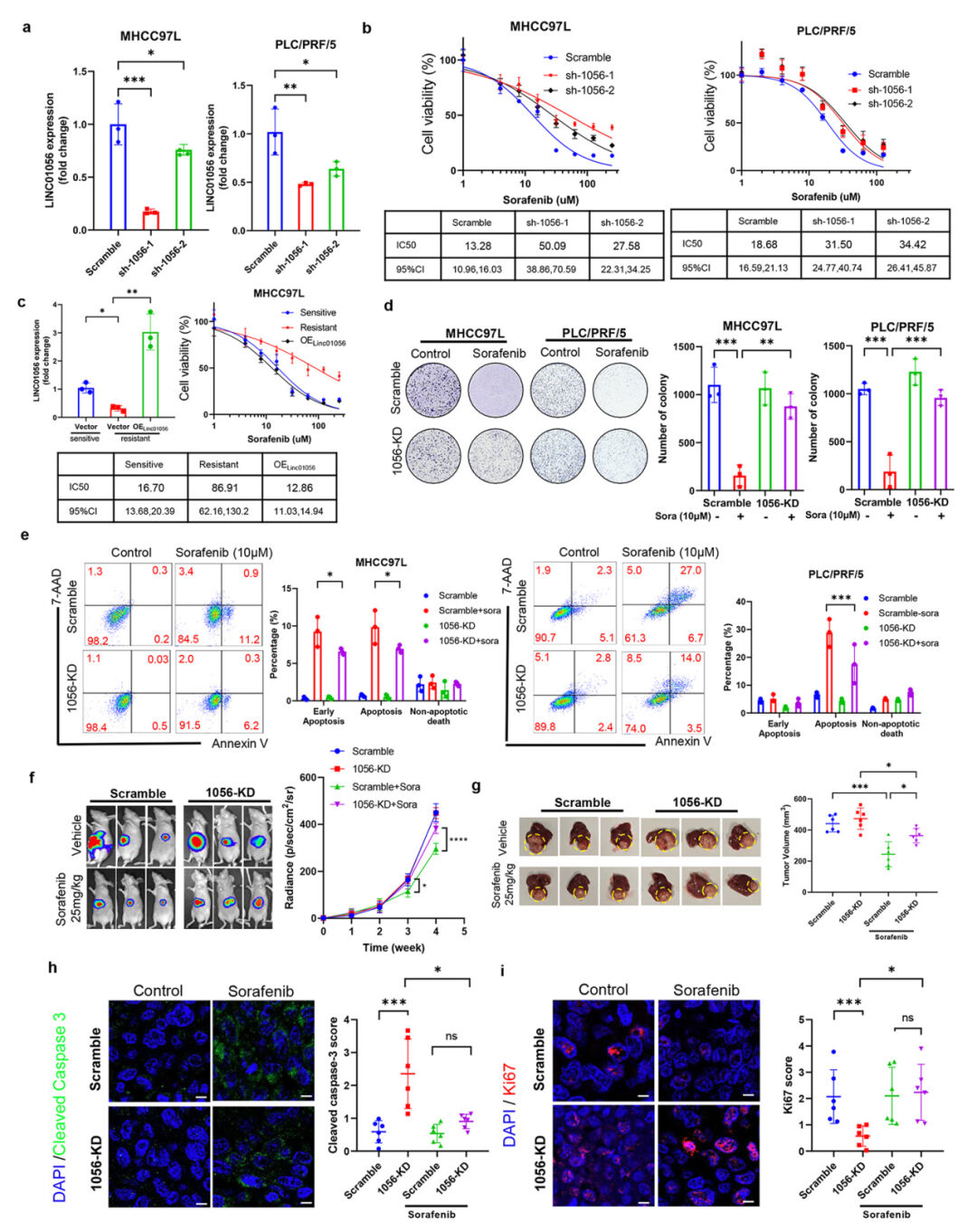
Fig1. Linc01056是HCC中索拉非尼反应所必需的
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38582885/
02
CodLncScape Provides a Self-Enriching Framework for the Systematic Collection and Exploration of Coding LncRNAs
CodLncScape为编码LncRNAs的系统收集和探索提供了一个自富集框架
发表期刊:Adv Sci
影响因子:15.1
发表时间:2024年4月11日
最近的研究表明,许多lncRNAs可以在特定条件下翻译蛋白质,执行不同的生物学功能,因此称为编码lncRNAs。然而,由于该领域的初步和分散性质,它们的全面景观仍然不清楚。本研究介绍了codLncScape,这是一个由codLncDB、codLncFlow、codLncWeb和codLncNLP组成的,用于编码lncRNA探索的框架。具体来说,它包含一个人工编译的知识库codLncDB,包含353个通过实验验证的编码lncRNA条目。在codLncDB的基础上,codLncFlow研究了这些lncRNAs的表达特征及其在泛癌背景下的诊断潜力,以及它们与精子发生的关联。此外,codLncWeb成为在各种编程环境中存储、浏览和访问有关编码lncRNAs的知识的平台。最后,codLncNLP作为一种知识挖掘工具,增强了codLncDB中内容的及时包含和更新。综上所述,本研究为lncRNA编码研究提供了一个功能完善、内容丰富的生态系统,旨在加速该领域的系统研究。
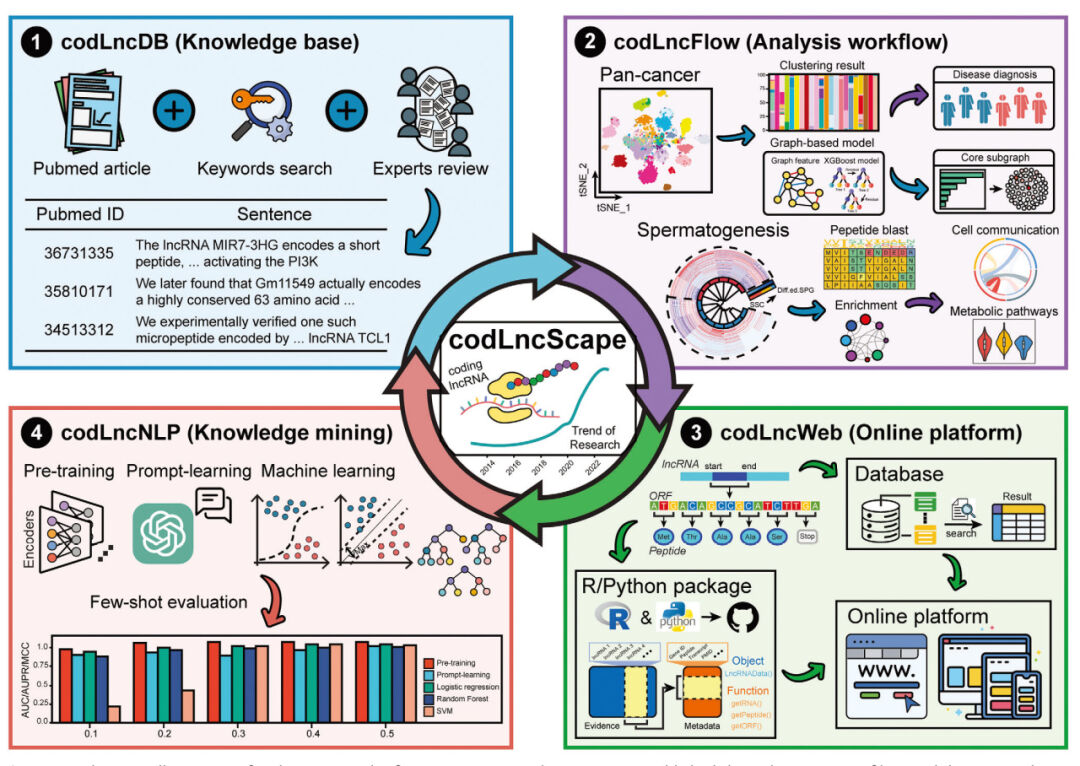
Fig2. CodLncScape示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38602457/
03
The long non-coding RNA Meg3 mediates imprinted gene expression during stem cell differentiation
长链非编码RNA Meg3介导干细胞分化过程中的印迹基因表达
发表期刊:Nucleic Acids Res
影响因子:14.9
发表时间:2024年4月13日
印迹的Dlk1-Dio3结构域包括发育基因Dlk1和Rtl1,它们在不同细胞类型的母体染色体上沉默。在亲本染色体上,该结构域的印记控制区激活一个多顺子,产生lncRNA Meg3和许多miRNA(Mirg)和C/D-box snoRNA(Rian)。尽管Meg3 lncRNA是细胞核定位,并与母体染色体相关,但尚不清楚它是否控制顺式中的基因抑制。本研究创造了携带异位poly(A)信号的小鼠胚胎干细胞(mESC),降低了多顺反子上的RNA水平,并产生了Rian-/-mESC。在ESC分化后,本研究发现Meg3 lncRNA(但不是Rian)是母体染色体上Dlk1抑制所必需的。通过CRISPR介导的父系Meg3启动子去甲基化获得的双等位基因Meg3表达导致双等位基因Dlk1抑制和Rtl1表达缺失。lncRNA表达还与Meg3 5'端的DNA低甲基化和CTCF结合相关。使用Capture Hi-C,研究人员发现这创建了一个拓扑相关结构域(TAD)组织,使Meg3接近母体染色体上的Dlk1。Meg3对基因抑制和TAD结构的需求可以解释人类DLK1-DIO3位点的异常MEG3表达如何与印记障碍相关。
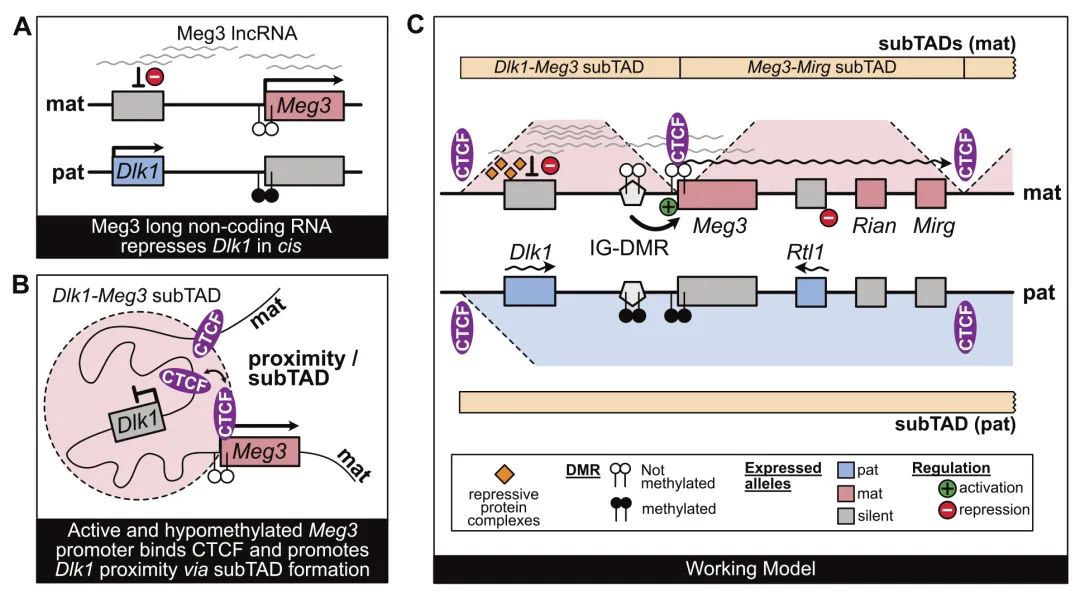
Fig3. Meg3 lncRNA表达如何控制印记基因表达的模型
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38613389/
04
Conserved long noncoding RNA TILAM promotes liver fibrosis through interaction with PML in hepatic stellate cells
保守的长链非编码RNA TILAM通过与肝星状细胞中的PML相互作用促进肝纤维化
发表期刊:Hepatology
影响因子:13.5
发表时间:2024年4月2日
背景和目的:纤维化是所有形式的慢性肝损伤的共同终点,纤维化的进展导致终末期肝病的发展。肝星状细胞(HSCs)的激活及其转分化为肌成纤维细胞会导致细胞外基质(ECM)蛋白的积累,形成纤维化瘢痕。长链非编码(lnc)RNAs调节HSCs的活性并为纤维化治疗提供靶标。
方法和结果:本研究鉴定了位于COL1A1附近的lncRNA TILAM,其在HSCs中表达,并在人和小鼠中诱导肝纤维化。人类造血干细胞和人类肝脏类器官的功能缺失研究表明,TILAM 调节COL1A1和其他ECM基因的表达。为了确定TILAM在体内的作用,研究人员注释了小鼠直系同源物(Tilam),生成了Tilam缺陷的GFP报告小鼠,并在两种不同的肝纤维化模型中刺激这些小鼠。单细胞数据和对Tilam缺陷报告小鼠的GFP表达分析显示,Tilam在小鼠HSCs中被诱导,并在体内发生纤维化。此外,在体内肝损伤的情况下,Tilam表达的缺失减轻了纤维化的发展。最后,本研究发现TILAM与PML相互作用调节一个反馈回路,TGF-β2通过该回路增强TILAM的表达和PML的核定位,从而促进HSCs的纤维化活性。
结论:TILAM在肝损伤造血干细胞中被激活,并与PML相互作用以驱动纤维化的发展。TILAM的缺失可作为对抗终末期肝病发展的治疗方法。
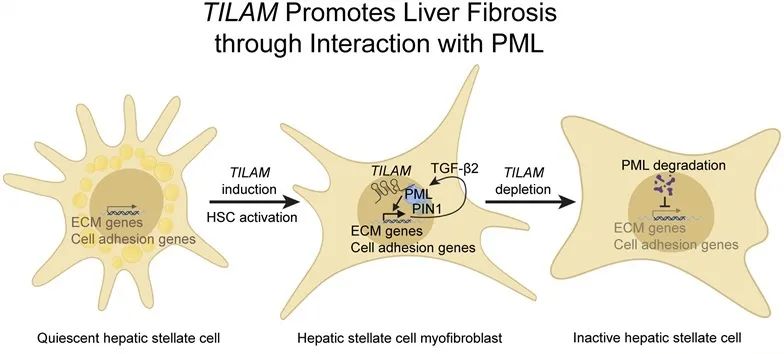
Fig4. 研究模型示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38563629/
05
MILIP Binding to tRNAs Promotes Protein Synthesis to Drive Triple-Negative Breast Cancer
MILIP与tRNAs结合促进蛋白质合成以驱动三阴性乳腺癌
发表期刊:Cancer Res
影响因子:11.2
发表时间:2024年4月9日
三阴性乳腺癌(TNBC)患者由于缺乏有效的治疗干预分子靶点,预后较差。本研究发现长链非编码RNA(lncRNA)MILIP通过与转运RNAs(tRNAs)络合以促进蛋白质产生来支持TNBC细胞存活、增殖和致瘤性,从而代表了TNBC的潜在治疗靶点。MILIP在通常携带肿瘤抑制因子p53功能缺失突变的TNBC细胞中高水平表达,MILIP沉默抑制了TNBC细胞活力和异种移植物生长,表明MILIP在TNBC中的功能独特,超出了其在其他类型癌症中抑制p53的既定作用。机制研究表明,MILIP与真核翻译延伸因子1α1(eEF1α1)相互作用,并通过其可变环与II型tRNAs tRNALeu和tRNASer形成RNA-RNA双链体,促进eEF1α1与这些tRNAs的结合。破坏MILIP和eEF1α1或tRNAs之间的相互作用会降低蛋白质合成和细胞活力。靶向MILIP抑制TNBC生长,并与在体内与临床上可用的蛋白质合成抑制剂omacetaxine mepesuccinate(INN)协作。总的来说,这些结果将MILIP确定为促进TNBC细胞中蛋白质产生的RNA翻译延伸因子,并揭示了靶向MILIP单独或与其他类型的蛋白质合成抑制剂联合用于TNBC治疗的治疗潜力。
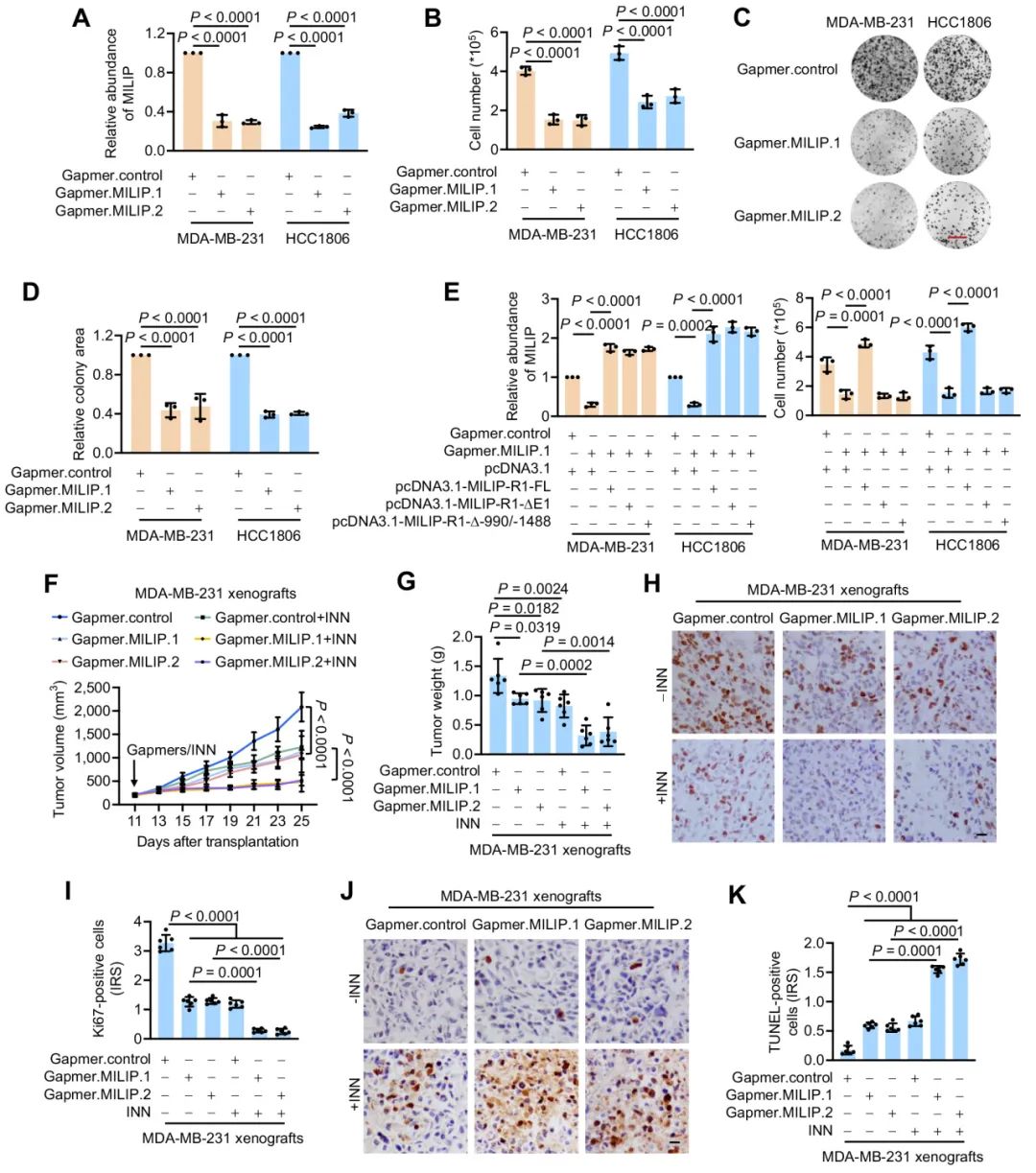
Fig5. MILIP Gapmers抑制并与INN协作抑制TNBC异种移植物的生长
原文链接:
https://pubmed.ncbi.nlm.nih.gov/38593213/