推荐产品
公司新闻/正文
lncRNA研究进展盘点丨20230718期
人阅读 发布时间:2023-07-19 14:25
01
lncRNA RMST的治疗性沉默可缓解小鼠和猪心肌梗死后的心脏纤维化并改善心脏功能发表期刊:Theranostics
影响因子:12.4
发表时间:2023年7月11日
背景:心脏纤维化是心肌梗死(MI)后成纤维细胞活化异常和细胞外基质(ECM)沉积的不良后果。最近,长链非编码RNAs(lncRNAs)被报道参与多种心脏疾病。然而,lncRNA RMST(横纹肌肉瘤2相关转录本)在心脏纤维化中的生物学功能在很大程度上仍然未知。
结果:本研究表明,RMST在小鼠和猪MI模型中表达上调,并与心脏纤维化相关。进一步的功能缺失研究表明,体外RMST沉默显著抑制CF(心肌成纤维细胞)增殖、FMT(成纤维细胞向肌成纤维细胞转化)和ECM的产生。相应地,体内RMST敲低减轻了MI小鼠的心脏纤维化,并改善了心脏收缩功能。此外,RMST作为miR-24-3p的竞争性内源性RNA。miR-24-3p抑制被消除,而miR-24-3p agomir则通过调节赖氨酰氧化酶信号通路再现了RMST敲低介导的对CF纤维化作用。最后,本研究在猪MI模型中评估了RMST敲低的治疗潜力,发现局部RMST敲低可显著抑制MI后猪的心肌纤维化,并改善心肌收缩功能。
结论:本研究结果将RMST确定为心脏纤维化的关键调节因子,靶向RMST可能为治疗纤维化相关心脏疾病提供一种新颖有效的治疗策略。
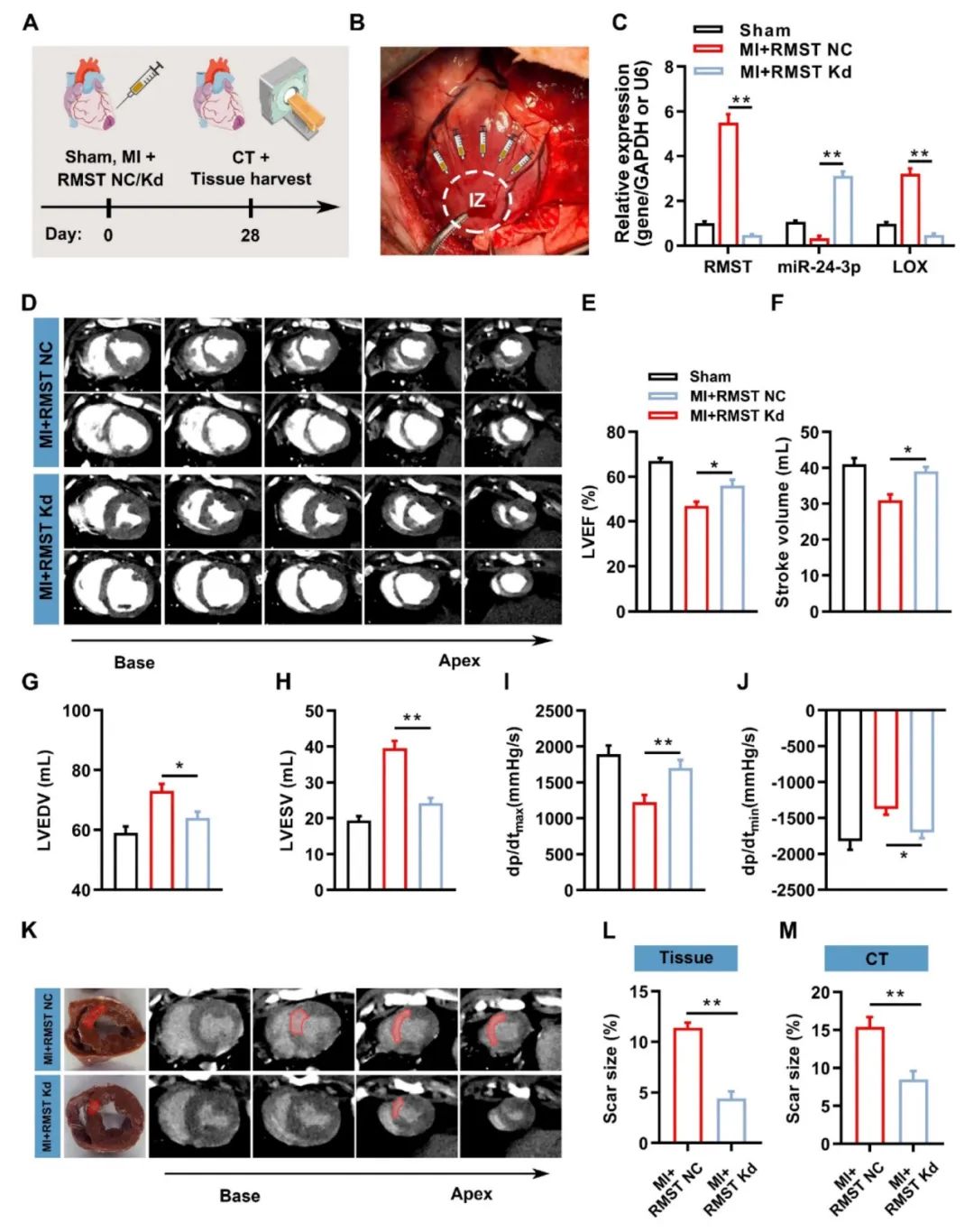
Fig1. 在猪MI模型中,RMST敲低可减轻心肌梗死面积并改善心肌功能
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37441584/
02
与糖尿病创面愈合中氧化应激相关的lncRNAs的调控机制及应用前景
发表期刊:Theranostics
影响因子:12.4
发表时间:2023年7月11日
糖尿病是一组血糖失衡的慢性疾病,长期高血糖会对机体的各个器官造成持续的损害,导致血管病变、神经病变和伤口愈合受损。糖尿病创面的形成涉及多种复杂的机制,其特征是持续的慢性炎症反应,血管生成的降解和细胞外基质调节失衡,所有这些都与氧化应激有关。此外,糖尿病创面的修复和愈合需要多种细胞、细胞因子、基因和其他因素的参与,这些因素共同构成了一个复杂的生物调控网络。最近的研究表明,长链非编码RNAs(lncRNAs)可以参与几种关键生物学途径和细胞功能的调节,这表明它们在糖尿病创面愈合中起着关键作用。LncRNAs是一个主要的RNA家族,具有有限的或没有蛋白质编码功能。许多研究最近报道了氧化应激与lncRNAs之间的密切联系。鉴于lncRNAs和氧化应激已被确定为糖尿病创面愈合的潜在驱动因素,因此可以推断它们与糖尿病创面愈合的联系。然而,氧化应激相关的lncRNAs在糖尿病创面愈合中的具体机制尚不清楚,阐明lncRNAs在这些过程中的功能仍然是一个重大挑战。本文综述了lncRNAs在糖尿病创面愈合的几个阶段中与氧化应激相关的机制,并讨论了lncRNAs通过改善氧化应激来治疗糖尿病创面的诊断和治疗潜力,以及为此目的使用lncRNAs的挑战。希望这些结果将为糖尿病患者创面愈合受损的诊断和治疗提供新的靶点和策略。

Fig2. 氧化应激相关lncRNA通路对糖尿病伤口愈合的调控作用
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37441585/
03
长链非编码RNA LINC01594抑制CELF6介导的致癌CD44变异体剪接从而促进结直肠癌转移
发表期刊:Cell Death Dis
影响因子:9.0
发表时间:2023年7月14日
长链非编码RNAs(lncRNAs)在肿瘤发生和肿瘤转移中起着关键作用。然而,lncRNAs在结直肠癌(CRC)中的潜在机制需要进一步探索。通过使用来自癌症基因组图谱(TCGA)和GEO数据库的数据,本研究发现了一种新的CRC相关lncRNA LINC01594,其在CRC中显著上调,并且与预后不良有关。体外和体内功能获得性和缺失性实验表明,LINC01594促进结直肠癌转移。LINC01594用作DNMT1支架,增加CELF6启动子甲基化水平。LINC01594还竞争性地结合转录因子p53,降低CELF6的表达。这抑制了CELF6诱导的CD44 V4-V7的外显子跳跃。综上所述,本研究重点介绍了一种新的CRC生物标志物和治疗靶点LINC01594,研究结果表明LINC01594-CELF6-CD44轴可能作为CRC的生物标志物和治疗靶点。

Fig3. LINC01594在CRC转移中的作用模型示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37452042/
04
TM4SF1-AS1通过促进癌细胞中的应激颗粒形成来抑制细胞凋亡
发表期刊:Cell Death Dis
影响因子:9.0
发表时间:2023年7月13日
长链非编码RNAs(lncRNAs)在肿瘤发展中起着关键作用。为了鉴定胃癌(GC)中失调的lncRNAs,本研究分析了组蛋白H3赖氨酸4(H3K4me3)的全基因组三甲基化,以筛选GC患者和健康个体非肿瘤性胃粘膜中的转录活性lncRNA基因。结果发现TM4SF1-AS1位点的H3K4me3在GC患者中特异性上调,并且在原代和培养的GC细胞中TM4SF1-AS1的表达显著升高。TM4SF1-AS1有助于体外和体内GC细胞生长,其致癌功能至少部分是通过与Pur-α(富含嘌呤元件结合蛋白α)和YB-1(Y-box结合蛋白1)的相互作用介导的。TM4SF1-AS1还激活GC细胞中的干扰素信号,该信号依赖于Pur-α和RIG-I。ChIRP-质谱分析表明,TM4SF1-AS1与几种应激颗粒(SG)相关蛋白有关,包括G3BP2、RACK1和DDX3。值得注意的是,TM4SF1-AS1通过在SGs中隔离RACK1(应激响应MAPK途径的激活因子)来促进SG形成并抑制GC细胞的凋亡。TM4SF1-AS1诱导的SG形成和凋亡抑制依赖于Pur-α和YB-1。这些发现表明,TM4SF1-AS1通过增强SG介导的应激适应来促进肿瘤发生。

Fig4. TM4SF1-AS1诱导的应激适应模型
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37443145/
05
转录因子TP63介导LncRNA CNTFR-AS1通过同源重组修复促进氧化钕纳米颗粒诱导的DNA损伤发表期刊:Environ Pollut
影响因子:8.9
发表时间:2023年7月12日
氧化钕纳米颗粒(NPs-Nd2O3)的广泛使用已经造成了环境污染和人类健康问题,因此引起了人们的极大关注。了解NPs-Nd2O3诱导的遗传损伤的机制,对于鉴定NPs-Nd2O3诱导肺损伤的早期标志物具有重要意义。目前,NPs-Nd2O3诱导DNA损伤的机制尚不清楚。在这项研究中,研究人员对暴露于不同浓度NPs-Nd2O3的人支气管上皮细胞(16HBEs)和单次气管内滴注NPs-Nd2O3的SD大鼠进行了功能测定。暴露于NPs-Nd2O3可导致16HBE细胞和大鼠肺组织细胞的DNA损伤。本研究发现了一种新型的长链非编码RNA,名为CNTFR-AS1,其在暴露于NPs-Nd2O3后高度表达。研究数据验证了转录因子TP63介导CNTFR-AS1的高表达水平,进而通过抑制HR修复来调节NPs-Nd2O3诱导的细胞DNA损伤。此外,CNTFR-AS1水平与职业工人的工作年数相关。总的来说,这些结果表明CNTFR-AS1在暴露于NPs-Nd2O3的支气管上皮细胞中作为一种新的DNA损伤调节因子。因此,本研究数据为鉴定lncRNA作为稀土肺损伤的早期诊断标志物提供了依据。

Fig5. 研究模型示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37451587/










