推荐产品
公司新闻/正文
lncRNA研究进展盘点丨20230524期
人阅读 发布时间:2023-07-03 10:55
01
影响因子:39.92
发表时间:2023年5月18日
背景:血管平滑肌细胞(VSMC)炎症的激活是引发血管疾病的关键。人类特异性长链非编码RNA在VSMC炎症中的作用尚不清楚。
结果:INKILN在收缩性VSMCs中表达下调,并在人动脉粥样硬化和腹主动脉瘤中诱导表达。INKILN被p65途径转录激活,部分通过其近端启动子内的预测NF-κB(核因子κB)位点。INKILN在体外培养的人VSMCs和离体培养血管中激活促炎基因表达。INKILN通过p65/NF-κB途径与MKL1(MKL1是VSMC炎症的关键激活因子)物理相互作用并稳定MKL1。INKILN缺失阻断了白细胞介素-1β诱导的p65和MKL1的核定位。敲低INKILN消除了p65和MKL1之间的物理相互作用以及NF-κB报告基因的荧光素酶活性。此外,INKILN敲低通过减少与去泛素化酶USP10(泛素特异性肽酶10)的物理相互作用来增强MKL1的泛素化。在细菌人工染色体转基因小鼠中,INKILN在受伤的颈动脉中被诱导,并加剧结扎损伤诱导的新生内膜形成。
结论:这些发现阐明了与INKILN/MKL1/USP10调控轴有关的VSMC炎症的重要途径。人细菌人工染色体转基因小鼠为在血管疾病条件下研究人类特异性长链非编码RNA提供了一种新颖且生理学相关的方法。
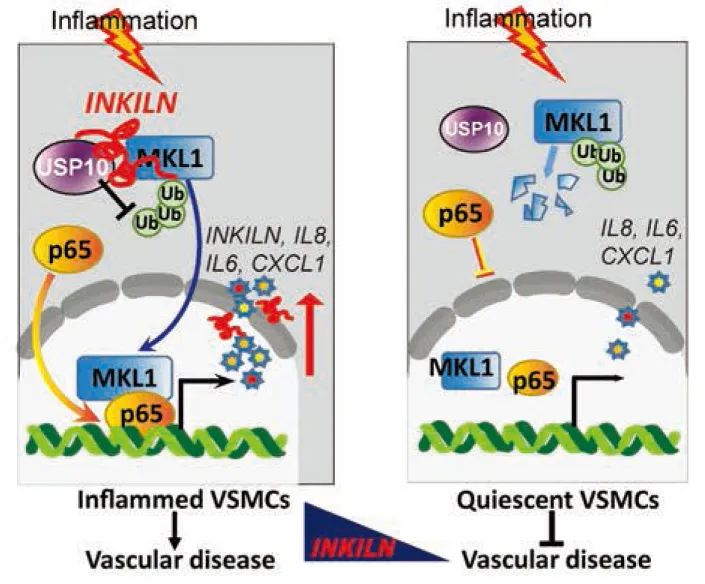
Fig1. INKILN激活血管平滑肌细胞(VSMC)炎症的工作模型
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37199168/
02
lncRNA SYTL5-OT4通过抑制ASCT2的自噬降解来促进血管选定
发表期刊:Drug Resist Updat
影响因子:22.84
发表时间:2023年5月13日
目的:在结直肠癌肝转移(CRCLM)患者中,血管选定(vessel co-option)是肿瘤对抗血管生成治疗(AATs)产生耐药性的原因。然而,血管选定的机制在很大程度上仍然未知。本研究了探索了一种新型lncRNA SYTL5-OT4和丙氨酸-丝氨酸-半胱氨酸转运蛋白2(ASCT2)在血管选定介导的AAT耐药中的作用。
结果:AAT耐药型CRCLM患者中SYTL5-OT4和ASCT2的表达较高。SYTL5-OT4通过抑制ASCT2的自噬降解来增强其表达。SYTL5-OT4和ASCT2通过增加肿瘤细胞的增殖和上皮-间充质转化来促进血管选定。ASCT2抑制剂和抗血管生成药物的联合治疗克服了CRCLM中血管选定介导的AAT耐药。
结论:本研究强调了lncRNA和谷氨酰胺代谢在血管选定中的关键作用,并为AAT耐药CRCLM患者提供了潜在的治疗策略。

Fig2. SYTL5-OT4在体内促进依赖于ASCT2的血管选定
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37207473/
03
表观遗传沉默的lncRNA SNAI3-AS1通过扰乱SND1介导的Nrf2 mRNA的m6A依赖性识别来促进胶质瘤中的铁死亡
发表期刊:J Exp Clin Cancer Res
影响因子:12.66
发表时间:2023年5月19日
背景:铁死亡与肿瘤进展和抗肿瘤治疗耐药性有关。长链非编码RNA(lncRNA)在肿瘤细胞的多种生物学过程中发挥调节作用,而lncRNA在胶质瘤铁死亡中的功能和分子机制尚待阐明。
结果:铁死亡诱导剂erastin通过增加SNAI3-AS1启动子的DNA甲基化水平下调神经胶质瘤中SNAI3-AS1的表达。SNAI3-AS1在胶质瘤中起到抑制肿瘤的作用。重要的是,SNAI3-AS1通过促进体外和体内铁死亡来增强erastin的抗肿瘤活性。在机制上,SNAI3-AS1竞争性地与SND1结合,并扰乱SND1对Nrf2 mRNA 3'UTR的m6A依赖性识别,从而降低Nrf2 mRNA的稳定性。挽救实验证实,SND1过表达和沉默可以分别挽救SNAI3-AS1的功能获得性和功能缺失性铁死亡表型。
结论:本研究结果阐明了SNAI3-AS1/SND1/Nrf2信号轴在铁死亡中的作用及详细机制,为诱导铁死亡改善胶质瘤治疗提供了理论支持。

Fig3. SNAI3-AS1/SND1/Nrf2轴调控胶质瘤细胞铁死亡示意图
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37202791/
04
上调长链非编码RNA Lnc-MRPL39-2:1通过与HuR结合并稳定β-Catenin mRNA诱导鼻咽癌的生长和侵袭
发表期刊:Int J Biol Sci
影响因子:10.75
发表时间:2023年5月25日
长链非编码RNAs(lncRNAs)一直通过各种分子机制调节肿瘤进展和治疗耐药性。本研究探讨了lncRNA在鼻咽癌(NPC)中的作用及其潜在机制。使用lncRNA阵列分析NPC和肿瘤旁组织的lncRNA表达谱,本研究检测到新的lnc-MRPL39-2:1,并通过原位杂交和cDNA末端的5'和3'快速扩增进行了验证。此外,体外和体内实验验证了其在NPC细胞生长和转移中的作用。研究人员进行了RNA pull-down实验、质谱(MS)分析、双荧光素酶报告基因实验、RNA免疫沉淀(RIP)实验,然后使用MS2-RIP分析鉴定lnc-MRPL39-2:1相互作用的蛋白质和miRNAs。研究发现在鼻咽癌组织中高表达的lnc-MRPL39-2:1与鼻咽癌患者预后不良有关。此外,lnc-MRPL39-2:1通过直接与Hu-抗原R(HuR)相互作用来诱导体内和体外β-Catenin的表达上调,从而诱导鼻咽癌的生长和侵袭。Lnc-MRPL39-2:1的表达也被microRNA(miR)-329抑制。因此,这些发现表明lnc-MRPL39-2:1在鼻咽癌肿瘤发生和转移中至关重要,并突出了其作为鼻咽癌预后标志物和治疗靶点的潜力。

Fig4. Lnc-MRPL39-2:1在体内促进鼻咽癌细胞的增殖和转移
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37215987/
05
长链非编码RNA #61通过其长臂环发挥了广泛的抗流感病毒作用
发表期刊:Antiviral Res
影响因子:10.10
发表时间:2023年5月18日
越来越多的证据表明,长链非编码RNAs(lncRNAs)在调节基因表达方面具有关键作用。然而,甲型流感病毒(IAV)-宿主lncRNA相互作用的功能意义和机制仍然不清楚。本研究确定了一个功能性lncRNA LncRNA#61,作为一种广泛的抗IAV因子。LncRNA#61在不同亚型的IAV中高度上调,包括人类H1N1病毒和禽类H5N1和H7N9病毒。此外,核富集的LncRNA#61可以在IAV感染后很快从细胞核转移到细胞质中。LncRNA#61的强制表达极大地阻碍了IAV各种亚型的病毒复制,包括人类H1N1病毒和禽类H3N2/N8、H4N6、H5N1、H6N2/N8、H7N9、H8N4、H10N3、H11N2/N6/N9病毒。相反,抑制LncRNA#61表达实质上有利于病毒复制。更重要的是,脂质纳米颗粒(LNP)包封策略递送的LncRNA#61在抑制小鼠病毒复制方面表现出良好的性能。有趣的是,LncRNA#61参与了病毒复制周期的多个步骤,包括病毒进入、病毒RNA合成和病毒释放期。机制上,LncRNA#61的四个长环臂主要介导其广泛的抗病毒作用,并有助于其抑制病毒聚合酶活性和关键聚合酶组分的核聚集。因此,研究人员将LncRNA#61定义为IAV的潜在广谱抗病毒因子。本研究进一步扩展了我们对lncRNAs惊人和意想不到的生物学特性以及它们与IAV的密切相互作用的理解,为开发针对宿主lncRNAs的新型广泛抗IAV疗法提供了有价值的线索。

Fig5. 四个长环臂主要介导LncRNA#61的抗IAV活性
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37196902/










