广州市锐博生物科技有限公司品牌商
18 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
推荐产品
公司新闻/正文
J Exp Clin Cancer Res丨新型circPAK1通过多种机制在HCC中发挥作用
616 人阅读发布时间:2022-12-12 08:59
近几十年来,肝细胞癌(HCC)的发病率和死亡率不断上升。HCC的治疗是一种以根治性切除为基础的综合治疗模式,目前仍缺乏有效的分子治疗靶点。尽管在改善治疗方案方面已经做出了巨大的努力,但HCC仍然与预后不良有关。因此,迫切需要对HCC发病的分子机制进行研究。
环状RNAs(circRNAs)是新发现的非编码RNAs的成员,最初被认为是pre-mRNA剪接错误的无功能产物。然而,越来越多的circRNAs已被鉴定和研究,它们在生物体中的作用已逐渐被发现,并被认为是普遍存在的调节分子。大量研究指出,circRNA与包括HCC在内的肿瘤的发病机制密切相关。与circRNA相关的经典研究机制包括分子海绵、m6A修饰、RNA结合蛋白、翻译等。此外,circRNA还可以通过细胞外囊泡转运,这有可能影响肿瘤细胞的化学敏感性,并作为治疗恶性肿瘤的化疗药物的靶标。此外,基于circRNA的疫苗已经设计成功,该疫苗无需核苷酸修饰即可通过体外转录快速生成,具有较强的稳定性。上述所有内容都表明circRNA具有广泛的研究价值。然而,大量的circRNAs仍有待发现和研究。
近日,Journal of Experimental & Clinical Cancer Research(IF12.658)期刊在线发表了一篇题为CircPAK1 promotes the progression of hepatocellular carcinoma via modulation of YAP nucleus localization by interacting with 14-3-3ζ的研究论文。报道了一个新型circRNA CircPAK1,其在HCC肿瘤组织和细胞系中高表达,并与HCC患者预后不良相关。并揭示了circPAK1通过与14-3-3ζ相互作用调节YAP核定位从而促进HCC进展的分子机制,暗示circPAK1可能是HCC患者潜在的治疗靶点。

首先,为了确定参与HCC进展的circRNAs,研究人员对HCC和配对的正常肝组织进行了高通量测序,并结合一系列过滤条件,鉴定出一个显著上调的新型circRNA circPAK1(来源于染色体11:77085372-77,103,586,由PAK1基因中相邻的4个外显子组成),FISH和qRT-PCR结果表明,circPAK1主要位于细胞质中。
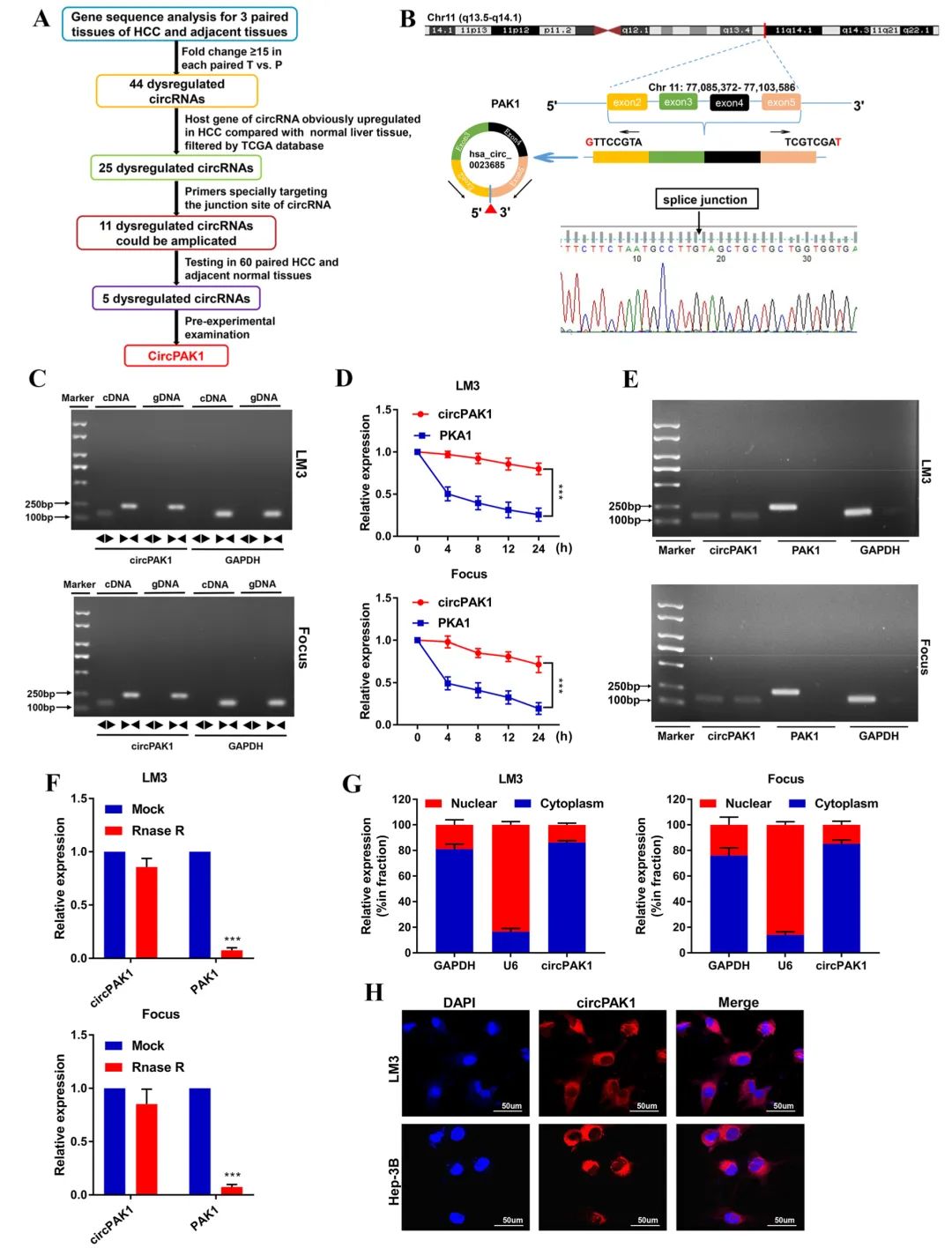
Fig1. circPAK1的鉴定
进一步的qRT-PCR检测发现,circPAK1在HCC组织和细胞系中显著上调,circPAK1的高表达与肿瘤大小、LN转移、TNM分期和MVI呈负相关。此外,与低表达组相比,高表达组患者的总生存期和无病生存期较差。
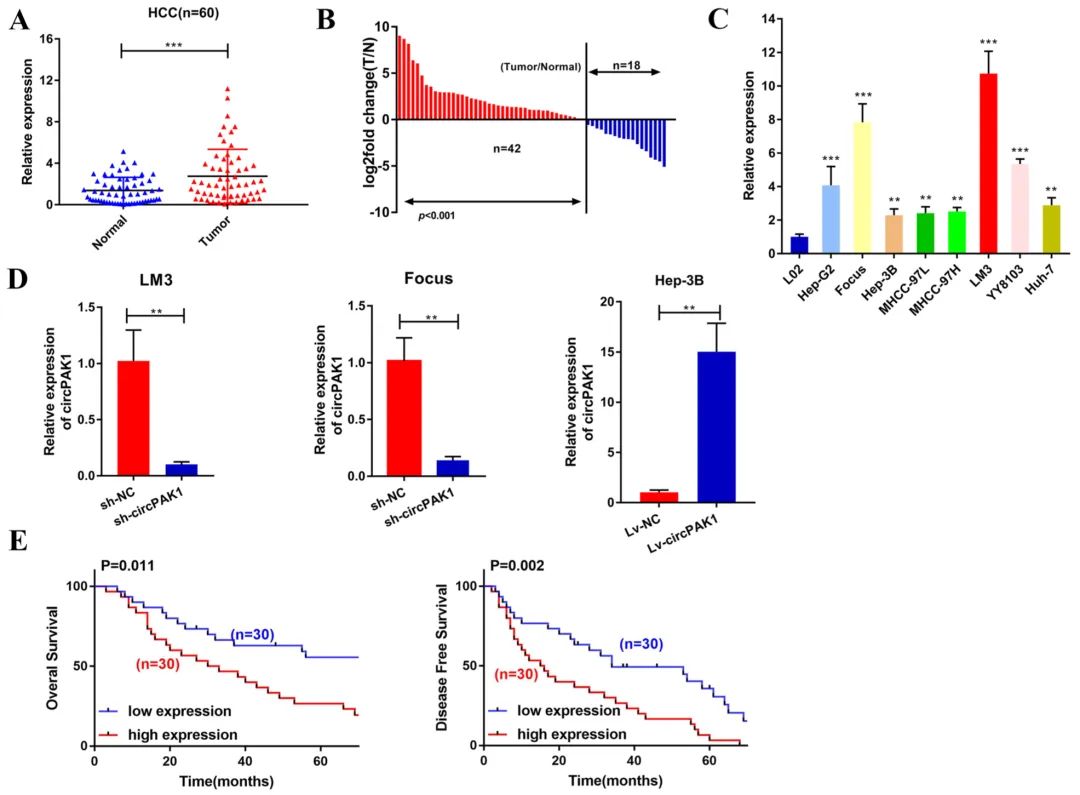
Fig2. circPAK1在HCC中的特征
接着,研究人员通过一系列体外和体内实验探索了circPAK1对肝癌细胞增殖、侵袭、转移和凋亡的影响。结果表明,circPAK1敲低抑制了HCC细胞的增殖、迁移、侵袭和血管生成,而circPAK1过表达导致HCC的细胞凋亡抑制和血管生成,促进了HCC的发展。动物实验也证实了circPAK1促进了HCC的生长和转移。
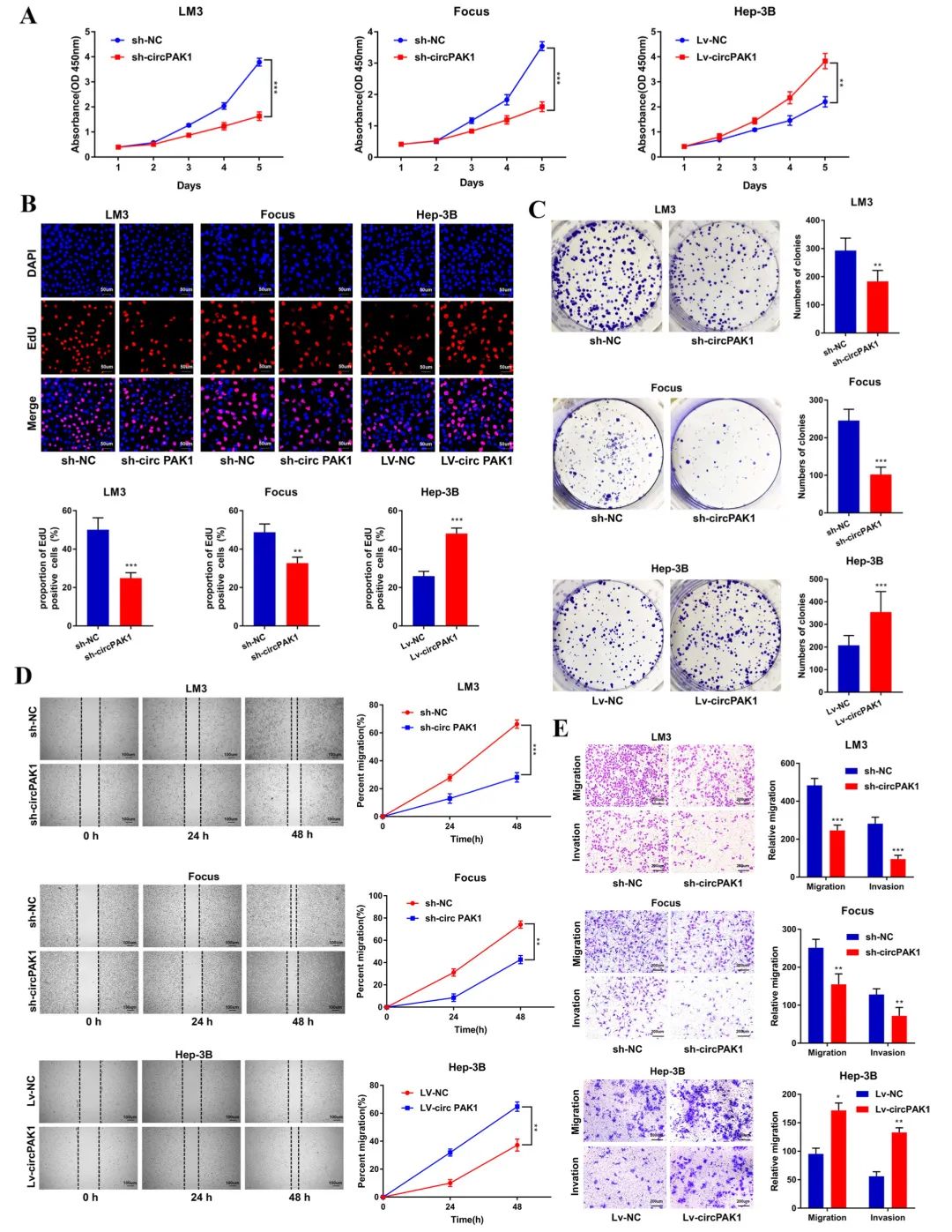
Fig3. CircPAK1促进HCC增殖、迁移和侵袭
此外,研究人员还使用壳聚糖材料制备了CS/si-circPAK1纳米复合物,以模拟基因靶向治疗。令人惊讶的是,通过皮下异种移植和肺转移模型发现,CS/si-circPAK1纳米复合物可以有效抑制HCC的生长和转移,甚至优于动物级si-circPAK1。这些发现可能为构建HCC circPAK1靶向药物带来启发。
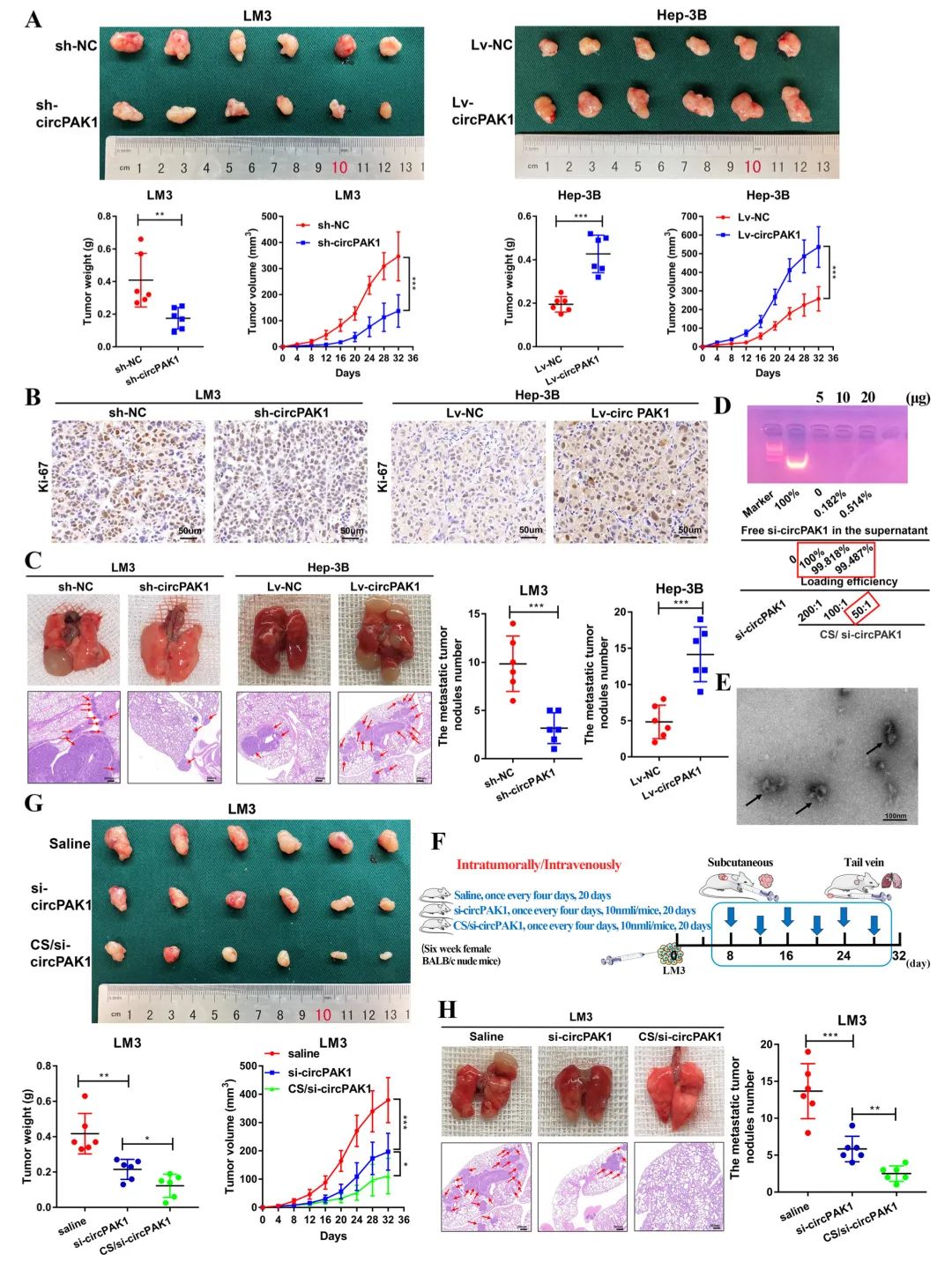
Fig4. CS/si-circPAK1纳米复合物在体内抑制HCC生长和转移
随后,为了探索circPAK1参与HCC发展的分子机制,研究人员进行了高通量测序、RNA测序、RNA探针pull-down、RNA免疫沉淀和免疫共沉淀等实验,以探讨circPAK1、14-3-3ζ、p-LATS1与YAP之间的关系。结果显示,circPAK1通过使Hippo信号通路失活来促进HCC的进展,这种信号通路失活是基于circPAK1与YAP竞争性结合14-3-3ζ,削弱14-3-3ζ对YAP的募集和胞质固定,从而促进YAP核的定位。
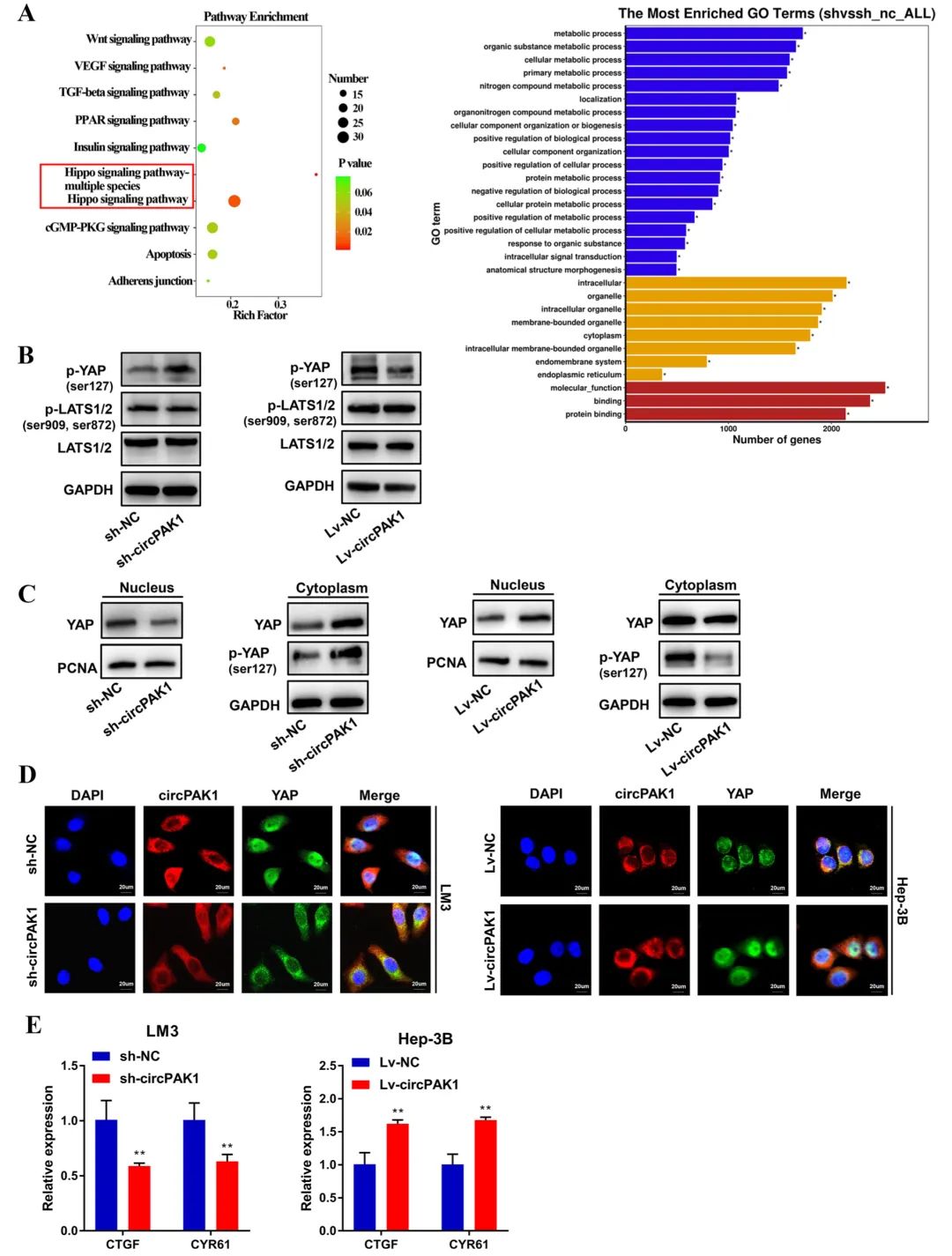
Fig5. CircPAK1通过失活Hippo信号通路介导HCC的致癌作用
最后,研究人员还证明了一种由乐伐替尼耐药细胞释放的外泌体介导circPAK1转移和乐伐替尼耐药传递的新机制。为了研究circPAK1是否参与介导肝癌乐伐替尼耐药,研究人员使用从乐伐替尼耐药HCC细胞系分离的外泌体来评估外泌体circPAK1与乐伐替尼耐药之间的关系。结果显示,circPAK1可以通过外泌体从乐伐替尼耐药细胞运输到敏感细胞,从而诱导接收细胞的乐伐替尼耐药。本研究发现可能使外泌体circPAK1成为液体活检中早期鉴定乐伐替尼耐药的有希望的生物标志物,并为克服乐伐替尼耐药提供新思路。
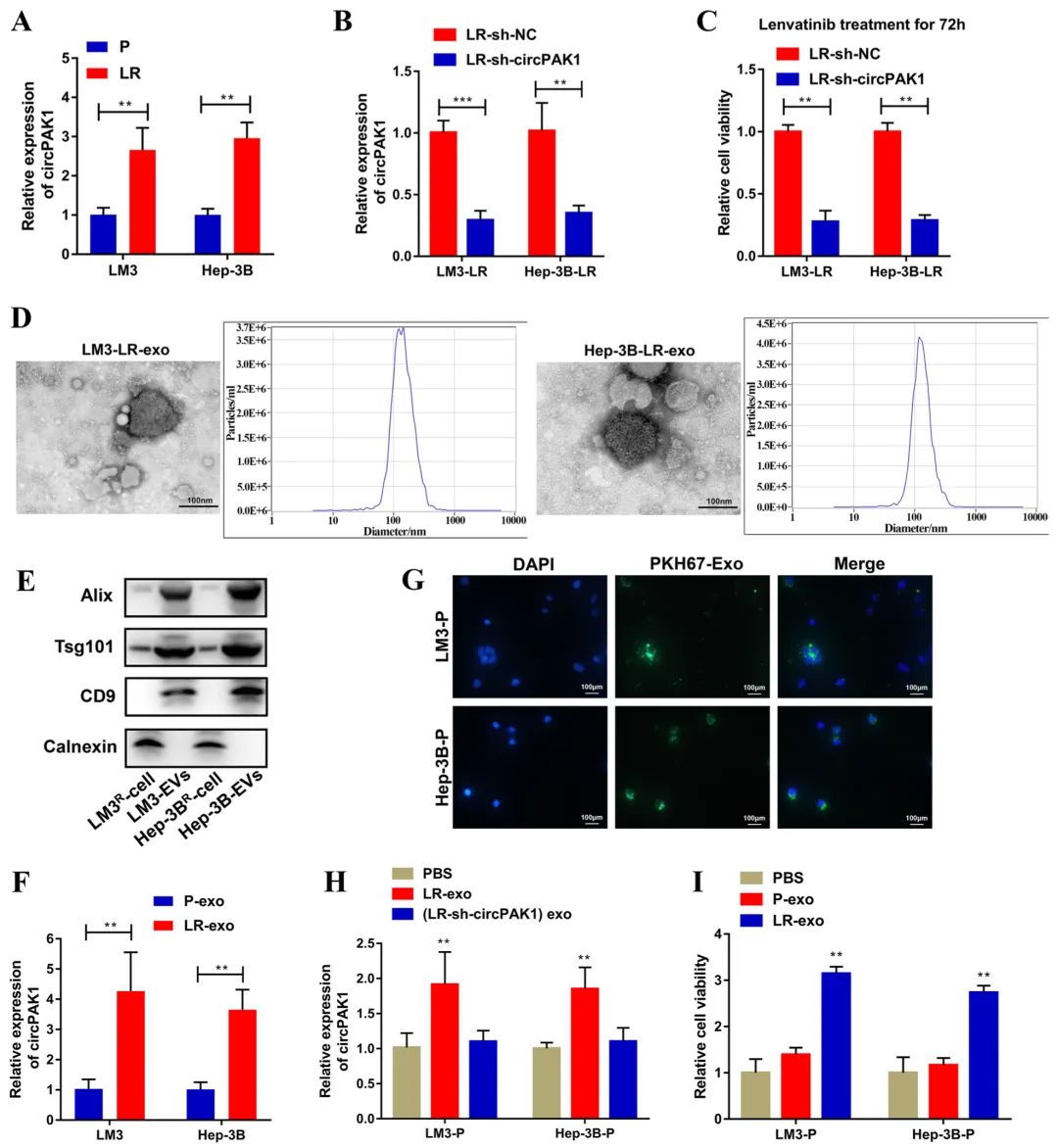
Fig6. CircPAK1通过外泌体传递乐伐替尼耐药
总之,本研究结果表明circPAK1通过与YAP竞争性结合14-3-3ζ介导YAP的细胞核定位,通过关闭Hippo信号通路导致HCC的进展。CS/si-circPAK1纳米复合物对抑制HCC体内生长和转移具有良好的效果。本研究还报道了一种新机制,通过这种机制,HCC衍生的外泌体传递circPAK1并促进了lenvatinib耐药性在HCC细胞中的传递。综上所述,circPAK1可能是HCC患者潜在的治疗靶点,并开发有效策略来逆转乐伐替尼耐药。
原文链接:
https://jeccr.biomedcentral.com/articles/10.1186/s13046-022-02494-z
本研究中使用到的circRNA动物用siRNA、生物素标记circRNA探针、circRNA FISH探针及FISH试剂盒产品均由锐博生物提供!更过关于circRNA研究产品与服务信息,欢迎登陆锐博生物官网(www.ribobio.com)进行查询或来电咨询!

RiBoBio新品上市!
* 锐博生物T7 mRNA转录试剂盒采用优化的帽结构类似物Ribo-Cap1,仅需一步共转录加帽即可完成mRNA的体外合成,加帽率可稳定在90%以上
* 与抗反帽ARCA相比,Ribo-cap1与GTP无竞争,不影响RNA的产率, 1μg模板投入量可产生70-150μg的mRNA
* 使用Ribo™ T7 mRNA转录试剂盒还可根据需求对单个或多个核苷酸单体进行替换,制备特殊化学修饰的mRNA
* 锐博生物可提供的修饰核苷包括N1-methylpseudo-UTP、5-Me-CTP、5-OMe-UTP、Pseudo-UTP等