推荐产品
公司新闻/正文
IF11+客户文章丨miR-145启动子介导的SOX9-CLDN8通路的高甲基化调节克罗恩病的肠粘膜屏障
人阅读 发布时间:2022-12-02 01:04
肠屏障损伤在克罗恩病(CD)的发病机制中起重要作用,而claudins(CLDNs)功能障碍是导致肠黏膜损伤的重要原因。SOX9是一种重要的转录因子,在CD患者病损结肠中表达上调;然而,它在CD中的确切作用在很大程度上仍然未知。近日,柳叶刀子刊eBioMedicine(IF11.205)期刊发表了一篇题为Hypermethylation of miR-145 promoter-mediated SOX9-CLDN8 pathway regulates intestinal mucosal barrier in Crohn's disease的研究论文,探索了SOX9和CLDN之间的相互作用,并进一步阐明CD的潜在机制。
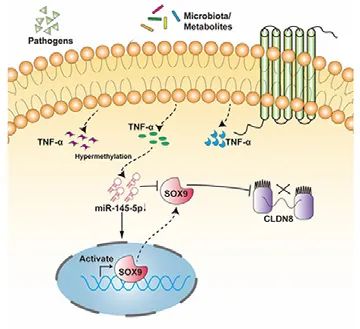
miR-145-5p/SOX9/CLDN8通路模型
研究结果
1、SOX9在CD病损黏膜中表达上调
首先,研究人员使用GEO数据库进行基因表达分析,以研究SOX9在CD患者中的表达谱。结果显示,CD患者中的SOX9表达似乎高于HCs(健康队照)。此外,另外36个样本(包括恶化和不显症状的UC(溃疡性结肠炎)和CD,感染性结肠炎和HCs患者)的表达谱显示,在受疾病影响的结肠中发现SOX9表达高于未受影响的结肠。随后的RT-qPCR、免疫印迹和IHC实验证实了与HCs相比,CD患者中的SOX9在mRNA水平上显著上调(约4倍)。此外,在TNBS诱导的结肠炎小鼠模型的肠粘膜中,在mRNA和蛋白质水平上也观察到Sox9表达的上调。

Fig1. SOX9在CD和TNBS诱导的结肠炎小鼠中表达上调
2、SOX9在结肠细胞中诱导连接紧密性损伤
TEER(跨膜电阻,可评估肠上皮细胞的细胞旁通透性和TJs紧密性)和细胞旁通透性实验可用于评估Caco-2细胞单层模型中肠粘膜屏障的失调。接下来,研究人员通过在Caco-2细胞中过表达或敲低SOX9来研究其在调节TJs(紧密连接)中的作用。结果发现,SOX9过表达(pcDNA-SOX9)显著降低了TEER,而敲低SOX9(si-SOX9)显著增强了上皮细胞的TJs。此外,敲低SOX9显著降低了FD4通透性,而过表达SOX9导致FD4通透性增加。表明SOX9可能通过调节潜在的TJs而对肠上皮屏障功能产生不利影响。

Fig2. SOX9在结肠细胞中诱导连接紧密性损伤
3、CD黏膜中SOX9表达与CLDN8呈负相关
生物分析显示SOX9与CLDN8启动子区域存在几个假定结合位点。此外,在CD和TNBS诱导的结肠炎患者中观察到CLDN8表达的下调。因此,研究人员密切关注SOX9-CLDN8通路。随后的研究发现,转染pcDNA-SOX9会导致Caco-2和NCM460细胞中的CLDN8在mRNA和蛋白质水平上显著降低。相反,当转染si-SOX9导致肠上皮细胞中的SOX9敲低时,CLDN8的mRNA和蛋白表达升高。暗示SOX9可能直接调控CLDN8的转录。

Fig3. CD黏膜中SOX9表达与CLDN8呈负相关
为了阐明SOX9介导CLDN8下调的潜在机制,研究人员进行了双荧光素酶报告基因和ChIP-qPCR实验,以研究SOX9作为转录因子对CLDN8启动子活性的调节作用。结果显示,在与SOX9过表达质粒共转染的293T细胞中,使用含有2.0 kb CLDN8启动子片段的质粒获得的荧光素酶活性显著降低。此外,ChIP-qPCR实验发现SOX9与CLDN8启动子区域的染色质相关,而不是较远的编码区域(不包含假定的SOX9结合基序)。这表明SOX9可能直接影响CLDN8的表达。

Fig4. SOX9通过结合CLDN8启动子负调节结肠上皮细胞中的CLDN8
4、miR-145-5p靶向结肠上皮细胞中的SOX9-CLDN8通路
为了进一步阐明靶向SOX9-CLDN8通路在调节CD患者肠上皮屏障的上游调控机制,本研究重点关注了miRNAs的作用,并将miR-145-5p鉴定为在3'UTR区域靶向SOX9的潜在上游分子。随后的双荧光素酶报告基因实验证实了miR-145-5p特异性靶向SOX9 3’UTR以抑制相应mRNA的表达。接下来,为了探索了miR-145-5p在SOX9中的调节作用,研究人员将miRNA mimic和inhibitor转染到Caco-2、SW480和NCM460细胞中。结果发现,miR-145-5p过表达抑制了所有肠上皮细胞中SOX9在mRNA和蛋白水平上的表达。然而,当这些细胞系转染miR-145-5p抑制剂时,仅在Caco-2细胞中观察到SOX9表达水平升高。这些结果证实了SOX9在肠上皮细胞中的表达受上游miR-145-5p负调控的观点。
随后,研究人员探索了miR-145-5p对TJs的影响。结果发现,Caco-2细胞单层模型转染mimic后,TEER值显著升高,FD4通透性降低;相反,转染inhibitor后,单层细胞TEER降低,FD4通透性增加。此外,miR-145-5p过表达显著增加了CLDN8和CLDN15的表达。总的来说,以上结果表明miR-145-5p是维持正常肠上皮屏障功能所必需的,并且它可能在SOX9-CLDN8通路中发挥重要作用。

Fig5. 鉴定靶向SOX9以调节肠粘膜屏障功能的miR-145-5p
5、miR-145-5p agomir可减轻WT小鼠TNBS诱导的结肠炎
为了阐明miR-145-5p在CD中的保护作用并研究其抑制剂的治疗效果,研究人员对TNBS诱导的结肠炎小鼠腹腔注射miR-145-5p agomir。结果显示,miRNA agomir治疗可减轻小鼠结肠炎症并显著恢复体重减轻。此外,治疗组经miR-145-5p agomir治疗后,肠道炎症和结肠髓过氧化物酶(MPO)活性得到缓解、组织学评分下降、FD40通透性显著更大的降低。重要的是,补充miRNA agomir可通过增加TNBS诱导的结肠炎小鼠中miR-145-5p的水平,降低Sox9的表达,并恢复Cldn8的表达。

Fig6. miR-145-5p agomirs在TNBS诱导的结肠炎小鼠中的治疗作用
为了证明miR-145/SOX9/CLDN8通路在结肠炎发生中的作用,研究人员进一步在Cldn8基因敲除小鼠中进行了一系列实验,以确认其在结肠炎启动中的作用。结果发现,Cldn8-/-小鼠经miR-145-5p agomir治疗后,不能减轻肠道炎症和改善结肠炎的各种主要体征。相反,当给药miR-145-5p agomir时,Cldn8-/-小鼠的体重减轻、MPO活性和组织学评分没有显著恢复,同时伴有FD40通透性增加。值得注意的是,外源性miR-145-5p补充剂抑制了动物模型结肠组织中的Sox9表达。本研究的动物实验结果表明,在不影响Cldn8表达的前提下,miR-145-5p治疗通过下调Sox9靶基因改善了体内TNBS诱导的结肠炎的炎症。

Fig7. Cldn8敲除小鼠中miR-145-5p agomirs的治疗作用
6、miR-145的启动子高甲基化导致其在CD中的下调
最后,研究人员试图探索与miR-145-5p在CD患者中下调相关的潜在机制。通过数据库分析发现,在miR-145的启动子中没有CpG岛,但检测到6个具有潜在甲基化特性的CpG位点。为了确定甲基化的存在,研究人员通过焦磷酸测序定量了粘膜活检样品中启动子的甲基化比例。结果发现,CD患者的总DNA甲基化比率显著升高。此外,-156 CpG位点比其他CpG位点的甲基化程度更高。随后,研究人员在体外分析炎症条件下miR-145编码基因的启动子甲基化水平。发现50 ng/mL的TNF-α和5 μmol/L的5-aza对miR-145-5p的表达有显著影响;因此,这些浓度被用于后续的实验。

Fig8. miR-145启动子的高甲基化抑制miR-145-5p的表达
此外,本研究探索了50 ng/mL TNF-α诱导的miR-145-5p表达降低是否通过异常甲基化介导,以及5 μmol/L的5-aza用于逆转高甲基化。结果发现,当加入5-aza,TNF-α刺激的NCM460细胞中miR-145-5p的表达得到挽救,SOX9和CLDN8的表达在mRNA和蛋白水平上也被逆转。甲基化分析显示,TNF-α刺激导致miR-145启动子区域的异常高甲基化,而TNF-α联合5-aza处理的NCM460细胞防止了高甲基化的发生。然而,与CD患者不同的是,-156和-432 CpG位点比其他位点更容易甲基化。这些结果表明,miR-145启动子失活发生在高甲基化之后,这可能支持miR-145-5p在CD中的表达下降。

Fig9. miR-145启动子介导的SOX9-CLDN8通路的高甲基化
接着,研究人员在Caco-2细胞单层中进行TEER和经上皮FD4通透性测定,以进一步研究miR-145启动子高甲基化对Caco-2细胞间TJs的影响。结果发现,Caco-2细胞经TNF-α处理后,TEER降低,FD4通透性增加。然而,与5-aza联合治疗显著减弱了这种对肠屏障的影响,表现为TEER增加,FD4通透性降低。证实了miR-145启动子介导的SOX9-CLDN8通路中发生高甲基化,以调节CD中的肠黏膜屏障。

Fig10. Caco-2细胞单层TEER和FD4通透性
原文链接:
https://www.sciencedirect.com/science/article/pii/S2352396422000305
本研究使用到的miRNA mimic、inhibitor及其NC、动物用miRNA agomir、miRNA靶基因3’UTR报告基因载体、siRNA产品均由锐博生物提供!更过关于miRNA研究产品与服务信息,欢迎登陆锐博生物官网(www.ribobio.com)进行查询或来电咨询!

新品上市!
* 锐博生物T7 mRNA转录试剂盒采用优化的帽结构类似物Ribo-Cap1,仅需一步共转录加帽即可完成mRNA的体外合成,加帽率可稳定在90%以上
* 与抗反帽ARCA相比,Ribo-cap1与GTP无竞争,不影响RNA的产率, 1μg模板投入量可产生70-150μg的mRNA
* 使用Ribo™ T7 mRNA转录试剂盒还可根据需求对单个或多个核苷酸单体进行替换,制备特殊化学修饰的mRNA
* 锐博生物可提供的修饰核苷包括N1-methylpseudo-UTP、5-Me-CTP、5-OMe-UTP、Pseudo-UTP等










