推荐产品
公司新闻/正文
J Hematol Oncol(IF23+)丨锐博动物用ASO助力发现SE劫持的LINC01977可作为早期LUAD潜在治疗靶点
人阅读 发布时间:2022-10-28 23:28
肺癌是世界范围内癌症相关死亡的主要原因,其中最常见的组织学亚型是肺腺癌(LUAD),占所有病例的40%以上。手术切除联合或不联合辅助化疗和/或辅助放疗是早期LUAD患者的标准治疗方法。然而,这些患者中有许多会在5年内复发,从I期疾病患者的复发率为20%到III期疾病患者的复发率为50%,从而导致患者的预后不佳。尽管循环肿瘤DNA(ctDNA)检测已被证明是一种基于微小残留疾病(MRD)以鉴定疾病复发高风险患者的有效方法,但重要的是要揭示导致早期LUAD患者复发的机制。
对癌症基因组和驱动事件的更好理解彻底改变了对具有基因组驱动改变的患者的治疗,这些改变可以用匹配的药物对其进行靶向治疗。针对EGFR突变以及ALK和ROS1融合事件的靶向治疗显著提高了LUAD患者的生存率。然而,迄今为止,癌症基因仅在转移性疾病背景下的突变尚未被鉴定。动态表观遗传改变,如增强子重编程和超级增强子(SE)劫持事件,现在被认为是转移的关键驱动因素。目前尚不清楚SE是否是LUAD转移的关键驱动因素,特别是在早期疾病患者中。
超级增强子是指具有丰富增强子活性的大型基因组结构域,可募集核心调节回路转录因子(TFs)来介导人类癌症的转录失调。之前的研究证明了ELF3、EHF和TGIF1形成了一个SE依赖性转录调节网络,以扰乱LUAD中的转录事件。SEs还会生成增强子RNAs(eRNAs)或劫持启动子以上调非编码RNAs,即超级增强子相关长链非编码RNAs(SE-lncRNAs)。据报道,TP63和SOX2通过激活鳞状细胞癌中lncRNA CCAT1的SE和启动子来共同调节其表达。由SE和TP63调节的LINC01503激活ERK和AKT通路,促进鳞状细胞癌的进展。然而,在LUAD中,被SEs劫持的lncRNAs的功能仍然未知。
TGF-β是一种分泌的细胞因子,可激活SMAD2和SMAD3,它们与SMAD4结合形成三聚体复合物,并易位至细胞核中。典型的TGF-β/SMAD3通路对于LUAD患者的恶性进展至关重要。SMAD3中的单核苷酸多态性(SNPs)高度预测吉非替尼治疗后LUAD患者的预后。此外,据报道,TGF-β可促进TAMs中程序性死亡配体1(PD-L1)的表达,而与PD-1抑制剂(帕博利珠单抗)相比,anti-PD-L1/TGF-β trap(M7824)治疗NSCLC的3期临床试验未显示具有显著的治疗益处,因此,临床试验终止了。肿瘤微环境中的M2样肿瘤相关巨噬细胞(TAM2)是TGF-β的主要来源。然而,癌细胞对外源性TME中TAM2高浸润的反应机制和适应性行为是否依赖于涉及SEs活性的内在特征仍然是未知的。
近日,Journal of Hematology & Oncology(IF23.168)期刊发表了一篇题为Super-enhancer hijacking LINC01977 promotes malignancy of early-stage lung adenocarcinoma addicted to the canonical TGF-β/SMAD3 pathway的研究论文。该研究探索了LUAD中失调的SE相关lncRNAs,确定了上调的LINC01977被SE劫持。揭示了LINC01977通过促进SMAD3的核积累和增强SMAD3/CBP/P300复合物的建立,参与了TGF-β/SMAD3通路,导致上皮-间充质转化(EMT)的中心开关ZEB1的表观遗传激活,从而促进早期LUAD恶性表型的作用机制。表明了SE劫持的LINC01977可能是一个有价值的治疗靶点,特别是对早期LUAD的治疗。

为了表征由SEs调控的失调的lncRNAs,研究人员对来自LUAD患者的5对肿瘤和邻近正常组织进行了超级增强子相关lncRNA(SE-lncRNA)微阵列分析。结果显示,与正常组织相比,恶性组织中有515个lncRNAs存在差异表达,其中189个显著上调,326个显著下调。通过与TCGA中失调的lncRNA进行重叠分析,获得了55个失调的lncRNAs,其中18个lncRNA转录本已在NCBI中得到验证。研究人员将注意力集中在转录本LINC01977上,由于:①它是分析中差异表达最显著的lncRNA;②定位于17q25.3,据报道其基因组不稳定性与NSCLC的恶性进展有关;③对GTEx数据集的分析表明,LINC01977在正常睾丸中显示出高表达,参阅癌症睾丸基因,其在肿瘤发生和进展中具有潜在作用。此外,公共数据库泛癌分析显示,LINC01977在癌细胞系和LUAD肿瘤组织中高表达,qRT-PCR检测验证了这一点。原位杂交和Kaplan–Meier生存分析表明LINC01977在LUAD组织中高度表达,与较差的总生存期相关。

Fig1. 鉴定LUAD中SE相关的lncRNAs
由于LINC01977被注释为SE相关lncRNA,因此研究人员评估了SE对LINC01977转录调控的影响。研究人员在ENCODE数据库中的典型 LUAD 细胞系(A549和PC-9)和正常肺组织中挖掘了H3K27ac和H3K4me1 ChIP-seq数据(SE的活性标记),并在A549细胞中鉴定出位于LINC01977上游异常活化的SE区域,其跨度为48kb。此外,来自公共数据库A549细胞的Hi-C数据突出显示,SE区域直接与LINC01977的启动子区域相互作用。为了阐明在A549细胞中鉴定的SE区域是否会影响LINC01977的转录,研究人员将LINC01977的SE区域分为6个组分(E1-E6),设计为双荧光素酶报告基因质粒,其中包含LINC01977启动子区域。结果发现,与从ChIP-seq数据中获得的SE特异性峰一致,与PC-9细胞相比,A549细胞中的大多数SE亚区域(5/6)普遍更高。结果表明,SE对A549细胞LINC01977具有较强的转录增强活性,而对PC-9细胞具有中等的转录增强活性。

Fig2. LINC01977是一种超级增强子相关的癌症睾丸lncRNA
为了研究LINC01977在LUAD恶性进展中的作用,研究人员选择靶向LINC01977的ASO进行了体外和体内功能缺失性实验。结果显示,LINC01977的缺失抑制了LUAD细胞系的增殖,阻碍了G1/S细胞周期转化,增加了细胞凋亡,显著减少了细胞迁移和侵袭,并降低了LUAD细胞的克隆形成。表明LINC01977的缺失在体外抑制了LUAD细胞的增殖和恶性表型。

Fig3. LINC01977在体外具有致癌作用
接下来,研究人员探索了LINC01977在体内的生物学功能。通过向裸鼠注射A549细胞建立皮下荷瘤模型,然后每3天瘤内注射LINC01977-ASO或对照组。结果显示,与对照组相比,注射LINC01977-ASO的肿瘤体积小、重量轻、生长迟缓。此外,研究人员评估了抑制LINC01977是否影响异种移植物转移模型中的肿瘤转移。结果显示,LINC01977-ASO抑制了远处转移的形成。以上结果表明LINC01977作为一种致癌基因促进了LUAD的恶性进展。
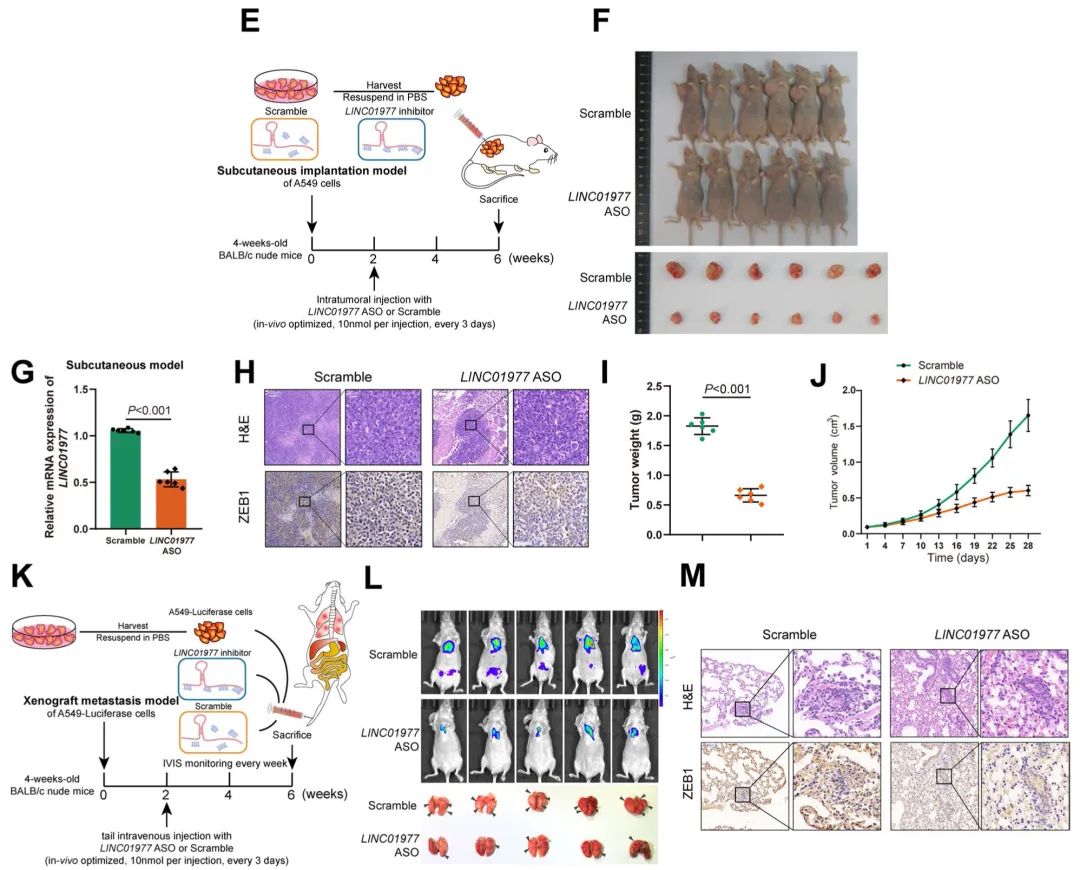
Fig4. LINC01977在体内具有致癌作用
机制研究表明,LINC01977与SMAD3相互作用以诱导其核转运,从而促进了SMAD3与CBP / P300之间的相互作用,从而调节了下游靶基因ZEB1。此外,SMAD3通过同时结合启动子和SE上调LINC09177的转录,这是由M2样肿瘤相关巨噬细胞(TAM2)的浸润诱导的,随后激活TGF-β/ SMAD3通路,从而促进早期LUAD的恶性进展。

Fig5. LINC01977通过典型的TGF-β/SMAD3吐了促进恶性肿瘤的作用机制示意图
最后,为了研究LINC01977和TAM2浸润(LUAD中最丰富的基质细胞群)之间的相关性,研究人员评估LINC01977和TAM2的表达。结果显示,LINC01977在早期LUAD中高表达,而TAM2在侵袭边缘显著富集。相关性分析表明,LINC01977与早期LUAD中的TAM2浸润和SMAD3表达呈正相关。此外,在TGF-β高表达的LUAD患者中观察到LINC01977的SE区域染色质可及性更高。LIN01977高表达的早期LUAD患者的无病生存期较短。表明LINC01977是早期LUAD预后不良的有希望的预测因子。

Fig6. LINC01977是早期LUAD预后不良的有希望的预测因子
总之,本研究结果表明,SE-LINC01977是早期LUAD转移和无病生存期较差的有希望的预测因子。机制上,机制上,LINC01977通过促进SMAD3的核积累和增强SMAD3/CBP/P300复合物的建立,参与了TGF-β/SMAD3通路,导致上皮-间充质转化(EMT)的中心开关ZEB1的表观遗传激活。此外,LINC01977表达与TAM2浸润和SMAD3表达呈正相关。LINC01977高表达的LUAD患者的无病生存期较短,特别是在早期。本研究揭示了癌细胞对外源性高TAM2浸润的内在反应不仅是由于TGF-β信号通路的激活,而是充分利用异常激活的SE来获得早期LUAD转移的肿瘤微环境的益处。
原文链接:
https://link.springer.com/article/10.1186/s13045-022-01331-2#Abs1
本研究使用到的lncRNA动物用ASO及对照产品、细胞用ASO、FISH探针&试剂盒、T7体外转录试剂盒均由锐博生物提供!更过关于lncRNA研究产品与服务信息,欢迎登陆锐博生物官网(www.ribobio.com)进行查询或来电咨询!

RIBOBIO

新品上市!
* 锐博生物T7 mRNA转录试剂盒采用优化的帽结构类似物Ribo-Cap1,仅需一步共转录加帽即可完成mRNA的体外合成,加帽率可稳定在90%以上
* 与抗反帽ARCA相比,Ribo-cap1与GTP无竞争,不影响RNA的产率, 1μg模板投入量可产生70-150μg的mRNA
* 使用Ribo™ T7 mRNA转录试剂盒还可根据需求对单个或多个核苷酸单体进行替换,制备特殊化学修饰的mRNA
* 锐博生物可提供的修饰核苷包括N1-methylpseudo-UTP、5-Me-CTP、5-OMe-UTP、Pseudo-UTP等










