推荐产品
公司新闻/正文
Advanced Science丨小细胞外囊泡miRNA测序助力发现CRC来源的sEVs促进肿瘤免疫逃逸的机制
人阅读 发布时间:2022-02-08 17:13
结直肠癌(CRC)是全球最常见的癌症之一。CRC的发生发展不仅受遗传和表观遗传调控,而且与肿瘤微环境(TME),尤其是肿瘤免疫微环境密切相关。近十年来,免疫检查点阻断(ICB)因其在恶性实体瘤(如黑色素瘤和非小细胞肺癌)治疗中的良好疗效而备受关注。ICB疗法也被批准用于治疗具有DNA错配修复缺陷(dMMR)/MSI-H分子特征的CRC患者。然而,dMMR/MSI-H CRC亚组仅占CRC患者的15%,且大多数CRC患者不能从ICB治疗中获益。因此,研究CRC与免疫系统之间的相互作用,进而调节TME中的免疫细胞,可能为CRC的免疫治疗提供一种有效的策略。
巨噬细胞是TME中存在的最丰富的免疫细胞类型之一,它们被称为肿瘤相关巨噬细胞(TAMs)。之前的研究表明,TAMs通过分泌IL6来增加CRC细胞的化学抗性,并抑制药物诱导的细胞凋亡,IL6在CRC细胞中调节STAT3-miR-204轴。其他研究也报道了TAMs表达的PD-1抑制吞噬作用和抗肿瘤免疫,并且TAM衍生的CCL5通过p65/STAT3-CSN5-PD-L1通路促进CRC细胞的免疫逃逸。这些研究表明,TAMs可以抑制局部免疫并促进肿瘤免疫逃逸和进展,TAMs可能代表癌症免疫治疗的潜在靶点。然而,如何在CRC TME中培养TAMs仍然不清楚。
小细胞外囊泡(sEVs)是由细胞分泌的,直径为30-150nm的细胞外囊泡,已成为细胞间信号传导的重要调节因子和有前途的生物标志物。sEVs携带复杂的生物分子,包括蛋白质、脂质、DNA和RNA。在这些货物中,microRNAs(miRNAs)被认为是最重要的信号分子之一:1)miRNAs长度为21-25个核苷酸,可以有效地包裹到sEVs中;2)miRNAs稳定分布于各种组织和体液中;3)单个miRNA可以调控多个靶基因,反之,多个miRNA可以协同调控单个基因,形成高效灵活的基因调控模式。之前的研究已经证实了sEV介导的功能性miRNAs传递在TME的细胞间通讯中发挥关键作用。
近日,Advanced Science(IF16.806)期刊在线发表了题为Colorectal Cancer-Derived Small Extracellular Vesicles Promote Tumor Immune Evasion by Upregulating PD-L1 Expression in Tumor-Associated Macrophages的研究论文。报道了CRC来源的小细胞外囊泡通过上调肿瘤相关巨噬细胞(TAMs)的PD-L1表达促进肿瘤免疫逃逸的作用机制,为CRC免疫治疗提供了一个全新的靶点。

首先,研究人员发现CRC细胞中的PD-L1水平非常低,但在TAMs中PD-L1水平很高,并鉴定了一个PD-L1+CD206+巨噬细胞亚群,该亚群是在巨噬细胞浸润过程中由肿瘤细胞诱导的,且与预后不良相关。此外,研究发现基于巨噬细胞和CD8+ T细胞之间相互作用的PD-L1介导的免疫抑制导致了CRC TME内免疫的改变。然后,研究人员通过mIF和IHC染色来确定巨噬细胞中的PD-L1表达是否有助于TAM的免疫抑制功能。结果表明TAMs中的PD-L1可抑制CRC TME中的CD8+ T细胞。

Fig1. CRC TME中巨噬细胞相关免疫的改变
之前的研究揭示了免疫逃避和由肿瘤分泌的sEVs介导的肿瘤生长之间的主要联系。研究人员推测CRC来源的sEV负责CRC对TAMs的调节。实验结果显示CRC细胞在体外可以通过递送sEVs来培养巨噬细胞并促进巨噬细胞PD-L1的表达。接着,研究人员想确定这些sEVs是否可以在体内进入和调节巨噬细胞。结果发现CRC来源的sEVs可在体内培养巨噬细胞并促进PD-L1的表达。

Fig2. CRC细胞来源的sEVs可以培养巨噬细胞并促进巨噬细胞PD-L1的表达
机制研究表明,CRC细胞可以分泌被巨噬细胞吸收的小细胞外囊泡(sEVs),诱导M2样极化和PD-L1表达,导致CRC TME中PD-L1+CD206+巨噬细胞丰度增加和T细胞活性降低。sEV来源的miR-21-5p和miR-200a被鉴定为介导CRC对巨噬细胞调节作用的关键信号分子。进一步的研究表明,CRC来源的miR-21-5p和miR-200a通过调节PTEN/AKT和SCOS1/STAT1通路,协同诱导巨噬细胞M2样极化和PD-L1表达,导致CD8+ T细胞活性降低和肿瘤生长增加。
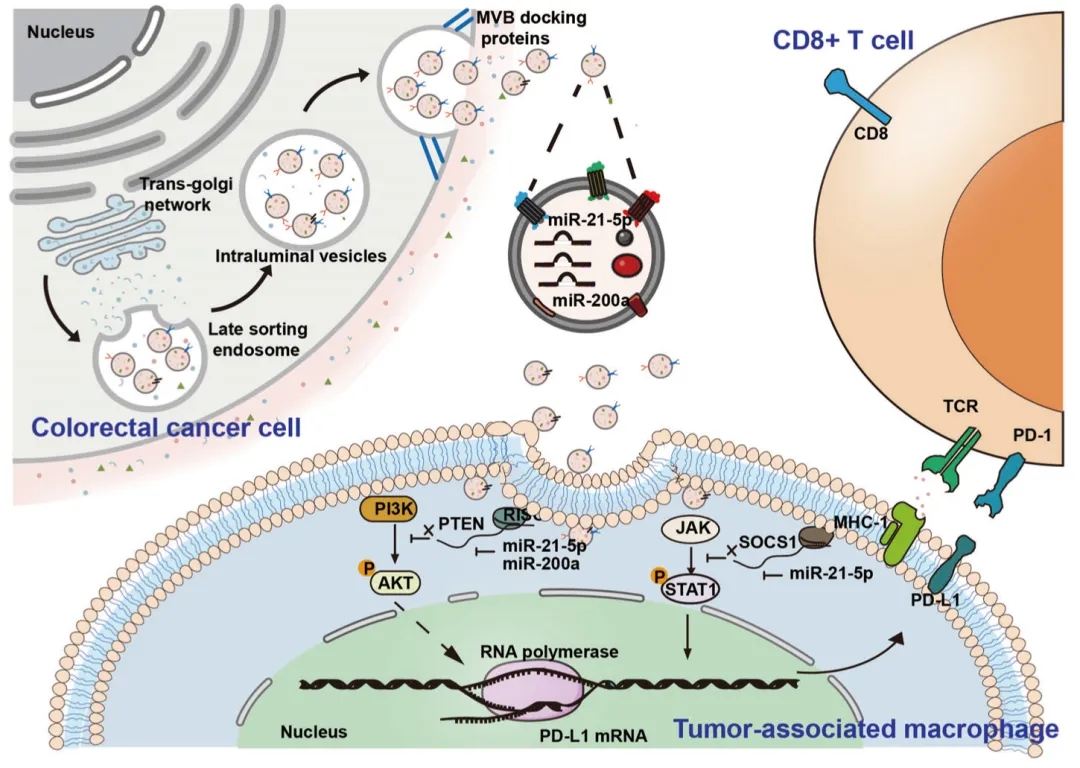
Fig3. CRC来源的sEVs可增强TAM中的PD-L1表达,然后抑制TME中的CD8+ T细胞并促进CRC肿瘤生长
总之,研究结果表明抑制CRC中特定sEV-miRNAs的分泌并靶向TAM中的PD-L1可作为CRC治疗的新方法,也是CRC中anti-PD-L1治疗的敏化方法。
原文链接:https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202102620
本研究涉及到的小细胞外囊泡miRNA测序服务由锐博生物提供!










